Science:对映选择性催化1,2-硼酸酯重排
有机硼化合物是一类很有价值的有机试剂,广泛应用于医药、农药、功能材料等的合成中。特别值得一提的是,手性纯烷基硼试剂的立体特异性转化是构建含碳和杂原子取代立体中心的强有力策略。如图1A所示,这些反应利用含α-离去基团的四配位硼酸酯衍生物的典型反应性(易发生1,2-重排),在带有离去基团的碳上表现为立体反转,在迁移碳上表现为立体保留。毫无疑问,这些重排反应在立体选择性合成中具有重要意义,例如:Matteson同系化反应通过二氯甲基取代硼酸酯的形成和重排进行碳链延伸(图1B),因此被认为是合成烷基硼酸酯的一个模板反应。事实上,当在硼上使用手性二醇助剂时,可以使该过程具有立体选择性。另外,这些非对映选择性重排反应的α-氯硼酸酯产物构型稳定,可以进行二次亲核加成和高立体定向重排,从而得到各种手性二醇取代的仲硼酸酯。
近日,美国哈佛大学的Eric N. Jacobsen教授(点击查看介绍)课题组从简单易得的硼酸酯和二氯甲烷出发合成了一系列α-氯频哪醇硼酸酯,后者在锂-异硫脲硼酸酯络合物的作用下实现了对映选择性催化1,2-硼酸酯重排反应(图1C)。需要指出的是,反应中产生的手性砌块可经历两个连续的立体特异性转化,从而获得一系列三取代立体中心。相关成果发表在Science 上。
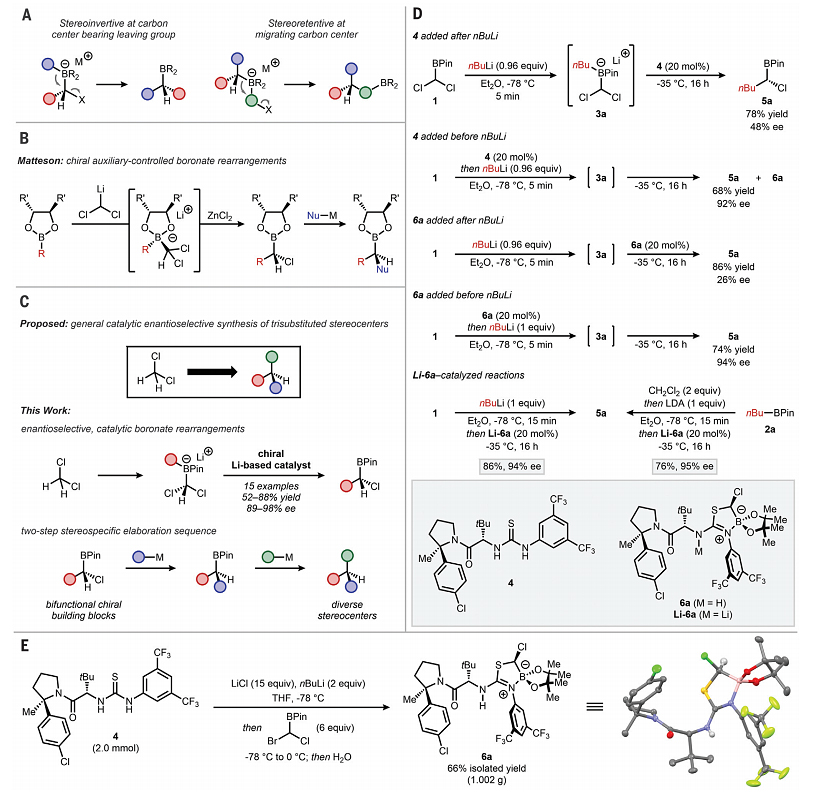
图1. 可控1,2-硼酸酯重排及反应优化。图片来源:Science
首先,作者选择二氯甲基频哪醇硼酸酯(1)为模板底物,向其中加入正丁基锂得到中间体3a,接着向溶液中添加芳基吡咯烷叔亮氨酸衍生的硫脲4,以78%的收率和48% ee值得到α-氯硼酸酯产物5a(图1D)。有意思的是,如果在加入正丁基锂前就先加入硫脲4,那么产物5a的ee值竟然高达92%,同时还观察到溶液中存在异硫脲硼酸酯衍生物6a(由化合物4与频哪醇硼酸酯反应得到)。于是,作者将6a分离纯化后添加到硼酸盐3a的溶液中,发现5a的ee值仅26%;但是在加入正丁基锂前就先加入化合物6a,则能以94%的ee值得到5a。研究表明6a在溶液中以锂盐Li-6a的形式存在并发挥作用。此外,通过去质子化硫脲4与过量外消旋溴氯甲基频哪醇硼酸酯的动力学拆分,成功地以克级规模合成了稳定的异硫脲-硼酸酯预催化剂6a(收率66%,图1E)。

图2. 锂-异硫脲硼酸盐的结构表征。图片来源:Science
接下来,作者用LiHMDS处理预催化剂6a得到锂-异硫脲硼酸酯Li-6a并对其进行了结构表征,红外光谱显示异硫脲N-C-N键(1596 cm-1 → 1555 cm-1)和酰胺C-O键(1658 cm-1 → 1618 cm-1)的伸缩振动频率发生了变化(图2A),该结果与密度泛函理论(DFT)计算的结果相一致,这可能是由于6a的N-H键被LiHMDS去质子化,并且锂离子被环外异硫脲氮和酰胺氧螯合。需要指出的是,该转化是可逆的,通过向Li-6a中添加一当量的HCl便可得到6a。另外,作者还合成了易结晶的甲基类似物Li-6b并对其进行了X-射线衍射分析,进一步证实了五元锂螯合模型(图2B),其中阳离子位于由4-氯苯基、叔丁基、异硫脲-硼酸酯杂环和3,5-双(三氟甲基)-苯基确定的高度不对称口袋中。尽管Li-6b也能催化硼酸盐3a的重排反应,但是对映选择性略有降低(87% ee)。
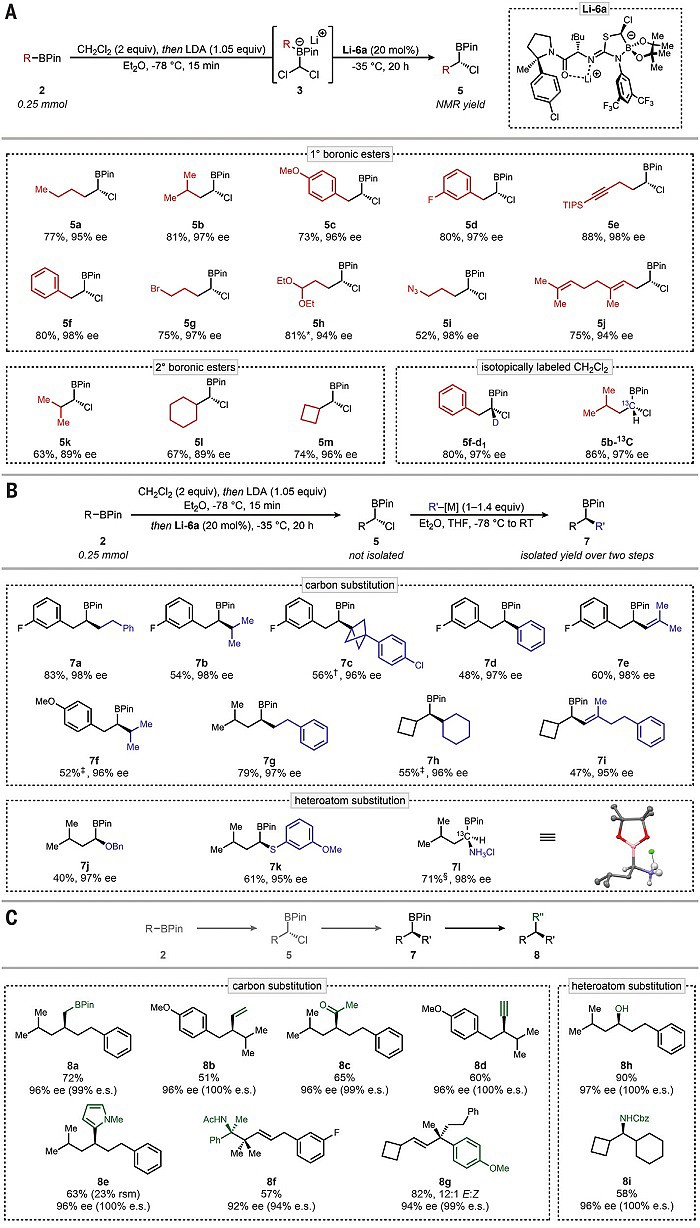
图3. 合成应用。图片来源:Science
在最优条件下,作者首先考察了硼酸酯的底物范围(图3A),结果显示多种简单易得的伯烷基(5a-j)和不受位阻影响的仲烷基(5k-m)频哪醇硼酸酯衍生物都能兼容该反应,以中等至较好的收率(52-88%)和优异的对映选择性(89-98% ee)得到所需的重排产物,特别是带有弱Lewis碱(5c、5h、5i)或对碱敏感(5e、5g)的官能团也能耐受该反应。然而,芳基或烯基频哪醇硼酸酯、带有更强Lewis碱取代基的底物以及叔烷基硼酸酯要么无法进行重排反应,要么对映选择性不太理想。有趣的是,通过使用市售的CD2Cl2(5f-d1)和13CH2Cl2(5b-13C)便能快速地合成带有同位素标记立体中心的化合物。其次,由于一次迁移后与硼酸酯相连的碳原子上还有一个氯原子,因此可以进行二次迁移。为此,作者开发了一种两步序列,即先进行Li-6a催化的重排反应,然后再加入不同基团(如:伯烷基(7a、7g)、仲烷基(7b、7f、7h)、环状叔烷基(7c)、芳基(7d)和烯基(7e、7i))取代的格氏试剂或杂原子亲核试剂(7j、7k)进行对映特异性重排,以良好的收率和优异的对映选择性得到一系列手性纯的仲硼酸酯产物。类似地,5b-13C也能转化成相应的α-硼胺(7l),后者可用于获得蛋白酶体抑制剂药物硼替佐米的同位素标记类似物。最后,作者利用碳-硼键转化将得到的仲硼酸酯产物(7f-h)进一步转化为三取代立体中心化合物(8a-e、8h、8i),并具有高收率和对映特异性(图3C)。此外,烯丙基硼酸酯中间体(7e和7i)在γ-位进行选择性转化,分别得到带有α-叔胺(8f)和季碳立体中心(8g)的全取代产物。
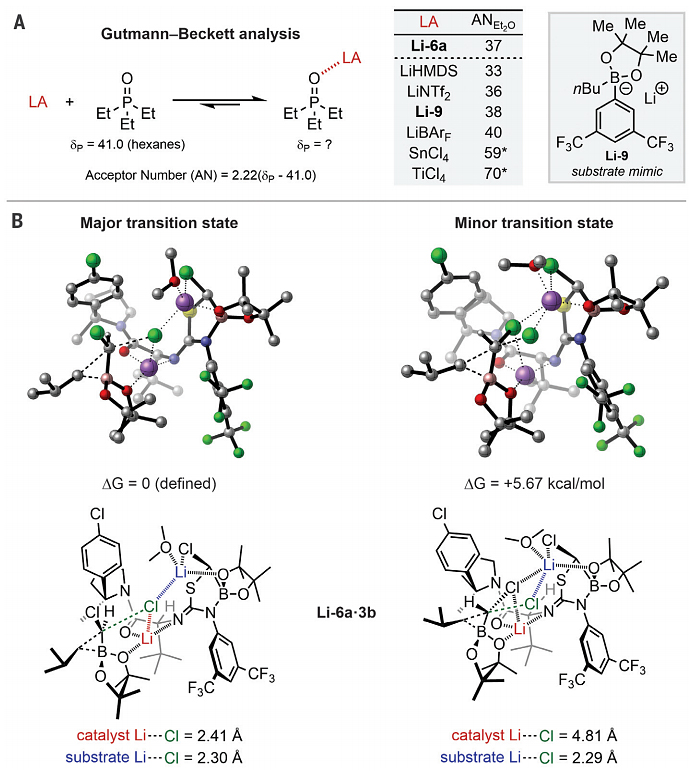
图4. 机理研究及计算分析。图片来源:Science
为了进一步探究异硫脲硼酸锂Li-6a如何诱导对映选择性1,2-硼酸酯重排,作者进行了Gutmann-Beckett分析,结果显示Li-6a仅具有中等Lewis酸性,类似于其他锂盐且远远低于传统Lewis酸催化剂(如TiCl4,图4A)。值得注意的是,硼酸锂Li-9作为不能进行重排的底物模拟物,其受体数比用Li-6a获得的受体数略高。鉴于在催化条件下观察到的对映选择性水平,Li-6a在促进重排方面必须要比硼酸锂底物3本身更具反应性。尽管这些观察结果不能排除Li-6a作为手性Lewis酸的可能性,但硼酸锂底物模拟物Li-9所表现出相似的Lewis酸性则排除了Lewis酸单独作为催化剂介导重排中速率加速的唯一因素。通过DFT计算,作者提出了可能的关键过渡态(图4B),即底物与催化剂形成一个双锂活性中心,两个锂离子的存在使得底物中碳氯键键长增加,导致氯原子与底物锂离子和催化剂锂离子之间的距离分别为2.30 Å和2.41 Å。总之,核磁共振(NMR)和DFT研究与异硫脲硼酸锂物种Li-6a通过双锂诱导的氯提取促进重排反应相一致,即借助于刚性催化剂骨架上的碱性官能团,将催化剂和底物锂离子以精确的几何形状定位。
总结
Eric N. Jacobsen教授课题组报道了对映选择性催化1,2-硼酸酯重排反应,成功地合成了一系列α-氯频哪醇硼酸酯,该手性合成砌块可经历两个连续的立体特异性转化,从而得到各种各样的三取代立体中心。具体而言,对映选择性反应由锂-异硫脲硼酸酯络合物催化,该络合物可能通过双锂诱导的氯提取来促进重排反应的进行。毫无疑问,该策略为手性硼酸酯的构建提供了新的可能性。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective catalytic 1,2-boronate rearrangements
Hayden A. Sharma, Jake Z. Essman, Eric N. Jacobsen
Science, 2021, 374, 752-757, DOI: 10.1126/science.abm0386
导师介绍
Eric N. Jacobsen
https://www.x-mol.com/university/faculty/26725
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号