解析微生物耐药性的功能图论
注:文末有研究团队简介及本文科研思路分析
金黄色葡萄球菌(Staphylococcus aureus)是人类面对的一种重要病原菌,可引起多种严重感染,万古霉素(vancomycin)作为治疗该菌引起疾病的最后一道防线,随着长时间的使用,也逐步产生了万古霉素耐药型菌株(VISA),探究其在不同万古霉素浓度下的表型可塑性极为重要。
微生物对不同药物浓度的反应在进化上是属于表型可塑性(phenotypic plasticity)概念。表型可塑性是指生物体随环境改变而改变其表型的能力,在生物适应性进化中起着关键作用。但是生物对环境变化的响应机制是高度复杂的,表型可塑性如何受基因控制是学术界的一项悬而未决的重要课题。近日,美国宾夕法尼亚州立大学杰出教授邬荣领与北京林业大学计算生物学中心团队合作,在功能作图(functional mapping)的基础上发明功能图论(functional graph theory),以此来推断表型可塑性的全基因组互作组网络(omnigenic interactome network),攻克了微生物耐药性这一难题。
在这项研究中,研究人员整合了功能作图、进化博弈论(evolutionary game theory)、捕食者-猎物理论(predator-prey theory)等多学科的知识,开发了一个联合统计框架,构建出基因相互作用的微分方程组。通过功能聚类和变量选择,运用龙格-库塔法对微分方程求解,实现了从任何维度的遗传数据中推断具有稳定性,稀疏性和因果关系的多层次全基因网络方法。
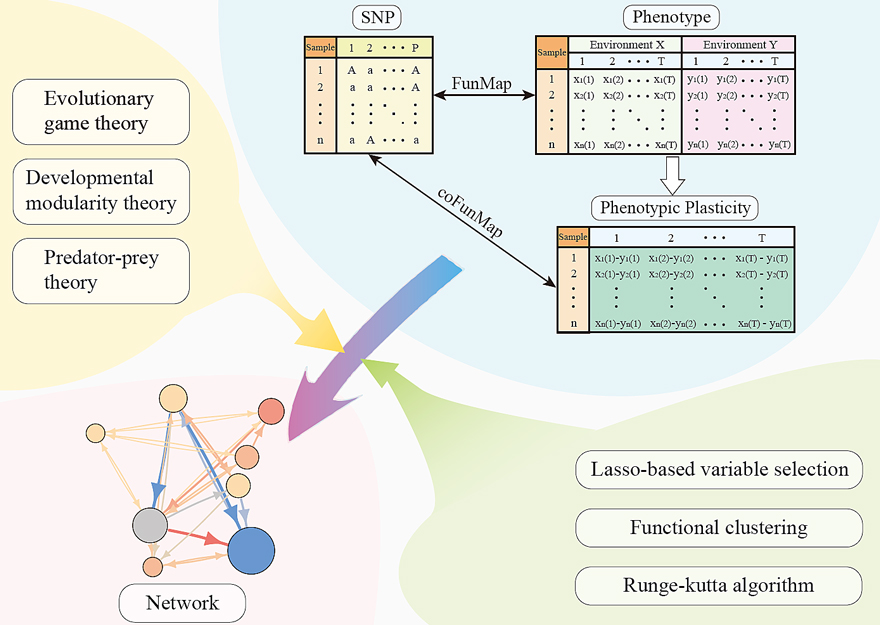
研究人员使用金黄葡萄球菌设计了两个表型可塑性实验,一个是有无抗生素环境的表型可塑性实验,一个是金黄葡萄球菌和大肠杆菌共培的表型可塑性实验。通过复合功能作图对影响表型可塑性的关键QTL进行定位,运用上述模型重建了对应的遗传网络,来探究该物种的表型可塑性遗传机制。在全基因网络中对SNP的净遗传效应分解为该SNP自身效应和其他SNP对其的影响,揭示了影响表型可塑性的关键QTL的基因调控机制,并构建了蛋白质网络对其进行了验证。
研究发现,一些QTL的遗传效应大并不是因为其自身效应大,而是一些其他SNP对其有一个促进作用。而一些并不显著的位点并非其自身效应小,而是其他位点对其有负的调控效应将其抵消掉了,假如将这些负的调控效应来源给断掉,这些不显著位点可能表现出极强的影响力。在过去的几十年中,GWAS方法因为只能识别一小部分遗传力,更多的遗传力丢失掉而饱受诟病。研究中提的全基因网络构建方法很好的解释了这些丢失的遗传力。
该研究提出了一个新的全基因网络构建模型框架,开辟了一条揭示基因如何与环境相互作用的新途径,系统地剖析了金黄葡萄球菌如何对非生物因素(药物)和生物因素(物种共存)作出反应的遗传结构,为金黄葡萄球菌的表型可塑性研究提供指导,为解析环境诱导的进化提供了一个强有力的系统工具,对计算生物学的发展具有重要意义。
这一成果近期发表在Nature Communications 上,文章的第一作者是北京林业大学博士生杨登程,通讯作者是邬荣领教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Inferring multilayer interactome networks shaping phenotypic plasticity and evolution
Dengcheng Yang, Yi Jin, Xiaoqing He, Ang Dong, Jing Wang & Rongling Wu
Nat. Commun., 2021, 12, 5304, DOI: 10.1038/s41467-021-25086-5
邬荣领教授简介

邬荣领,1995年获美国华盛顿大学(西雅图)数量遗传学博士学位,现任美国宾夕法尼亚州立大学统计学、公共卫生科学杰出教授,统计遗传研究中心主任。
研究兴趣包括,发展跨学科统计方法,揭示复杂性状及人类复杂疾病的遗传控制机理。提出的基因功能定位(functional mapping)方法能有效发现性状发育的遗传规律,刻画基因效应随时空变化的关键模式。将功能定位理论与进化博弈论、尺度理论、食饵-捕食者理论、发育模块理论相结合,提出解析复杂性状复杂性的功能图论(functional graph theory),并据此发展出一系列计算方法用于构建从分子到表型的多层次、多空间、多刻度的基因型-表型关系立体网络,为系统生物学、系统医学、系统药物学研究提供分析工具。在Nature Reviews Genetics、Nature Communications、PNAS、Journal of the American Statistical Association、Annals of Applied Statistics、Physics of Life Reviews、Physics Reports、Briefings in Bioinformatics、Cell Reports、Evolution等国际重要刊物上发表SCI论文逾400篇,研究成果被Science、Cell等重要刊物引用或重点介绍。
https://www.x-mol.com/university/faculty/236892
本文科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:复杂性状是受多因子控制的,具有动态特征,并对环境信号极为敏感。解析复杂性状形成的遗传机制是当代生物学最为困难的任务之一,具有高度挑战性。我们认为,传统的方法试图发现影响复杂性状的单个主因子固然十分重要,但是它们难以驾驭复杂性状的“复杂性”这一根本问题。有鉴于此,我们另辟蹊径,把复杂性状作为一个动态系统,借助跨学科理论,构建决定系统动态行为的互作网络,勾画出影响复杂性状最终表型的信息流与路线图,对于复杂性状如何产生,如何发展,如何发挥作用等问题进行逐一的详细解析。
Q:研究过程中遇到哪些挑战?
A:构建复杂性状网络的最大挑战是维度、因果链、样本个体化。比如,一个肿瘤常常会有成千上万个细胞,每个细胞各具特色;而每个细胞内又有成千上万个基因、蛋白、代谢物等等。构建这个亿级,甚至千亿级的网络,一方面计算难以实现,另一方面也违背网络稀疏性与稳定性的生物学原则。据此,我们引入发育模块理论与生态斑块理论,通过多维统计方法把所有生物对象分解成各个相互不同而又相互依赖的网络模块。把各网络模块再进一步分解形成网络亚模块,这个过程持续进行直至模块内基因数量达到“社交网络“理论所要求的标准。据此,我们能构建出多层次、多通道、巨型而又精密的互作组网络,为解析复杂性状提供重要分析工具。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A: 为系统生物学、系统医学、系统药物学研究提供分析工具。在精准育种领域,人们利用它能找到关键基因通道,从而对基因进行有效定向编辑。在药物设计领域,人们利用它能发现、配置最佳的药物组合,更有效地治疗人类复杂疾病。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号