双(二氟甲基)三甲基硅负离子:Me3SiCF2H对可烯醇化酮亲核二氟甲基化的关键中间体
(二氟甲基)三甲基硅烷(Me3SiCF2H)是Ruppert-Prakash试剂(Me3SiCF3)的类似物。自从2011年中国科学院上海有机化学研究所胡金波课题组的赵延川等人首次系统研究了Me3SiCF2H作为二氟甲基负离子源,并实现了其对醛、酮、亚胺的亲核二氟甲基化反应(Org. Lett., 2011, 13, 5342),自此Me3SiCF2H广泛地用于多种二氟甲基化反应的构建中。然而由于二氟甲基的吸电子能力比三氟甲基弱,Me3SiCF2H的反应性与Me3SiCF3存在显著的差别。以Me3SiCF3进行的三氟甲基化反应在各种Lewis碱的活化下,可以顺利发生;而类似的二氟甲基化却对反应条件要求苛刻,存在明显的溶剂效应及碱效应,对适用的底物范围有所限制。例如,对芳香醛的亲核二氟甲基化需要在极性溶剂中进行,在非极性溶剂中无法进行;对双芳基酮的亲核二氟甲基化,需要使用化学计量的叔丁醇钾,而小于化学计量的氟化铯不能引发反应。长期以来,Me3SiCF2H不能高效实现对可烯醇化酮的亲核二氟甲基化。近日,该课题组陈定奔、倪传法等人在研究对可烯醇化酮的亲核二氟甲基化中,首次观察到[Me3Si(CF2H)2]- 这一超配位硅物种,通过详细的机理研究指出该物种是反应中的一个关键中间体,并且首次揭示了通常被忽略的双氟烷基超配位硅物种在氟烷基化反应中可以发挥重要作用。
该小组首先研究了Me3SiCF2H在THF中被亲核试剂活化时所产生的超配位硅中间体及其二氟甲基化能力(图1a)。根据以前的报道,最初选用了CsF和t BuOK作为活化硅的亲核试剂。但是在较大的温度范围内,氟谱跟踪仅观察到二氟甲烷与Me3SiCF2H的特征峰。他们认为观察不到超配位二氟甲基硅中间体的原因可能是:二氟甲基负离子与碱金属阳离子之间有很强的相互作用,导致超配位二氟甲基硅中间体很容易分解为二氟甲基负离子,继而从溶剂THF或体系痕量的水中攫取质子生成二氟甲烷。

图1.Me3SiCF2H的亲核活化(根据Angew. Chem. Int. Ed., 2016, 55, 12632整理)
已有报道表明,抗衡阳离子效应可以显著影响超配位硅负离子的稳定性。因此他们决定利用冠醚作为添加剂,通过与金属阳离子络合,减弱二氟甲基负离子与金属阳离子的作用,来稳定超配位硅中间体。他们发现,当使用CsF/18-冠-6组合时,在室温下,氟谱跟踪可以观察到化学位移在大约-130 ppm出现了一个信号强度较弱的峰。当用溶解性更好的t BuOM/18-冠-6组合时,这个信号进一步增强,并且可以在较大的温度范围内观察到(图1b)。他们结合硅谱、氢谱、碳谱以及异核相关谱图数据确定该物种为五配位的双(二氟甲基)三甲基硅负离子[Me3Si(CF2H)2]-。尽管二氟甲基基团的电负性要比三氟甲基弱,但Me3SiCF2H仍然具有一定的Lewis酸性来络合二氟甲基负离子。[Me3Si(CF2H)2]-是观察到的唯一的超配位二氟甲基硅物种。反应以氘代THF作为溶剂在允许观测的范围内升高温度时,始终没有观察到二氟甲基负离子,但是观察到了氘代二氟甲烷,表明二氟甲基负离子动力学不稳定,更容易攫取质子。
在确定了五配位的[Me3Si(CF2H)2]-这一中间体后,他们对其亲核二氟甲基化的能力进行了研究(图2)。当使用可烯醇化的酮作底物时,存在显著的阳离子效应:t BuOCs/18-冠-6组合可以顺利促进二氟甲基化的进行;但是t BuONa/18-冠-6组合尽管可以产生[Me3Si(CF2H)2]-,却很难发生二氟甲基化,几乎全部转化为二氟甲烷。因此阳离子作用不但影响[Me3Si(CF2H)2]-的产生,而且影响其对可烯醇化酮的反应性。在催化量t BuOM/18-冠-6引发的二氟甲基化反应中,同样存在阳离子效应。
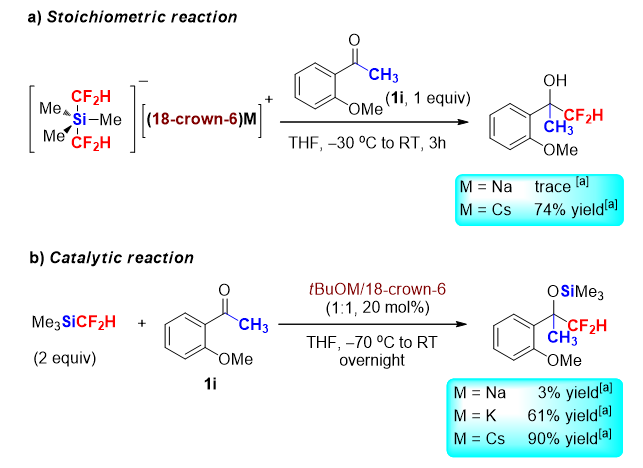
Scheme 2. 亲核二氟甲基化的阳离子效应.(根据Angew. Chem. Int. Ed., 2016, 55, 12632整理)
为了弄清[Me3Si(CF2H)2]-在催化循环中的作用,他们结合变温核磁观察了催化量t BuOCs/18-冠-6引发的二氟甲基化的反应过程。他们发现,[Me3Si(CF2H)2]-的生成速率远远大于与酮的反应速率。在反应过程中,始终存在一定量的[Me3Si(CF2H)2]-,表明该中间体一直在不断地消耗和再生。
使用CsF/18-冠-6组合也可以观察到[Me3Si(CF2H)2]-,当使用易得的CsF代替t BuOCs时,同样可以促进二氟甲基化反应顺利进行(图3)。该反应不但适用于烯醇化的芳香酮、脂肪酮,而且也适用于对芳香醛、脂肪醛、双芳基酮、内酯等羰基化合物的亲核二氟甲基化,反应具有很好的普适性。
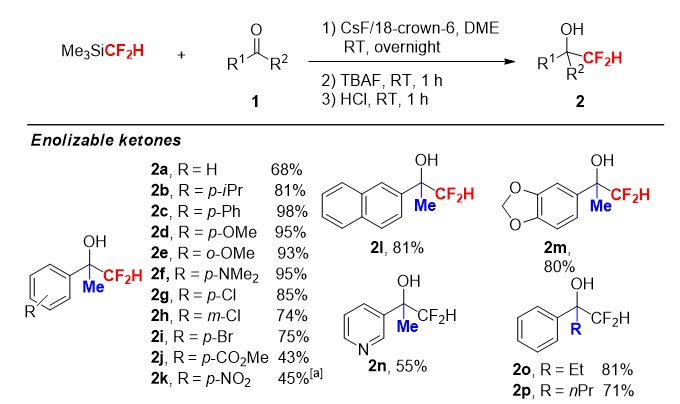

图3. 底物普适性生的扩展(根据Angew. Chem. Int. Ed., 2016, 55, 12632整理)
最后,根据观测到的信息,他们提出了一个以五配位双(二氟甲基)硅负离子为关键中间体的自催化循环过程(图4)。首先,引发剂与Me3SiCF2H作用产生[Me3Si(CF2H)2]-,其中Cs与18-冠-6络合抑制了强碱性的二氟甲基负离子产生,进而稳定该中间体,有利于进行羰基加成而不是发生烯醇化过程。加成得到的烷氧基负离子作为新的亲核试剂与Me3SiCF2H作用得到产物,由此循环产生[Me3Si(CF2H)2]-。实验发现,由于[Me3Si(CF2H)2]-的产生速率远远大于对羰基的加成反应速率,烷氧基配位的超配位二氟甲基硅中间体直接对底物二氟甲基化的可能性不大。因此二氟甲基化的机理不同于常规理解的三氟甲基化反应的机理。
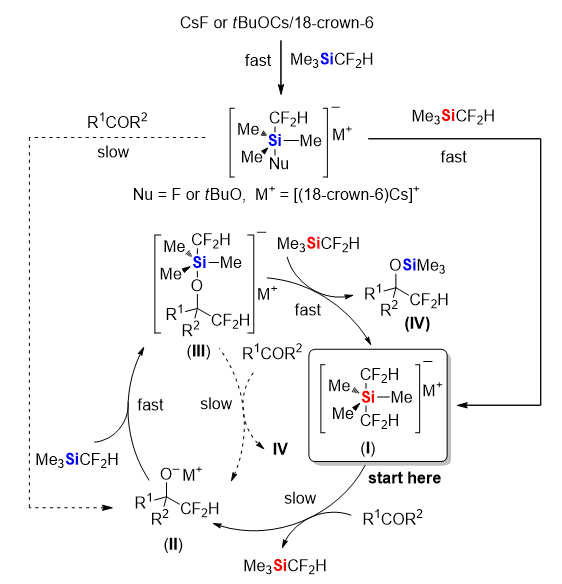
图4. 反应可能的机理(图片来源:Angew. Chem. Int. Ed., 2016, 55, 12632)
综上所述,本文作者利用抗衡阳离子调控的策略实现了Me3SiCF2H对可烯醇化酮的高效亲核二氟甲基化反应,该试剂是一种温和的二氟甲基化试剂。除此之外,作者首次观察到[Me3Si(CF2H)2]-作为反应中的关键中间体,可以降低游离的二氟甲基负离子的强碱性,从而揭示出通常被忽略的超配位双(氟烷基)硅负离子在氟烷基化中可以发挥重要作用。
这一成果近期发表在Angew. Chem. Int. Ed. 上,文章第一作者陈定奔,台州学院副教授,从2014年9月开始,在胡金波研究员指导下进行博士后研究,主要从事亲核氟烷基化反应及其机理的研究工作。
该论文作者为:Dingben Chen, Chuanfa Ni, Yanchuan Zhao, Xian Cai, Xinjin Li, Pan Xiao, and Jinbo Hu*.
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Bis(difluoromethyl)trimethylsilicate Anion: A Key Intermediate in Nucleophilic Difluoromethylation of Enolizable Ketones withMe3SiCF2H
Angew. Chem. Int. Ed., 2016, 55, 12632-12636, DOI: 10.1002/anie.201605280
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号