Science:电光催化“合力”实现碳氢键双胺化
含氮化合物广泛存在于食品、医药、材料及化工等领域中,关于含氮化合物的高效构筑往往是有机化学家们研究的热点。其中将未活化的C-H键转换为有价值的C-N键可极大地促进复杂分子的合成,特别是与生物医学相关的分子。为此,化学家已经开发了多种C-H键胺化反应,但绝大多数方法仅能实现单个C-H键的转化,而许多合成过程则需要安装多个C-N键。因此,迫切需要发展一种能够同时实现多个C-H键活化的化学反应,但是该过程仍颇具挑战。
2019年,美国康奈尔大学的Tristan H. Lambert教授课题组报道了一种有效的氧化化学策略(Angew. Chem. Int. Ed., 2019, 58, 13318–13322),将光能和电能在单个催化剂中结合在一起,该过程称为电光催化(electrophotocatalysis,EPC)。具体而言,在相对温和的电化学势下对三氨基环丙烯(TAC)离子1进行电化学氧化,并伴随可见光辐射以激发生成的自由基二价阳离子2(图1A)。光激发得到的自由基二价阳离子3是一种非常有效的氧化剂,可以促进具有挑战性的反应(如苯和其他缺电子芳烃的氧化官能团化或醚的区域选择性C-H键官能团化)。在此基础上,作者设想能否利用TAC EPC提供的强氧化性和选择性条件使一系列Ritter型C-H键官能团化反应序列发生,其中最初形成的乙酰胺基团促进了相邻(邻位)位置的第二次胺化反应。近日,他们报道了电光催化的烷基化芳烃的邻位C-H键胺化反应(图1C),制备了一系列1,2-二胺衍生物。根据所使用电解质的不同,可得到3,4-二氢咪唑或氮丙啶产物。相关成果发表在Science 上。
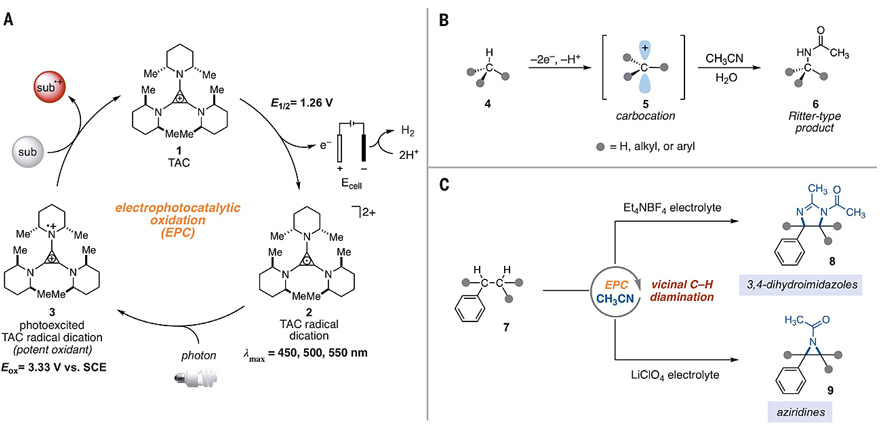
图1. C-H键的电光催化胺化。图片来源:Science
经过反应条件筛选,作者确定了能够将各种苄基烃有效转化为相应的N-酰基-4,5-二氢咪唑加合物的反应条件(图2)。具体而言,用白色紧凑型荧光灯(CFL)对底物、8 mol%TAC 1、四乙基四氟硼酸铵(Et4NBF4)以及乙腈:三氟乙酸(5:1)的溶液进行可见光照射,同时电解槽(碳毡阳极和铂板阴极)处于受控电势[2.4 V,阳极电势(Eanode)= 1.3 V vs Ag/AgCl]。对照实验表明如果没有催化剂1或没有光照射,则只能检测到痕量的此类产物。在该条件下,异丙基苯(枯烯)以72%的收率转化为化合物10(图2)。芳环上的卤素取代基(11-14)、被保护的苯胺氮(15)和溴甲基取代基(16)也能兼容该反应。然而,4-异丙基联苯没有产生任何二胺化产物17,而是得到了未知的混合物。尽管存在强氧化条件,但苄基三氟乙酰胺基团仍具有较好的耐受性(18)。当使用4-甲基异丙基苯时,以51%的收率生成了二胺化产物19,同时得到了由苄位甲基的Ritter反应产生的副产物(收率:11%)。对于4-乙基异丙基苯而言,产生了41%的二胺化产物20以及41%的乙基官能化产物。相比之下,1,4-二异丙基苯能够有效地转化为二胺化产物21。异构体1,3-二异丙基苯也得到了加合物22,但收率显著降低。类似地,2,4,6-三异丙基苯甲酸甲酯和2,4,6-三异丙基溴苯仅在4-异丙基上进行官能团化,分别以67%和87%的收率得到23和24。
此外,作者还考察了非苄基碳(25-32)氨基化的位点选择性。在所有情况下,均观察到亚甲基碳的官能团化优先于甲基碳。相反,产物32中的甲基被优先官能团化。鉴于α,α-二芳基胺是生物医学相关化合物中的重要组成部分,因此作者研究了偕二芳基底物的这种转化,1,1-二苯乙烷能够有效地进行反应,以80%的收率得到化合物33。尽管收率略有下降,但可以耐受一个(34)或两个(35)环上的氟取代基。同时,醇、酯、烷基氟和酰胺取代基都可兼容该反应(36-39)。苯基环戊烷以85%的收率得到双环化合物,形成5:1的N-酰基异构体混合物(40和40')。类似地,六元环和七元环产物(41和42)也分别得到区域异构体混合物,而八元环和十二元环产物(43和44)则分别得到单一异构体。值得一提的是,通过使用TBAPF6作为电解质,可以提高一些环状底物的收率。螺环化合物45也是可得到的,表明张力环中C-H键也可官能团化。除乙腈外,其他腈也可用于该反应中,从而产生衍生自丙腈、丁腈或苄腈作为氮源的二胺化产物(46-48)。最后,作者还评估了未支化苄基底物的二胺化过程。正丙基苯和卤代正丙基苯均能与CH3CN反应,以中等的收率得到目标产物(49-51)。其中正丙基苯以3:1的比例获得了两种异构体(49和49');当使用更长的烷基链底物(如正丁基苯(52和52')和正十二烷基苯(55和55'))时,也观察到了类似的区域选择性。另外,环状茚满也可实现这一转化,以32%的产率得到化合物56。

图2. 底物范围。图片来源:Science
在研究过程中,作者发现将电解质从Et4NBF4改为LiClO4会得到邻位C-H键双官能团化产物:N-酰基氮丙啶(图3)。因此,枯烯及其卤代衍生物以较低至中等的产率产生了氮丙啶(57-59),而其它氧化剂则未提供任何氮丙啶或二胺化产物。对于带有侧羧基取代基的底物,氮丙啶产物(60和61)是主要的。偕二芳基底物的产率较高(62-64)。3-苯基戊烷也能以中等的收率形成氮丙啶65,后者为1:1的非对映异构体混合物。通常情况下,带有富电子芳环的底物不能很好地参与该过程。但是仍能以中等收率制备66-68。

图3. 电光催化相邻C-H键氮杂环丙烷化。图片来源:Science
由于后期C-H键官能团化为药物化合物库的多样化提供了强大的工具,因此作者测试了几种生物活性分子相似物的双官能团化反应(图4A)。二溴异丁香衍生物能以42%的产率产生二胺化产物69。在标准条件下,塞来昔布(Celebrex)类似物70的产率为56%,而FKGK11甲基化衍生物类似物71的产率为38%。同时,沙利度胺5HPP-33类似物以50%的产率转化为72。此外,视黄酸受体激动剂和CYP11B1抑制剂均具有联芳基部分,分别以67%和35%的收率提供类似物73和74。尽管存在敏感的苄基C-N键,但仍能以68%的收率得到insertraline类似物75。除了二胺化产物外,氮丙啶化过程可在更复杂的环境中实现,从而可直接得到产物76和77。

图4. 合成应用。图片来源:Science
鉴于1,2-二胺在药物合成、配体及其它方面都有重要的应用,作者发现对本文的电光催化过程稍微修饰就能以良好的产率分离出游离的1,2-二胺(图4B)。按照上述二胺化步骤,用KOH、乙醇和乙二醇处理粗制的反应混合物并加热至回流,便可得到二胺产物78-84(其中分离出的80和81为二甲苯磺酸盐)。异丙苯(99,<0.03美元/毫升)可通过该方法有效地转化为有价值的2-苯基丙烷-1,2-二胺78(569美元/克)。另外,通过在室温下使用相似的水解条件,可获得游离的二氢咪唑加合物85-90(图4C)。为了进一步证明该方法的合成潜力(图4D),作者对二芳基乙烷(91、92)进行电光催化处理,然后水解和形成酰胺,可以高收率制备Y5受体拮抗剂(93、94)。此外,91可选择性地进行二胺化和水解,得到哌嗪97,后者进行酰化得到A2腺苷受体抑制剂98。类似地,三氟甲基化合物95以相似的顺序结合,可快捷地合成血管加压素激动剂96。最后,异丙苯(99)也可以通过简单的两步氮丙啶化和水解直接转化为重要的β-氨基醇100(357美元/克)。
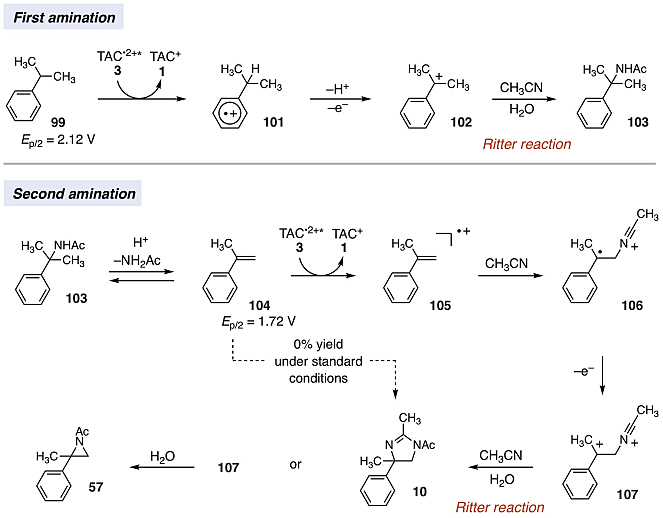
图5. 反应机理。图片来源:Science
关于机理,作者认为该反应是从底物的苄基C-H键的Ritter型胺化开始的,该过程与已知的电化学Ritter型反应相符(图5)。在这种情况下,TAC光激发的自由基二价阳离子3对底物99进行单电子氧化产生自由基阳离子101,然后去质子化和第二次氧化得到阳离子102,后者经溶剂解提供了Ritter加合物103。在标准反应条件下,乙酰胺103转化为二氢咪唑产物10。目前,有关第二次C-H键氨基化的途径尚不确定。一种可能的途径是最初形成的Ritter产物103经历可逆的酸催化消除反应,生成α-甲基苯乙烯104,后者经单电子氧化、溶剂捕获、氧化得到二氢咪唑产物10或氮丙啶57,这两种产物的生成取决于电解质。
总结
Tristan H. Lambert教授课题组报道了烷基化芳烃在乙腈作为溶剂和氮源的条件下,通过电光催化策略实现了邻位C-H键胺化反应,最终形成1,2-二胺衍生物,二胺化与合理的官能团相容性使这种反应具有实用价值。同时,在单个催化剂的操作内将光能和电能结合在一起具有提高合成能力的价值。C&EN以“Technique turns C-H neighbors into diamines”为题对本工作也进行了评论[1]:研究人员通过在一个反应中转化两个相邻的C-H键,提高了C-H键活化的前瞻性。这种罕见的双活化方法为合成有价值的分子提供了一条新途径,并且为创建功能强大的催化剂提供了一种相对简单的方法。北卡罗来纳大学教堂山分校的光化学家David Nicewicz说,该反应会对乙烷进行4电子氧化,显示了使用电化学的真正能力。他说,如果团队使用化学氧化剂,“他们需要用相当大的量”,而在这种情况下,“他们只需要接通电源而已”。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Electrophotocatalytic diamination of vicinal C–H bonds
Tao Shen, Tristan H. Lambert
Science, 2021, 371, 620-626, DOI: 10.1126/science.abf2798
参考资料:
[1] C&EN评论链接:
https://cen.acs.org/synthesis/c%E2%80%93h-activation/Technique-turns-CH-neighbors-diamines/99/i5
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号