Angew. Chem.:电化学氧化巢式碳硼烷B-H键功能化
碳硼烷因其具有独特的立体结构、三维芳香性、较高的热稳定性和代谢稳定性、低毒性、高硼含量等特点,在材料、生物医药、催化等领域具有巨大应用前景。巢式碳硼烷是由闭式碳硼烷失去一个硼顶点而形成,因其具有较好的水溶性而在医药研发方面具有巨大的应用潜力。因此,对巢式碳硼烷的功能化修饰方法的研究具有重要意义。然而到目前为止,有关巢式碳硼烷功能化方法的研究报道却相对较少。
南京大学燕红课题组一直致力于碳硼烷化学的研究。近期该课题组通过电化学氧化的策略,实现了巢式碳硼烷与含孤对电子杂原子的氧化偶联反应。在温和的反应条件下以良好的产率得到B-S、B-Se、B-Te、B-N、B-P、B-As、B-Sb等一系列硼和杂原子偶联的目标化合物,同时避免了化学计量氧化剂和金属催化剂的使用(图1)。
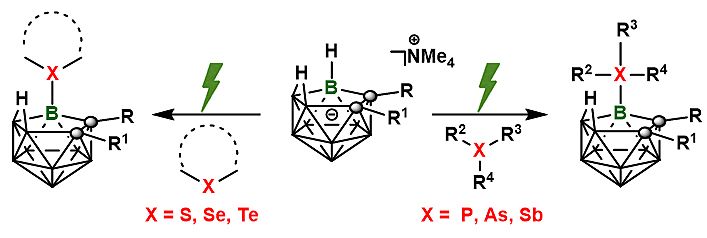
图1. 电化学氧化巢式碳硼烷B-H官能团化
作者首先以双苯基巢式碳硼烷与二乙基硫醚作为起始原料对反应条件进行了优化,反应在最优条件下以78%的收率得到目标化合物。在最优的反应条件下,作者对杂原子底物和巢式碳硼烷底物的适用范围分别进行了考察,实验结果表明,反应的产率取决于杂原子底物的亲核性,亲核性越强,反应收率越高;取代基的位阻效应也会明显影响反应效率,如硫醚一端连接异丙基,反应产率明显降低。S、Se、Te同一主族元素随着原子序数的增大,其亲核性逐渐增大,反应收率也逐渐提高。此外,15主族的N(含N杂环)、P、As、Sb在该电反应条件下,也都能够以中等以上的收率得到目标化合物。值得注意的是,硼簇化合物与As、Sb的偶联反应尚未被报道。巢式碳硼烷碳原子上无论是被烷烃或(杂)芳烃取代,均能够以较好的收率得到目标化合物。由于产物中未生成对称平面,因此所得到的产物是一对外消旋体,这可通过单晶X-射线衍射数据得知,同时也对化合物3进行了手性拆分,显示出了1:1的对映体。
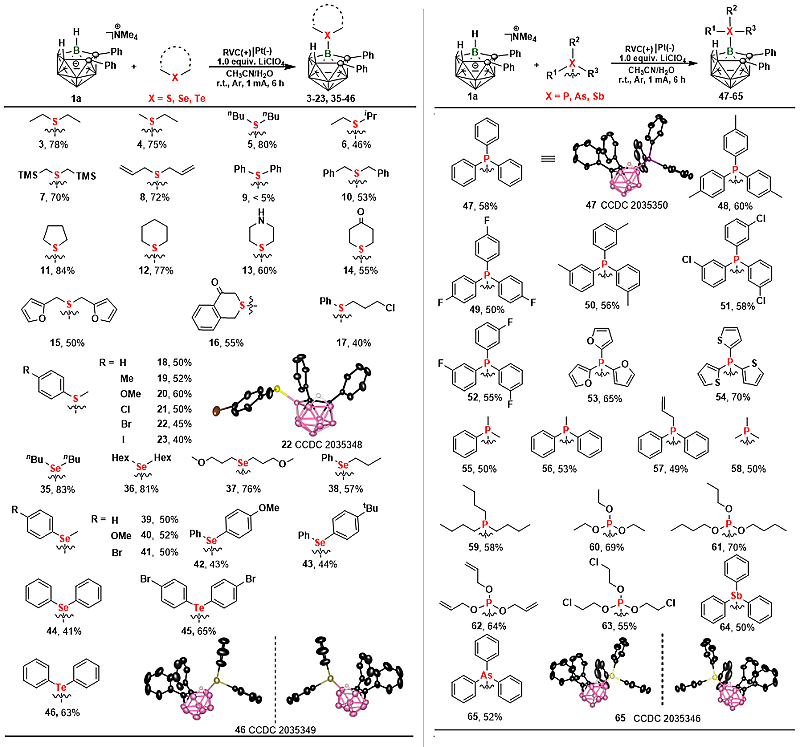
图2. 底物适用范围研究
为了挖掘该类化合物的潜在应用,首先对化合物的稳定性进行了考察,核磁跟踪实验结果表明,目标化合物在酸性和中性条件下较稳定,而在碱性条件下不太稳定;此外,化合物的热稳定性也较好。当将反应规模放大到5 mmol,仍能以略微降低的产率得到B-S成键的目标化合物,说明了该电反应具有一定的实用性。将富含硼的碳硼烷硼簇与药物分子片段结合有利于硼中子俘获疗法(BNCT)试剂的开发,值得高兴的是,在该电反应条件下,巢式碳硼烷能分别与含布洛芬、吲哚美辛、环丙贝特、丙磺舒等药物片段分子有效地结合(图3)。
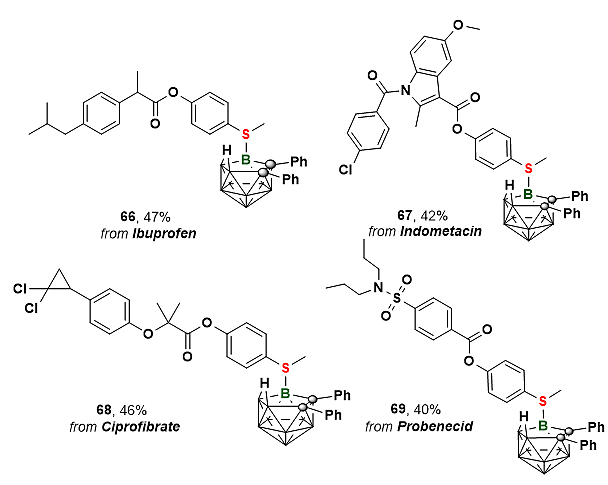
图3. 巢式碳硼烷对药物分子片段的后修饰
为了更加深入了解该反应机理,利用桥氢氘代的巢式碳硼烷和二乙基硫醚在标准条件下反应,得到桥氢未被氘代的目标化合物24,表明此反应可能经历了一个脱氢和氢迁移的过程。同时,也进行了循环伏安法实验,结果表明巢式碳硼烷在反应过程中最先被氧化。根据以上实验结果以及相关的文献报道,作者提出如下可能的反应机理:巢式碳硼烷在阳极被连续两次氧化,得到阳离子中间体II,随后活泼桥氢离去,亲核底物对缺电子的B-H键进行亲核加成,最终得到目标化合物。在该过程中,还伴随着B-H的迁移形成新的桥氢。
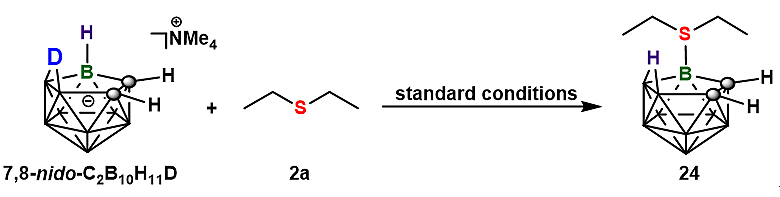
图4. 同位素标记实验
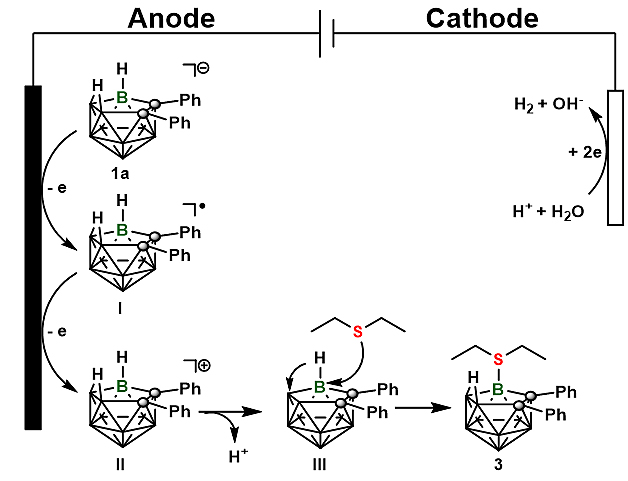
图5. 可能的反应机理
总结
燕红教授课题组开发了一种电化学氧化巢式碳硼烷B-H键功能化的方法,具有简洁高效、条件温和、底物适用范围广,官能团容忍性较好等优点,丰富了巢式碳硼烷B-H键功能化的方法,为其在药物化学,材料化学等领域的应用开辟了更广的空间。相关研究成果近期发表在Angewandte Chemie International Edition。文章的第一作者为南京大学化学化工学院博士研究生陈蒙。研究得到了国家自然科学基金的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Electrooxidative B-H Functionalization of nido‐Carboranes
Hong Yan, Meng Chen, Deshi Zhao, Jingkai Xu, Chunxiao Li, Changsheng Lu
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202015299
导师介绍
燕红
http://www.x-mol.com/university/faculty/11500
芦昌盛
http://www.x-mol.com/university/faculty/11504
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号