CCS Chemistry | 新发现:MonM,原来你是这样的一个酶
摘要:复旦大学张琪课题组通过基因挖掘发现了一个新型的linaridin天然产物—mononaridin。生物合成研究揭示参与mononaridin生物合成的MonM是一个具有丰富催化多样性的N-甲基转移酶。利用MonM的催化特性,张琪课题组开发出一种温和高效的多肽抗生素荧光标记方法。南京大学梁勇课题组通过DFT计算,解释了烯丙基转移反应更具优势的化学机制。
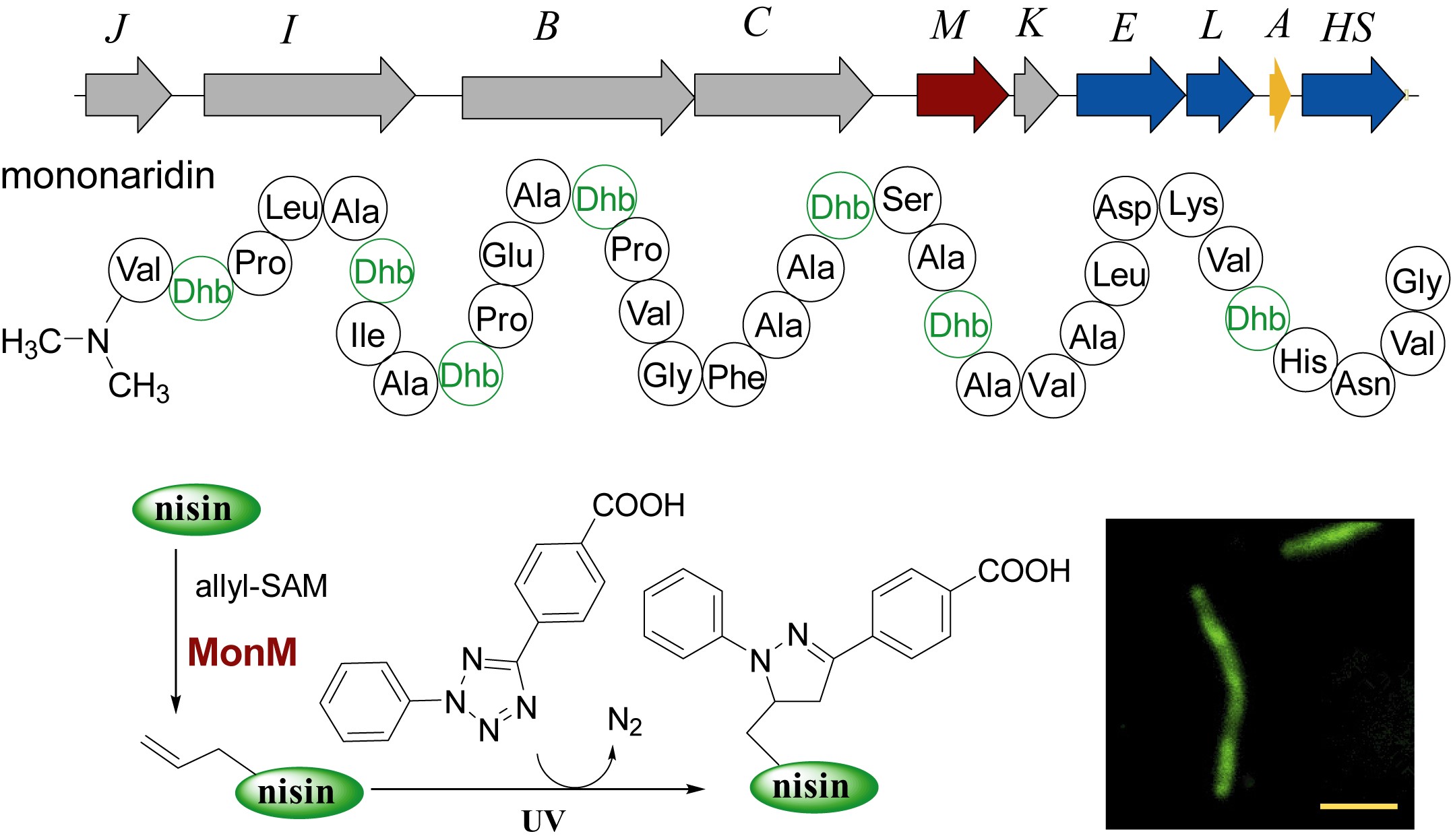
核糖体肽类天然产物(RiPPs)是近十年逐渐进入人们视野的一大类肽类天然产物。这类化合物在自然界中分布及其广泛,具有丰富的结构多样性和生物活性多样性。含有多个脱水氨基酸的线性骨架的Linaridin天然产物是一小类具有“神秘”色彩的核糖体肽天然产物。目前linaridin家族仅有4个成员被报导,包括cypemycin和legonardin(图1A)。复旦大学张琪课题组在linaridin类化合物的基因组挖掘、生物合成和结构改造方面做了一系列工作(综述见Nat. Prod. Rep. 2020, doi: 10.1039/c9np00074g.)。
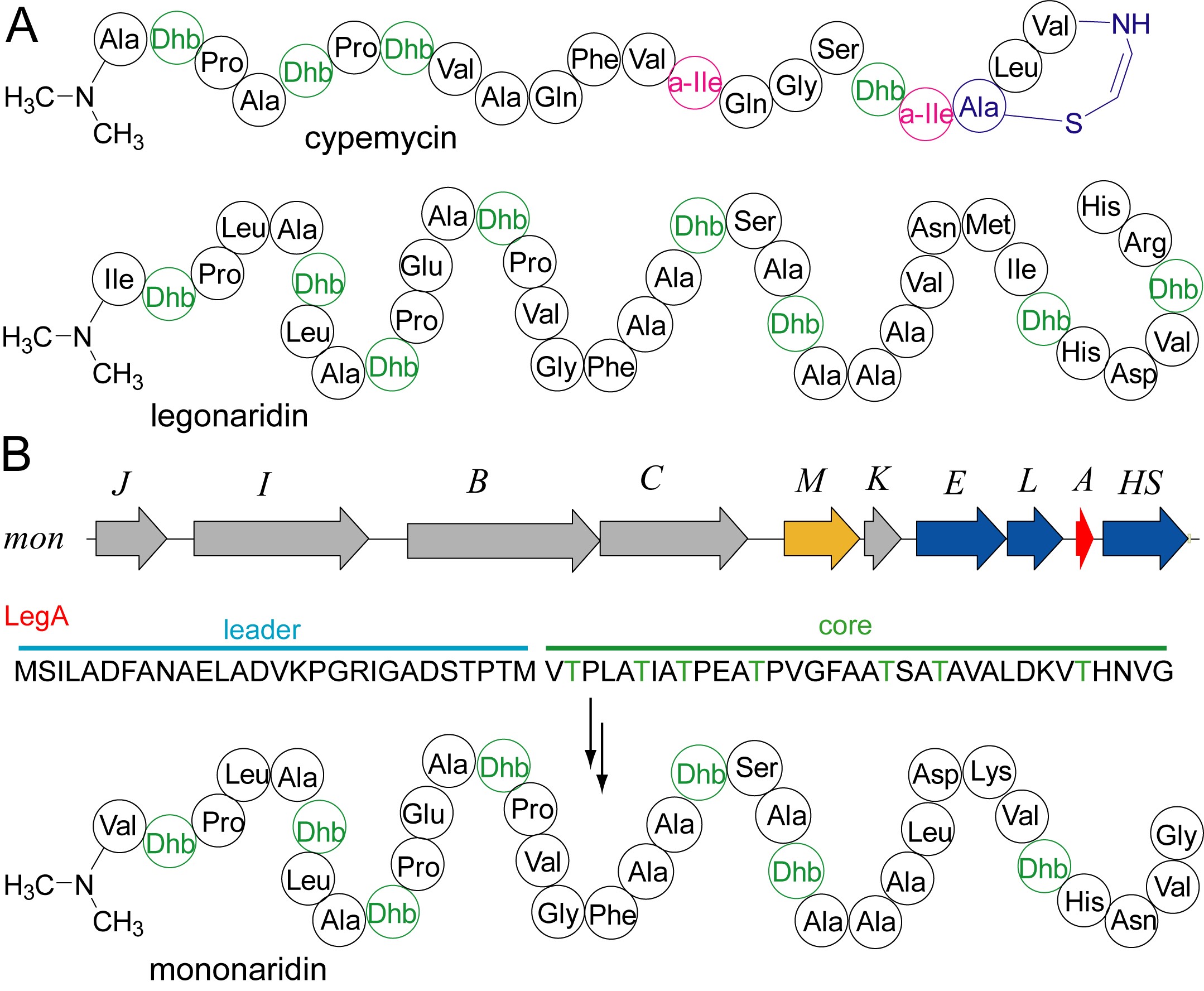
图1
近期,该课题组研究人员在链霉菌中发现linaridin基因簇,利用模式菌S. albus进行异源表达后得到新型天然产物mononaridin(图1B)。基因敲除实验证实基因簇中MON、MonE、MonL、MonC、MonI和MonM等多个基因都直接参与了mononaridin的生物合成。同时,研究人员注意到: N-甲基转移酶MonM的基因敲除突变株产生了一个N端去甲基化的类似物dm-mononaridin!这表明MonM是一种新的α-N-甲基转移酶。
进一步实验表明,除了天然底物S-腺苷甲硫氨酸(SAM)以外,MonM还能有效地利用SAM结构类似物ethyl-SAM和allyl-SAM,催化乙基转移和烯丙基转移反应。与乙基转移反应相比,烯丙基转移反应更为高效。为了解释该现象,南京大学梁勇课题组以2-氨基-N-甲基丙酰胺为烷基化受体进行了详细的DFT计算(图2)。计算结果表明受烯丙基双键的影响,该反应的能垒比乙基转移低6个kcal。而对于烯丙基转移反应,氨基受体进攻烯丙基C3位置的能垒和C1较为相近(图2D),表明该反应从C1和C3两个位置均可能发生。该结果较好地解释了尽管烯丙基位阻比乙基更大,酶对于烯丙基有更好容忍性的实验现象。
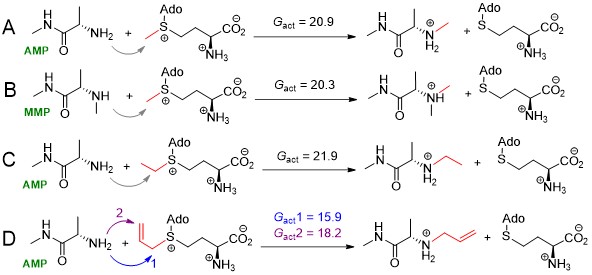
图2.
实验发现,对于其他含有alpha-氨基的多肽,例如RiPP抗生素乳酸链球素nisin,MonM也可以催化其N端烷基化。上述实验表明,MonM具有丰富的催化多样性。
作者利用MonM催化的烯丙基化反应,结合烯丙基双键与四氮唑在温和紫外光下的“光点击反应”,成功地实现了nisin的荧光标记,并对其与细胞的结合进行了成像分析(图3)。该结果显示出MonM在多肽结构改造中的巨大潜力。
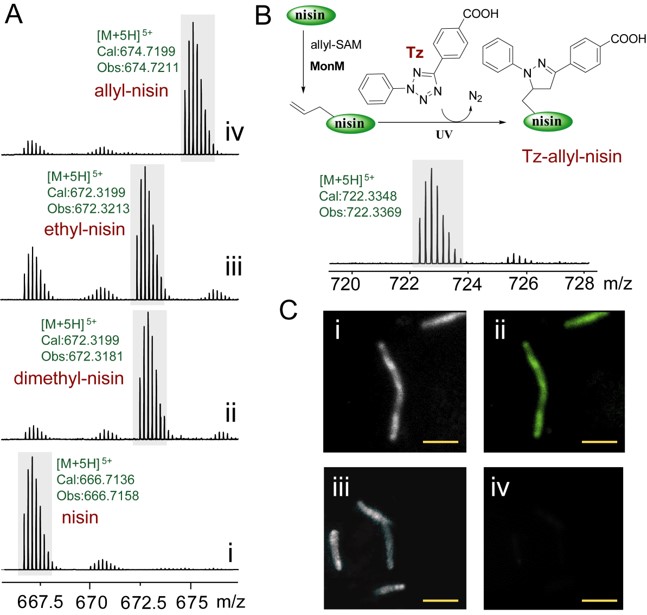
图3
综上所述,课题组在linaridin基因簇基因表达过程中发现的MonM是一个具有高度催化多样性的α-N端甲基转移酶。进一步,利用MonM的催化多样性,课题组成功地开发了一种温和高效的多肽抗生素荧光标记方法,显示出MonM在多肽结构改造中的巨大潜力。该工作以research article 的形式发表在CCS Chemistry,并已在“Just Published”栏目上线。此项研究得到了国家自然科学基金、国家重点研发计划以及江苏省创新人才计划的资助。
 扫描二维码,免费阅读下载原文。
扫描二维码,免费阅读下载原文。
文章详情:
Genome Mining and Biosynthesis Study of a Type B Linaridin Reveals a Highly Versatile α-N-Methyltransferase
Fangting Wang , Wanqing Wei , Junfeng Zhao, Tianlu Mo, Xin Wang, Xuedong Huang , Suze Ma , Shu Wang, Zixin Deng , Wei Ding , Yong Liang * & Qi Zhang*
Citation:CCS Chem. 2020, 2, 1049–1057
文章链接:https://doi.org/10.31635/ccschem.020.202000247
 关注CCS Chemistry微信公众号,了解更多文章信息。
关注CCS Chemistry微信公众号,了解更多文章信息。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号