CCS Chemistry:非Ni不可,三组分模块化合成1,1-二芳基烷烃
摘要:武汉大学阴国印课题组利用镍催化,发展了一种模块化合成1,1-二芳基烷烃的方法。这种新路径使用了更为廉价的催化剂和反应原料,实现了传统方法中烯烃转化存在的一些挑战。
1,1-二芳基烷烃作为一种重要的药效团,存在于在很多药物和生物活性分子中。因此,二芳基烷烃分子骨架的合成引起了化学家们的极大兴趣。传统的合成策略是利用苄基亲电试剂与芳基偶联试剂进行交叉偶联。尽管这种方法发展非常成熟,但是从逆合成的观点来说,通过三组分模块化合成二芳基烷烃是自由度更高、更具吸引力的策略(图1a)。在这一概念的吸引下,化学家们在三组分组装二芳基烷烃的策略上做了许多尝试,通过Pd催化的烯烃1,1-二芳基化的方法取得了不错的成果(图1b)。但是,这些工作通常需要借助导向基团或烯烃底物的空间位阻来对反应的区域选择性进行调控。因此,能否开发出无导向基团的非活性烯烃的双芳基化策略,就成为了化学家亟待解决的一个问题。
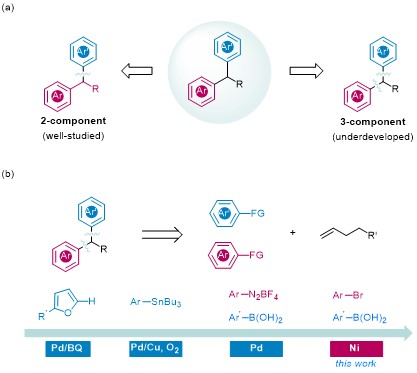
图1
此前,武汉大学阴国印课题组曾实现了通过Ni催化的迁移交叉偶联来合成1,1-二芳基烷烃的反应,其中涉及到关键的苄基-Ni中间体(II)。作者推测,如果烯烃插入芳基-Ni物种后发生1,2-Ni迁移,也能得到苄基-Ni中间体(II),随后苄基-Ni中间体(II)与芳基亲核试剂转金属化,利用这种关键中间体可以得到1,1-二芳基烷烃(图2)。值得注意的是,在卤离子存在的条件下,分子间非活化烯烃对芳基-金属键插入的区域选择性仍然是一项具有挑战性的任务。
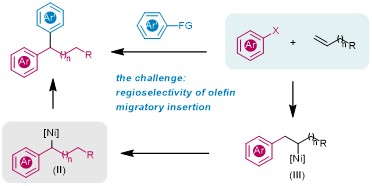
图2
通过条件筛选,作者确立了以Ni(NO3)·6H2O为催化剂,NaOMe为碱,CPME为溶剂的最优条件。该反应底物范围适应性较广,芳基偶联试剂和非活性烯烃均具有不错的官能团兼容性(图3)。值得注意的是,该反应具有良好到适中的区域选择性,但是产物中仍然伴随着少量1,2-双芳基化副产物的产生。在使用未保护的溴代苯胺和溴代吲哚作为芳基偶联试剂时,反应显示出较低的区域选择性。
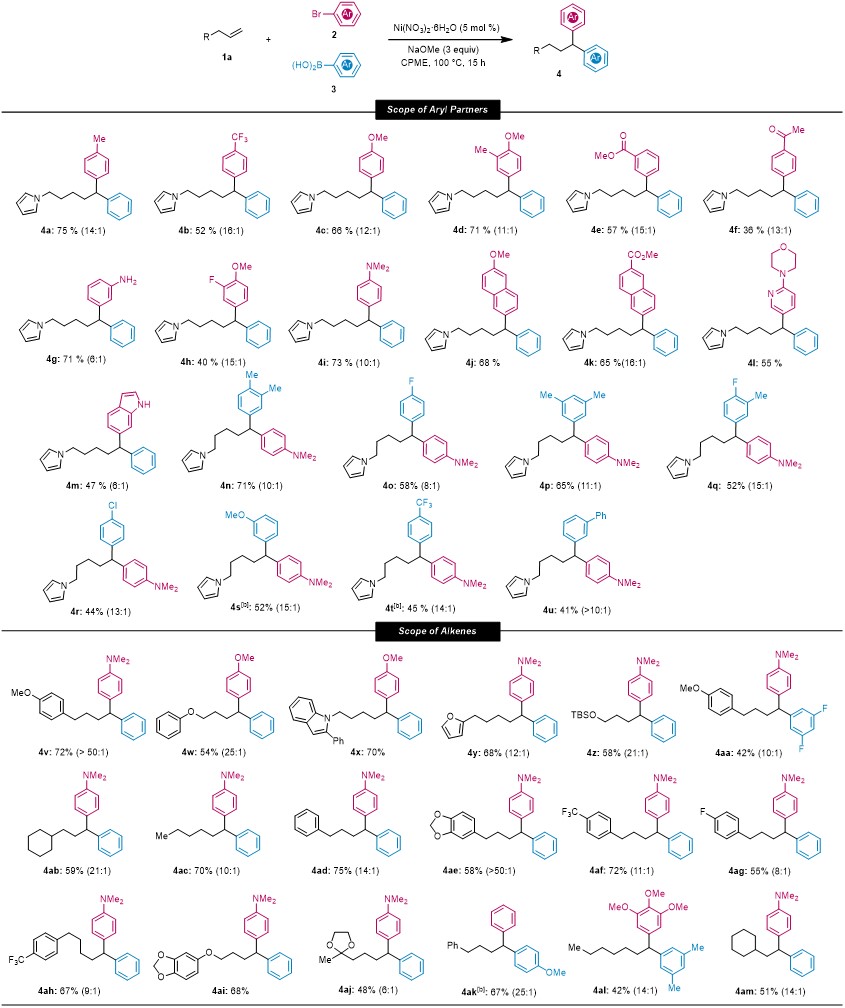
图3
为了进一步探索这一反应的应用范围,作者也考察了气态的烯烃(图4a)。仅通过使用含烯烃气体的气球,乙烯和丙烯就可以进行反应得到1,1-二芳基烷烃。
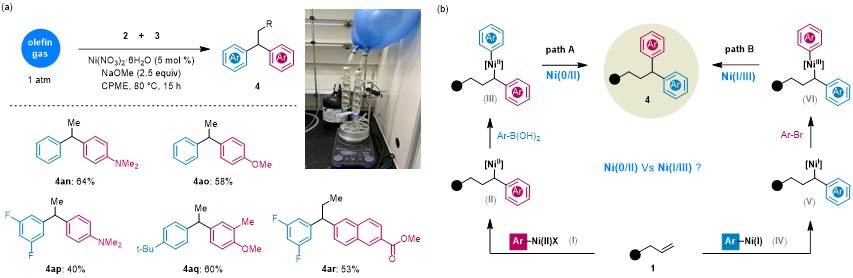
图4
基于之前文献报导的先例,作者认为反应机理可能遵循两种路径(图4b)。路径A是一个Ni(0/II)的催化过程,路径B则是一个Ni(I/III)的催化过程。两种路径的主要区别在于反应的启动方式不一样,路径A是通过Ni与芳基溴化物的氧化加成开始反应,路径A是通过Ni与芳基硼酸的转金属化开始反应。随后作者进行了一系列的机理实验,结果支持反应是通过路径A实现的。有趣的是,随着芳基溴化物取代基给电性减弱,1,1-和1,3-双芳化产物的比例也随之降低,其趋势通过根据取代基的Hammett常数σ和两种双芳化产物的比例所绘制的散点图得以体现(图5)。这一结果表明给电性越强的芳基越有利于π-苄基Ni(II)中间体的形成。
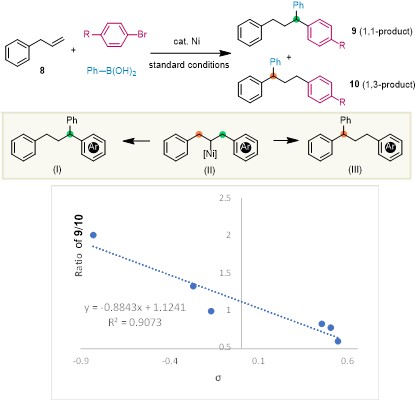
图5
综上所述,该研究工作提供了一种模块化合成1,1-二芳基烷烃的方法,这种新型的方法,使用了更为廉价的催化剂和反应原料,实现了传统方法中一些存在挑战的烯烃的转化。此工作得到了国家自然科学基金的资助。该工作以communication的形式发表在CCS Chemistry,并在官网“Just Published”上线。
 扫描二维码,免费阅读下载原文
扫描二维码,免费阅读下载原文
文章详情:
Modular Synthesis of Diarylalkanes by Nickel-Catalyzed 1,1-Diarylation of Unactivated Terminal Alkenes
Zheqi Li, Dong Wu, Chao Ding, & Guoyin Yin*
Citation:CCS Chem. 2020, 2, 576–582
文章链接:https://www.chinesechemsoc.org/doi/10.31635/ccschem.020.202000183
 关注CCS Chemistry 微信公众号,了解更多文章信息。
关注CCS Chemistry 微信公众号,了解更多文章信息。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!











































 京公网安备 11010802027423号
京公网安备 11010802027423号