《Nature》:经典的Diels-Alder反应,突破经典的新发现
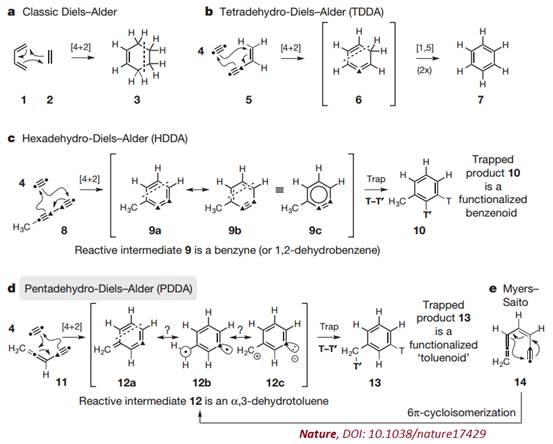
Diels-Alder反应(D-A反应)是有机化学中非常重要的反应之一,发现者德国化学家Otto Diels 和他的学生Kurt Alder因此获得1950年的诺贝尔化学奖。Diels-Alder反应中,双烯体(diene)和亲双烯体(dienophile)发生[4+2]环加成反应,生成六元碳环,例如丁二烯和乙烯反应生成环己烯。如果反应物对的氢原子减少,例如炔或烯炔,所得的产物中的氢原子也会减少,从环己烯变成苯环。这些Diels-Alder反应的变体中,少了4个氢原子的称为四脱氢Diels-Alder(tetradehydro-Diels-Alder,TDDA)反应,而少了6个氢原子的则称为六脱氢Diels-Alder(hexadehydro-Diels-Alder,HDDA)反应。
明尼苏达大学Thomas R. Hoye课题组长期致力于Diels-Alder反应的研究,X-MOL曾报道该课题组利用Diels-Alder反应在更温和的条件下成功合成了(±)-paracaseolide A(点击阅读详情)。最近,Hoye课题组再次在经典Diels-Alder反应中找到了新的突破,他们在《Nature》报道了Diels-Alder反应的一种全新环异构化过程(cycloisomerization),并命名为五脱氢Diels-Alder(pentadehydro-Diels-Alder,PDDA)反应。(The pentadehydro-Diels-Alder reaction. Nature, DOI: 10.1038/nature17429)
研究人员们进行的第一个PDDA反应使用了氮原子连接的四炔底物(下图15-Ms),在碱性条件下发生哌啶催化的异构产生中间体16(下图),后续分析结果表明这是个限速步骤;接着发生快速的PDDA环化生成α,3-脱氢甲苯(α,3-dehydrotoluene)中间体17(下图);α,3-脱氢甲苯中间体十分活泼,会在更短时间内被亲核试剂捕获,生成带有苯环的化合物18a(下图)。

研究人员随后在实验中证实了这种高活性的α,3-脱氢甲苯中间体的存在。这种Diels-Alder反应中前所未见的中间体与苯炔(benzyne)有着相同的氧化态,同苯炔一样,能被多种捕获剂捕获,产生结构不同的多种产物。
这种全新的脱氢Diels-Alder反应,产物多样性是一大优点,能很好的补充经典Diels-Alder反应和脱氢Diels-Alder反应的产物范围,进一步扩展了Diels-Alder反应的应用空间。
http://www.nature.com.edgesuite.net/nature/journal/vaop/ncurrent/full/nature17429.html
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
























































 京公网安备 11010802027423号
京公网安备 11010802027423号