JACS:分子“裁缝”——首例金属-类卡拜实现双键的断与连
过去的半个世纪,有机化学见证了金属-碳单/双键形成策略及其基础上发展的各类方法学的长足进步,有些已在合成工业中占了重要地位甚至摘得了科学桂冠——诺贝尔奖(如Grignard、Suzuki、Heck、Grubbs等)。另一方面,尽管金属-炔键配合物(即金属-卡拜,metal-carbynes)在催化炔烃复分解反应中广泛应用,但在催化卡拜转移中却鲜有探索,主要原因是缺少适当的一价碳源。令人奇怪的是,学术界也未见金属-卡拜配合物的等价物——金属-类卡拜(metal-carbynoids)的相关研究报道。直到2018年,在西班牙加泰罗尼亚化学研究所(ICIQ)作为独立PI仅四年的Marcos G. Suero博士课题组利用光氧化还原催化方式发现了第一个卡拜等价物——重氮甲基自由基(下图int-1),并且实现了芳烃C-H官能团化(Nature, 2018, 554, 86)。
Marcos G. Suero博士和重氮甲基自由基。图片来源:ICIQ和Nature
因为上述重氮甲基自由基是在光氧化还原催化下异裂三价碘化合物1a或1b得到的,这引起了Marcos G. Suero博士课题组的进一步思考:是否可以通过熟知的双铑催化剂产生含有三价碘取代的铑-卡宾配合物?若是可行,那么后者中三价碘基团具有离去性,可产生铑-类卡拜(下图Rh-carbynoid 3),从而模拟单价阳离子卡拜(:+C−R)的性质,如在烯烃C(sp2)−C(sp2)键中插入一价碳单元得到烯丙基阳离子(下图allyl cation 5,经历环丙烷化后Woodward-Hoffmann-DePuy规则下的协同开环及高价碘基团离去),进而被多种亲核试剂进攻得到烯丙基砌块6或消除质子得到二烯7。整个过程就像“裁缝”一样在双键上进行“切断-缝合(cut and sew)”。很明显,这会涉及烯烃双键的α-或π-键的活化,而目前除了复分解反应和重排反应还没有其他方式能实现这一过程,因为双键的解离能高达174.1 kcal/mol。Marcos G. Suero博士近日带领课题组实现了这一转化,大大扩展了烯烃作为合成原料的应用途径,结果发表在JACS 上,作者仍然是上篇Nature 的第一作者——Zhaofeng Wang。
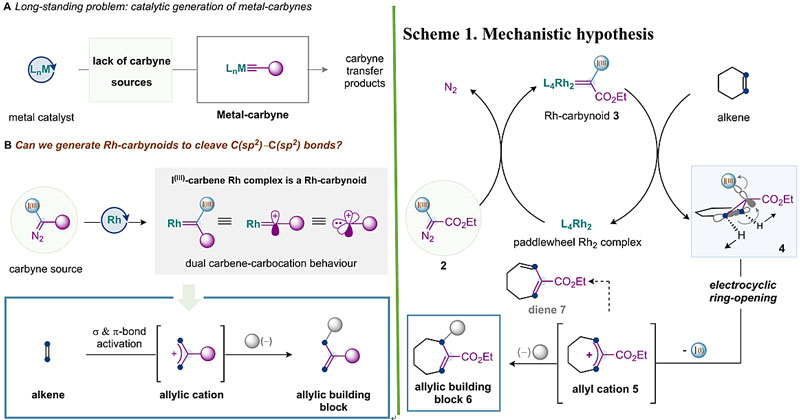
铑-类卡拜的产生及对烯烃插入的设想。图片来源:J. Am. Chem. Soc.
研究人员最初尝试用环己烯1a(5 eq.)、高价碘化合物2a与Rh2(Oct)4在-50 ℃下反应1小时后,向其中加入四丁基溴化铵(3 eq.)再反应1小时,以17%的收率得到烯丙基溴代物6a。若换成更大位阻的催化剂Rh2(Adc)2或Rh2(esp)2(Du Bois catalyst)可显著提高收率(30-48%)。同时还发现高价碘试剂的性质对反应影响很大,比如假环状的2a、2d和2e都能很好的进行转化(以2e为最优),而环状的2b则完全无效。过量的烯烃似乎对转化有利,因为他们用等摩尔量的环己烯和2e反应时产率明显下降(entry 8),可能是过量的烯烃阻止了中间体3的副反应发生。另外,替换成其他溴源如Bu4PBr或TMSBr则对反应无益。
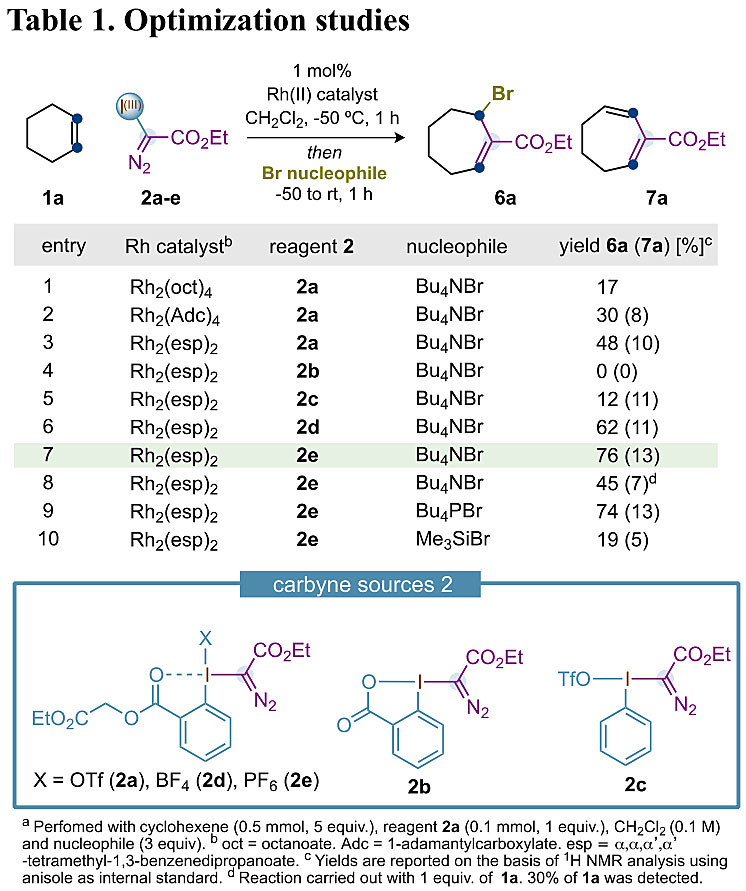
反应条件优化。图片来源:J. Am. Chem. Soc.
在优化的条件下,研究人员对不同亲核试剂进行了拓展,可喜的是试验的十几种亲核试剂均能很好地捕获烯丙基碳正离子从而构建多种烯丙型分子砌块。比如:1)用Bu4NBr或Et3N•3HF可构建碳-溴或碳-氟键;2)用甲醇、四丁基醋酸铵、水或TEMPO可构建碳-氧键;3)用硫醇可构建碳-硫键;4)用Bu4NSCN、叔丁基氨基甲酸酯、Bu4NN3或4-甲氧基苯胺可构建碳-氮键;5)用富电子的芳烃、杂芳烃、烯丙基三丁基锡、烯醇硅醚或叔丁基异氰化物、吡啶氧化物以及水的混合物则可构建碳-碳键。总的结果就是形成了一个新的C-C单键、一个新的C-C双键和在原烯烃sp2杂化碳上产生新的不对称碳。
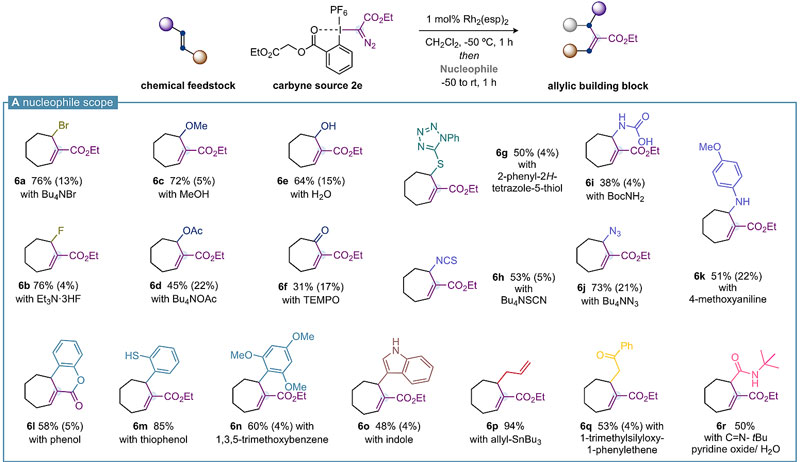
不同亲核试剂的应用。图片来源:J. Am. Chem. Soc.
接着研究人员又对烯烃底物范围进行扩展,廉价的石油化工原料当然是首选。就拿乙烯来说,全球一年生产量大约有1.34亿吨,要是能进行高附加值的开发必将创造更大的价值。令人欣喜的是乙烯也能在上述条件下高效的转化为烯丙基溴代物6s,这也是目前已知对乙烯进行该转化的首例。同样地,丙烯、1-丁烯和1-己烯也可以发生该反应,并且观察到很好的linear/branched选择性和Z/E选择性,这也表明了中间体10的电环化开环是对旋(R基团向内)后产生烯丙基阳离子11,然后溴从α-碳位阻较小的一侧进攻。对于更有挑战的1,2-二取代烯烃而言,在电环化开环时理论上可以产生两个性质相似的亲核位点(α和α'),势必会产生多种混合物。但这个方法很神奇地得到了很高的区域选择性和立体选择性(6x、6y)。另外,对于更大的环烯(如环庚烯、环辛烯和环十二烯)也毫无疑问的可以进行相应的转化(6z、6aa、6ab)。该方法学还有一个亮点在于将商业易得或从酮易制备的1,1-二取代烯烃(如6ac和6ad)转化为四取代的烯烃,并且立体选择性很好,这在之前很难有通用的方法进行合成。
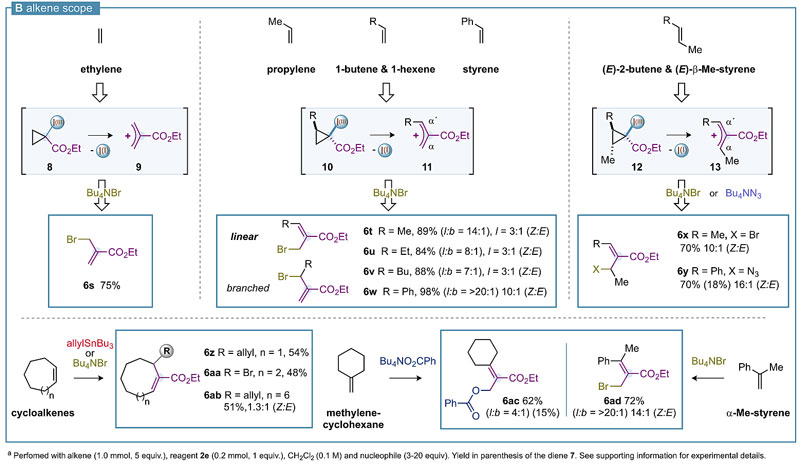
烯烃底物范围的扩展。图片来源:J. Am. Chem. Soc.
烯丙基阳离子除了能被外源性的亲核试剂进攻外,还能被分子内的亲核基团(如醇)进攻发生串联反应得到环化产物,对于新生成环一般符合Baldwin环化反应规则,即14、15、16和18通过exo-型环化得到,17则通过endo-型环化得到。
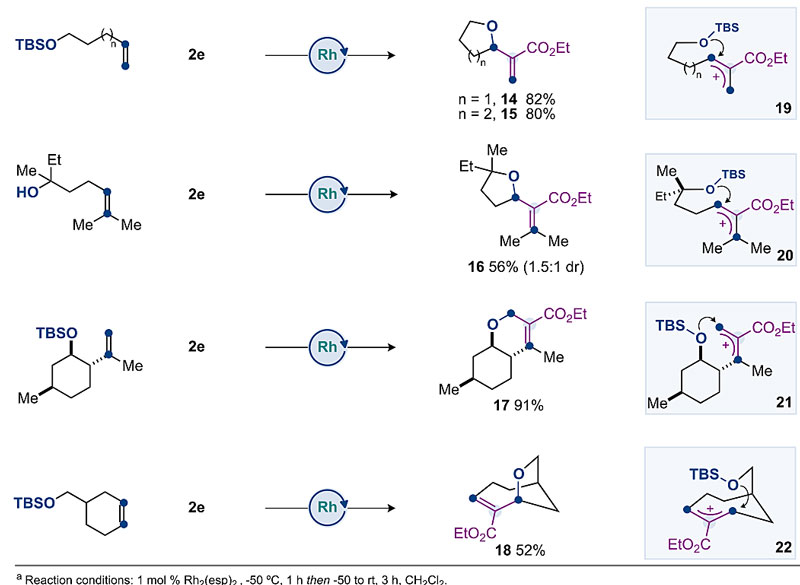
C(sp2)−C(sp2)切断串联分子内环化。图片来源:J. Am. Chem. Soc.
前文已经提到,研究人员设想该转化存在一个三价碘取代的三元环中间体。尽管该中间体被普遍认为是热力学不稳定的,但研究人员还是想努力拿到这一中间体来证明其设想的正确性。起初他们用苯乙烯和环己烯作为底物在−50 ℃反应下并未获得成功,这可能类似于取代的环丙基对甲苯磺酸酯的电环化开环在动力学上要比相应的未取代的环丙基对甲苯磺酸酯更容易进行。有了这个解释,他们用乙烯和2f为底物,Rh2(Adc)4为催化剂在室温下成功分离得到环丙烷衍生物23,这也是首例烷基-三价碘复合物的报道。控制实验表明中间体23在亲核试剂Bu4NBr进攻下毫无悬念地开环生成烯丙基溴24,进一步证明了设想机理的准确性。

环丙基-三价碘化合物23的制备。图片来源:J. Am. Chem. Soc.
总结
Marcos G. Suero博士研究团队基于金属-类卡拜复合物在烯烃双键活化中做出了重要贡献,或可大大拓展石油化工原料的应用前景和价值。延伸一点来说,笔者个人认为好的有机合成方法学往往要基于扎实且深刻的理论积累和理解,而不是盲目的试错或者期待从副反应中发现意外。这篇工作当是一种范式。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Catalytic Cleavage of C(sp2)–C(sp2) Bonds with Rh-Carbynoids
Zhaofeng Wang, Liyin Jiang, Pau Sarró, Marcos G. Suero
J. Am. Chem. Soc., 2019, 141, 15509-15514, DOI: 10.1021/jacs.9b08632
(本文由峰千朵供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号