Angew. Chem.:烯丙基醇的绿色环氧化
环氧化反应在药物和天然产物的合成过程中应用十分广泛,甚至部分药物本身就是环氧类化合物。在所有的环氧化合物中,烯丙醇环氧是非常重要的一类,他们往往是构建多羟基化合物和醇胺类化合物的前体。
然而通过烯丙醇合成烯丙醇环氧化合物通常需要用化学氧化剂,比如过氧酸、过氧醇;即使以氧气为最终氧化剂的烯丙醇环氧化反应通常也需要添加数倍当量的醛类化合物作为牺牲试剂。此外,三级烯丙醇由于醇羟基α位取代基位阻效应,反应效率较低,以氧气为氧化剂的环氧化反应很难实现。北京大学焦宁教授(点击查看介绍)课题组长期致力于氧气活化,利用氧气作为氧源实现了多种含氧化合物及药物分子衍生物的合成。近期,该课题组利用铜催化,以氧气为氧化剂和氧源,实现了三级烯丙醇的环氧化,反应不需要使用醛作为牺牲试剂,创新性地采用了1,4-二氧六环作为溶剂,同时作为氧原子转移的媒介。另外,通过调整所用的铜催化剂,该反应能高选择性地进一步得到半频哪醇重排产物(图1)。
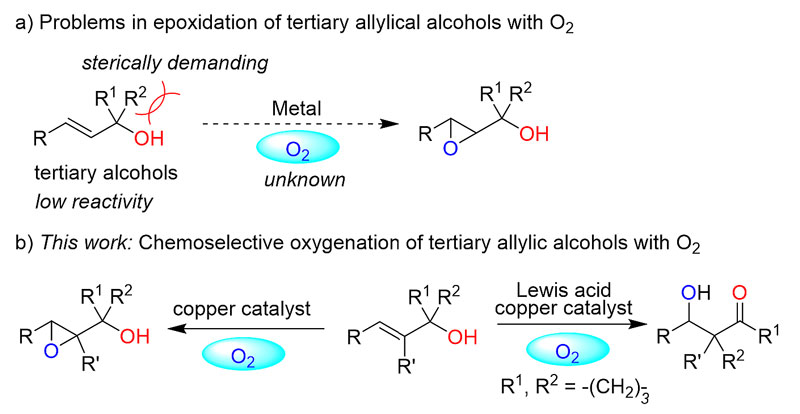
图1. 以氧气为氧化剂的三级烯丙醇环氧化
反应的底物扩展显示,二级烯丙醇以及具有挑战性的三级烯丙醇在该反应体系中均能兼容。取代的烯丙醇在Lewis酸性较强的三氟甲基磺酸铜的催化下,能通过半频哪醇重排反应一步得到环戊酮衍生物(图2)。动力学实验证明,该环戊酮产物的中间体就是该烯丙醇的环氧化合物。
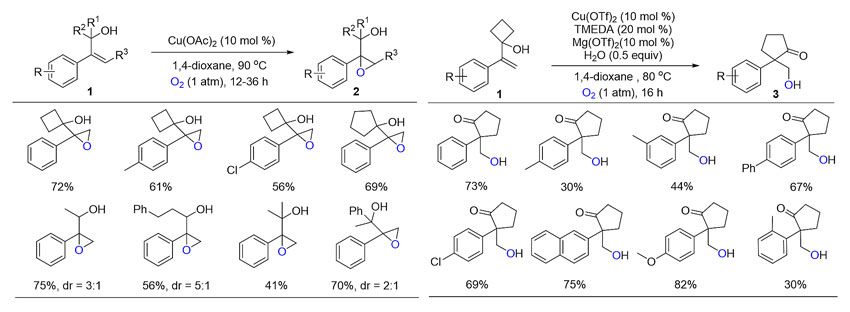
图2. 底物适用性考察
作者对该环氧化反应的机理进行了深入的研究。18O同位素标记实验证明产物中环氧骨架中的氧原子来自氧气。当在体系中加入一倍量的对甲氧基苯甲酸时,1,4-二氧六环氧化开环后与苯甲酸酯化的产物被分离得到。作者认为,1,4-二氧六环可能作为还原剂与氧气反应现场生成了过氧化合物,过氧化物氧化烯丙醇生成环氧化合物。为了捕捉1,4-二氧六环氧化后形成的自由基中间体,在反应一段时间后,作者在体系中添加了自由基补获剂,成功捕捉到了1,4-二氧六环氧化后通过β-断裂形成的碳自由基(图3a)。通过以上机理实验,作者提出了铜催化的自由基反应机理(图3b)。
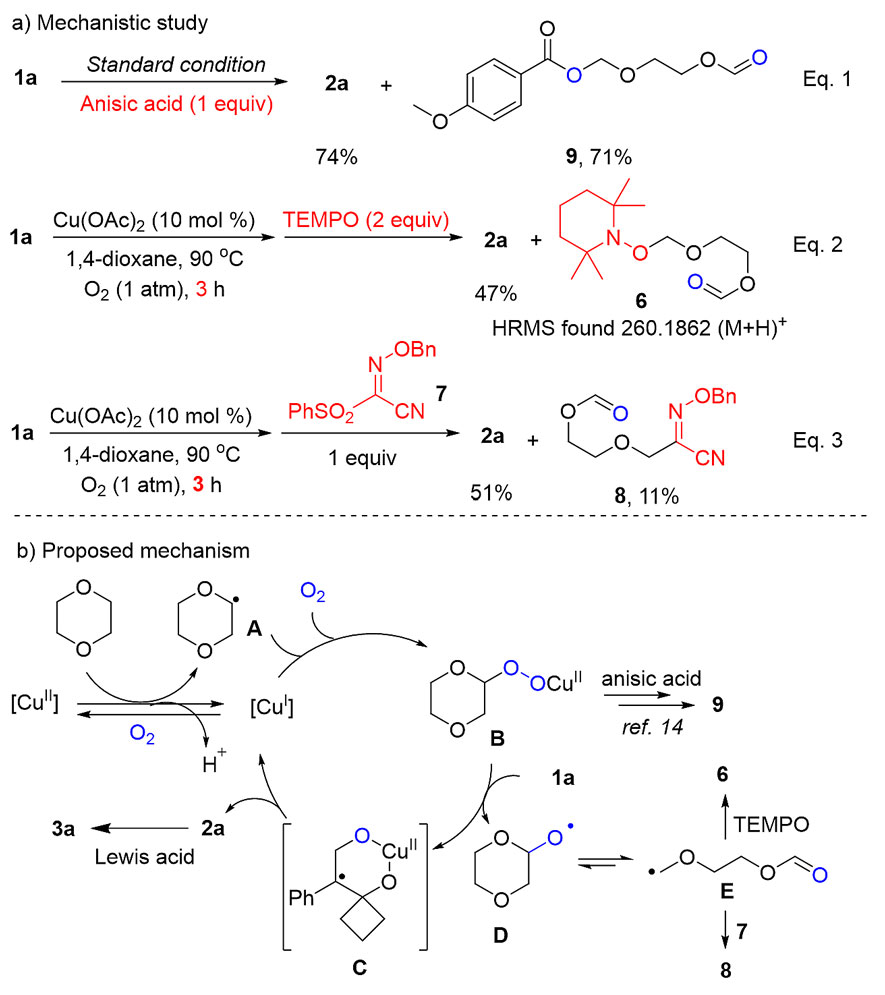
图3. 机理实验和反应机理
综上所述,本文利用氧气作为绿色氧化剂和氧源,高化学选择性地实现了三级烯丙醇的环氧化反应,发现并证明了常规溶剂1,4-二氧六环作为氧原子转移媒介的功能,相关工作发表在Angew. Chem. Int. Ed.上。该成果第一作者是北京大学硕士研究生朱本聪,通讯作者是北京大学焦宁教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Highly Selective Aerobic Oxygenation of Tertiary Allylic Alcohols with Molecular Oxygen
Bencong Zhu, Tao Shen, Xiaoqiang Huang, Song Song, Yuchao Zhu, Ning Jiao
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201903690
导师介绍
焦宁
https://www.x-mol.com/university/faculty/26819
(本稿件来自Wiley)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号