四氢异喹啉生物碱的精巧生物合成 | 瞿旭东团队Chem. Sci.
四氢异喹啉生物碱(tetrahydroisoquinoline alkaloids, THIQAs)是一类重要的天然产物,通常在C-1位含有苄基(即苄基异喹啉生物碱,BIAs)或苯基(即苯基异喹啉生物碱,PIAs)并具有显著的生物活性(图1)。目前,临床上已经应用十几种天然或半合成的THIQAs来治疗多种疾病。不过,自然条件下多数THIQAs只存在于各种植物中,提取不易,因此科学家们一直致力于开发其人工合成方法。然而,不对称催化等化学合成法对映选择性较差,成本昂贵,无法进行商业规模生产。于是不少科学家将视线转向生物合成。在天然产物中,四氢异喹啉(THIQ)骨架通过去甲乌药碱合成酶(norcoclaurine synthases, NCSs)催化的Pictet-Spengler反应进行生物合成(图2A)。随着对BIAs生物合成理解的日益深入,在微生物宿主中引入植物的部分或者全部生物合成途径相关基因,通过生物合成法来生产BIAs已经成为一种可行的策略。相比于化学合成法,这种方法更经济、操作更简单,从而更具有吸引力。然而,通过微生物生产植物THIQAs仍然存在许多挑战,比如:(1)对于PIAs及许多BIAs的生物合成途径的理解,目前还并不清楚,难以转移到微生物中,目前有成功报道的也只是少数BIAs;(2)大多数高价值THIQAs都带有许多取代基,例如在C6、C7、C3'和C4'位置上带有甲氧基;(3)在微生物中引入植物基因一方面会加大微生物的代谢负担,另一方面,不少植物酶在微生物系统中表达较差或者活性较低。此外,NCSs的底物范围窄,难以用于合成多种THIQAs。

图1. 代表性的THIQAs。图片来源:Chem. Sci.
近日,上海交通大学和武汉大学的瞿旭东教授(点击查看介绍)课题组发展了一种生物催化方法,使用亚胺还原酶(imine reductases, IREDs)和N-甲基转移酶(N-methyltransferase, NMT)从二氢异喹啉(DHIQ)前体出发合成植物THIQAs(图2B)。亚胺还原酶IR45的工程化,可显著扩展其底物特异性,从而可以将1-苯基和1-苄基6,7-二甲氧基-DHIQs高效且立体选择性地转化为相应的(S)-四氢异喹啉((S)-THIQs)。乌药碱N-甲基转移酶(CNMT)能够进一步有效地将这些(S)-THIQ中间体转化为(S)-THIQAs。通过在一个反应中结合IRED、CNMT和葡萄糖脱氢酶(GDH),他们在大肠杆菌中构建了两种人工模拟生物合成途径,并成功地将其应用于5个(S)-THIQAs的合成。这种高效(自DHIQs产率100%)且易于调控(添加其他基因)的生物合成方法适用于生产各种植物THIQAs。相关成果发表在Chemical Science 上。

图2. 植物THIQA的生物合成法。图片来源:Chem. Sci.
Cryptostyline I、II和III(1-3,图1)是从植物中分离出的三个有代表性的PIAs,作者选择它们作为本研究的目标。通过化学合成,以较好的收率(90-91%)得到三种cryptostyline(1-3)的1-苯基-6,7-二甲氧基-DHIQ前体(1a-3a,图3)。先前的研究表明(S)-IRED IR45对1-苯基-DHIQ具有良好的耐受性,因此选择该酶用于新底物的活性测定,结果表明IR45能够有效地将1a还原为(S)-1-亚甲基二氧苯基-6,7-二甲氧基-THIQ(1b,图2),转化率为100%,ee 值≥99%(图4),但它对两个空间位阻较大的底物2a和3a却没有活性。
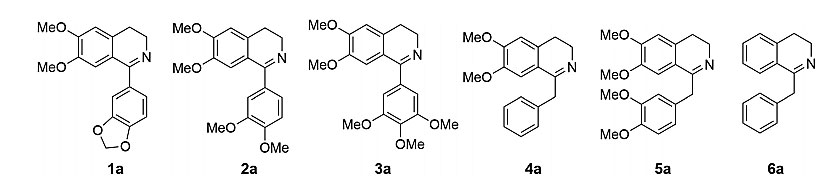
图3.本研究中涉及到的DHIQ底物。图片来源:Chem. Sci.

图4. IR45及其突变体对1a-5a的转化率和对映选择性。图片来源:Chem. Sci.
作者进行了底物1a与IR45的分子对接研究,在IR45结合口袋中,计算模型显示1a被天冬氨酸(D183)和NADPH紧密包围(图5)。其中亚胺键的位置靠近NADPH的si-面,这与产物的S-构型一致。从模型中可以看出,右侧的裂口是容纳亚甲基二氧苯基的主要限制因素(图5)。然而,对该区域进行酶工程可能会严重损害酶的活性和稳定性。因此,作者设想通过突变结合口袋底部的F190和W191残基,或许可以扩大结合口袋,让底物进入左腔稍微深一些,从而有可能减少右侧裂口与底物2a和3a之间的空间位阻。先前的研究显示W191在底物结合和维持酶的催化活性构象中发挥着重要作用。随后将W191进一步突变并对其进行动力学分析,结果表明W191F对酶的催化构象影响最小。接着,作者将W191F顶部的其他19个残基进行突变,结果显示突变体F190L-W191F能够显著提高2a和3a的活性(24 h内的转化率分别为75%和100%),并且产物2b和3b的立体选择性很好(图2、图4)。这些结果说明,通过酶工程作者成功地拓宽了IR45的底物特异性,并使有效地将大位阻DHIQ前体转化为相应的THIQ。

图5. 底物1a和4a与IR45结合的模型。图片来源:Chem. Sci.
接下来,作者将IR45应用于BIAs的合成。值得注意的是,野生型IR45能够有效地将DHIQ底物4a和5a转化为相应的(S)-THIQ(转化率100%;ee 值> 99%)。最佳突变体F190M-W191F能够显著提高对4a和5a的催化活性(图6)。有趣的是,野生型IR45所不能催化转化的大位阻底物2a和3a,其平面骨架却比4a和5a的还要小一些,这有点让人意外。为了探索酶腔中结合的差异对催化活性的影响,作者进行了4a与IR45的分子对接研究(图5B)。计算分析表明4a的DHIQ平面与1a的构象相同。不同于1a,4a的苄基向右侧裂口下方的大空腔弯曲,这种定位上的差异可能会减少原本较大的底物4a的空间位阻。
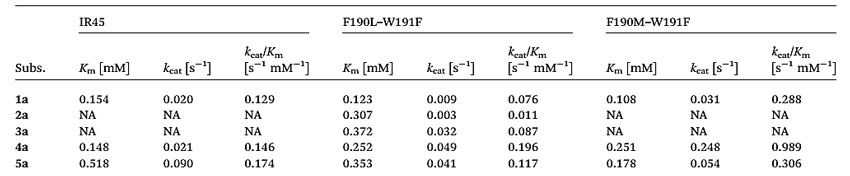
图6. IR45及其突变体与1a-5a转化的酶动力学研究。图片来源:Chem. Sci.
接下来,作者研究了N-甲基化步骤。CNMT是(S)-reticulene合成过程中的关键酶,作者分析了它对THIQ底物1b-5b的N-甲基化活性。为了改善表达,作者将CNMT基因针对大肠杆菌进行了密码子优化。而且结果也让人满意,CNMT在大肠杆菌中得到了很好的表达。得到的CNMT能够有效地将所有的S-THIQ底物转化为相应的N-甲基化产物(转化率100%)。作者随后尝试将亚胺还原酶和N-甲基化酶结合起来,他们用纯化的F190L-W191F和F190M-W191F与CNMT和GDH(用于从葡萄糖中回收NADPH),分别合成了THIQAs 2、3和1、4、5。反应结果也让人满意,底物转化率为100%。
在这些结果的支持下,作者尝试在大肠杆菌中构建THIQAs的人工生物合成途径。为了达到最高的转化效率,每个步骤都在大肠杆菌系统中进行了单独评估,然后进行条件优化。首先作者在单个细胞中共表达了三种酶IRED、NMT、GDH,构建了微生物中合成THIQAs的最小生物合成途径。在最佳条件下,1a、4a和5a(50 mg L-1)可以在一到三天内完全转化为相应的生物碱(图7和图8);通过乙酸乙酯萃取,可以分别以95%、98%和95%的产率获得纯生物碱1、4和5。为了克服细胞膜通透性的障碍并进一步提高2a和3a的转化率,作者将酶促转化和全细胞生物转化结合到一个反应中。F190L-W191F和GDH这两种酶首先过表达,并通过超声裂解得到粗酶液,随后直接加入到表达CNMT的大肠杆菌的培养液中,这种酶促转化和全细胞生物转化的结合可以将2a和3a(50 mg L-1)完全转化为相应的THIQAs(图7和图8),2和3的分离产率分别为93%和96%。这些结果表明,通过系统性地提高酶活性并优化生物催化条件,作者发展的基于IRED的人工生物合成途径可成功地用于两种类型植物THIQAs的合成。

图7.前体1a-5a通过IRED的方法生物合成1-5。图片来源:Chem. Sci.

图8. 基于IRED生物合成THIQAs 1-5。图片来源:Chem. Sci.
总结
瞿旭东教授课题组使用一种基于IRED的生物催化策略,成功地生物合成5种在药学上有价值的PIAs和BIAs。值得注意的是,这3种PIA的天然生物合成途径目前尚未研究清楚。通过酶工程,作者显著拓宽了IRED IR45的底物特异性,两个突变体F190L-W191F和F190M-W191F可以有效地将大位阻1-芳基-6,7-二甲氧基-DHIQ底物转化为(S)-THIQs,CNMT也能够实现大位阻底物的转化,再将(S)-THIQs转化为(S)-THIQAs。这种基于IRED的生物合成法可高效(100%收率)制备多种植物THIQAs,通过添加其他酶(如P450),还有望进一步扩展到其他复杂THIQAs的生物合成中。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Biosynthesis of plant tetrahydroisoquinoline alkaloids through an imine reductase route
Lu Yang, Jinmei Zhu, Chenghai Sun, Zixin Deng, Xudong Qu
Chem. Sci., 2019, DOI: 10.1039/c9sc03773j
导师介绍
瞿旭东
https://www.x-mol.com/university/faculty/49560
关于Chemical Science:
英国皇家化学会综合性旗舰期刊,最新影响因子为9.556。发表化学领域最前沿、最重要、最具挑战性的高影响力研究成果。Chemical Science 是化学领域中影响力最大的开放获取期刊(open access),所有文章均可免费阅读。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号