天然产物(+)-sarcophytin的全合成
肉质软珊瑚是一类广为研究的肉兰属植物,其中可分离得到多种西松烷二萜类天然产物,几十年来一直都是合成化学家的研究热点。1998年,印度安德拉大学的Ammanamanchi Anjaneyulu等人从印度洋安达曼及尼克巴群岛的黄色皮革珊瑚中分离得到(+)-sarcophytin 1。随后一系列肉质软珊瑚家族的其他天然产物相继分离并表征,该类分子中包含顺-反-顺构型的十二氢菲核心骨架,C10位的三级醇与C3或C14位的酮可形成桥连的半缩酮结构。到目前为止,许多课题组已对C3位无酮官能团的chatancin 3进行了合成研究,但对于sarcophytin 1的合成尚无报道。
最近,瑞士苏黎世联邦理工学院的Erick Carreira教授(点击查看介绍)从商品化的手性合成砌块出发,以烯酮作为亲双烯体、Z型的双烯酸酯作为双烯体,通过分子内的Diels–Alder环加成策略实现了(+)-sarcophytin 1及其对映异构体4的汇聚式合成。同时,他们还对(+)-sarcophytin的绝对构型进行了重新修正,由此确认了其正确结构。相关工作发表在Angew. Chem. Int. Ed. 上。
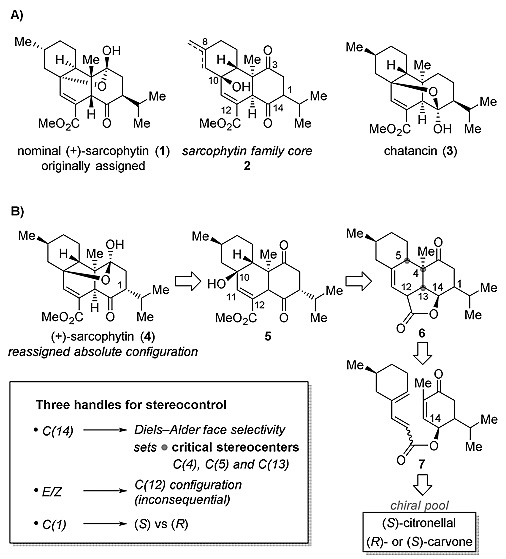
图1. sarcophytin (1)及其衍生结构和逆合成分析。图片来源:Angew. Chem. Int. Ed.
作者对4进行了逆合成分析,4中的C(11)-C(12)双键可以通过跨环的Diels–Alder反应进行构建。而在逆合成分析中一个关键的问题是,6中C(10)-C(11)双键的C(10)位能否引入一个羟基,同时产生不饱和酯5。四环中间体6可以从酯7通过Diels–Alder反应来构建。中间体7可以断裂为两个复杂程度相似的片段,从而实现汇聚式合成。中间体7中C(14)的构型对面选择性的控制至关重要,其构型会对C(4)、C(5)和C(13)的立体中心造成重要影响。此外,天然产物的C(12)位为sp2杂化,这就涉及中间体7中双烯酸酯需要选择顺式构型还是反式构型。考虑到天然产物中的C(1)位易于发生差向异构化,中间体7中也存在C(1)的构型需要选择R 还是S 的问题。这种逆合成分析思路可通过控制环加成反应的条件,将中间体7高效地转化为特定立体构型的6,因而具有灵活可控性。
羟基烯酮9的制备已有文献报道,香茅醛10在PCC的作用下得到中间体11,接着在盐酸水溶液回流条件下发生异构化/逆Aldol缩合反应,以两步54%的总收率得到(S)-3-甲基环己酮中间体12。当作者使用大位阻的碱LDA或LiTMP时,目标产物环己烯基三氟甲磺酸酯13和副产物14的比例是2/1及3.4/1,而当使用NaHMDS作为碱,以二乙二醇二甲醚为溶剂,12与Comins试剂反应,以6/1的选择性得到主要产物13,13接着与丙烯酸甲酯发生Heck反应并水解,以59%的两步总收率得到反式的二烯酸15。为了合成顺式的二烯酸18,作者首先通过Negishi反应合成环己烯基炔基酯17,随后进行水解,并在Lindlar催化剂的催化氢化作用下顺利得到顺式二烯酸18。
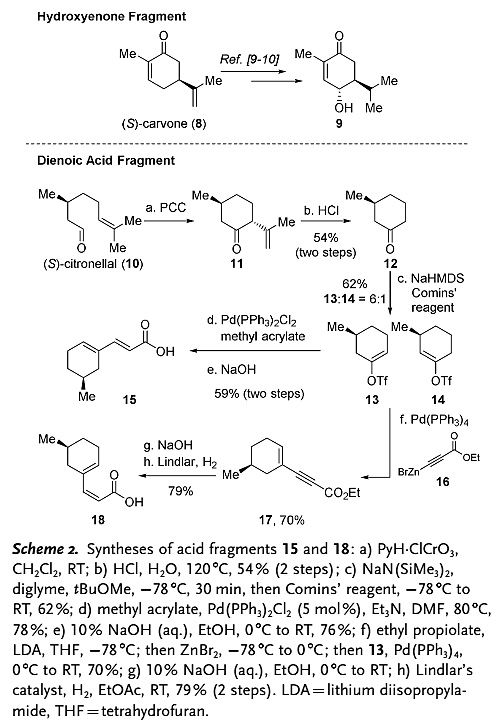
图2. 中间体15和18的合成。图片来源:Angew. Chem. Int. Ed.
作者通过羟基烯酮ent-9分别与双烯体15和18发生DCC参与的酯化反应,合成了(E, anti )-19和(Z, anti )-19,两种中间体的C(1)位均是R构型。(E, anti )-19即使在150 ℃的加热条件下也不反应,(Z, anti )-19在100 ℃加热时能以54%的产率得到(1R,12S )-20中间体,然而中间体18与ent-9酯化得到的产物(Z, anti )-19产率较低,(E, anti )-19是主要副产物。作者还通过Mitsunobu反应合成了(E, syn )-19和(Z, syn )-19,其C(1)位均是S构型。(E, syn )-19即使在150 ℃加热条件下也不反应,而(Z, syn )-19在100 ℃的条件下就能以76%的产率得到(1S,12S)-20中间体。
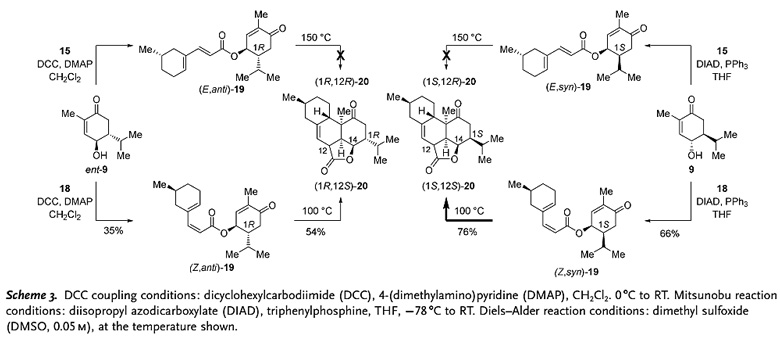
图3. Diels–Alder环加成反应。图片来源:Angew. Chem. Int. Ed.
(1S,12S )-20继续进行烯烃环氧化反应,随后在DBU的作用下环氧开环得到烯丙醇中间体21,其构型通过X射线单晶衍射加以确定。21接着在碱性条件下,以K2S2O8作为氧化剂,在过渡金属盐RuCl3•nH2O的参与下发生内酯开环和醇羟基氧化反应,随后C(1)位发生原位差向异构化和半缩酮化,以64%的总收率得到中间体23。羧酸23进行酯化,最终完成了(+)-Sarcophytin的合成。
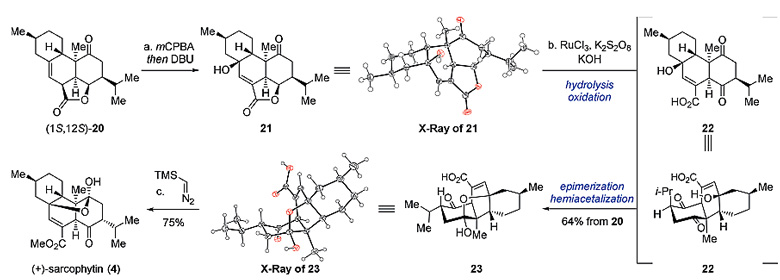
图4. (+)-sarcophytin 1的全合成。图片来源:Angew. Chem. Int. Ed.
分离得到的天然产物绝对构型一直存在一些疑问,这些怀疑来源于1中的十二氢菲核心骨架与其他同一家族的次级代谢产物如chatancin 3中C(5)、C(8)、C(10)和C(13)位置的立体中心为对映异构的关系。作者首先以(+)-sarcophytin 1中标注的绝对构型的分子为合成目标,以(R )-(-)-香芹酮和(R )-(+)-胡薄荷酮为起始合成原料,最终得到旋光值相反的产物(-)-sarcophytin 4。因此,该合成工作也证实了以往的怀疑,说明(+)-sarcophytin的构型应该是与该类家族天然产物其他成员的构型是一致的。
——总结——
Erick Carreira教授通过分子内的Diels–Alder环加成策略实现了(+)-sarcophytin 1的汇聚式合成,与此同时还重新确定了(+)-sarcophytin 1的正确结构。Z 构型的双烯酸酯作为合适双烯体可用于高立体选择性地构建十二氢菲核心骨架。其他西松烷二萜类天然产物分子的合成也在进一步的研究中。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Total Synthesis of (+)-Sarcophytin
Angew. Chem. Int. Ed., 2017, DOI: 10.1002/anie.201711372
导师介绍
Erick Carreira
http://www.x-mol.com/university/faculty/2773
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号