当前位置:
X-MOL 学术
›
Food Hydrocoll.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
A novel polysaccharide gel bead enabled oral enzyme delivery with sustained release in small intestine
Food Hydrocolloids ( IF 11.0 ) Pub Date : 2018-11-01 , DOI: 10.1016/j.foodhyd.2018.05.039 Yi-Wei Wang , Li-Ye Chen , Feng-Ping An , Man-Qian Chang , Hong-Bo Song
Food Hydrocolloids ( IF 11.0 ) Pub Date : 2018-11-01 , DOI: 10.1016/j.foodhyd.2018.05.039 Yi-Wei Wang , Li-Ye Chen , Feng-Ping An , Man-Qian Chang , Hong-Bo Song
|
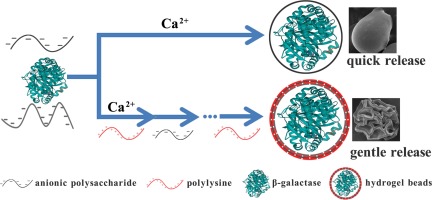
Abstract We report a novel oral delivery system based on sodium alginate/κ-carrageenan binary polysaccharide gel bead. β-galactase was selected as a model molecule to evaluate the capacity of the beads as delivery system. After enzyme encapsulation, the hydrogel beads were subsequently coated with κ-carrageenan (κ-CG) and e-polylysine (e-PL). Scanning electron microscope (SEM) images revealed the microstructural differences between the beads synthesized with and without e-PL coating. Fourier transform infrared spectroscopy (FTIR) spectra further proofed the successful coating of e-PL and κ-CG. Releasing studies showed that the enzyme releasing time is significantly prolonged by e-PL coating. In vitro experiments showed that, the hydrogel beads synthesized with 0.6% e-PL were stable and compact in the simulated gastric fluid environment with negligible swelling, which can protect the loaded enzyme effectively. More than 94.6% lactase activity can be retained after treated with simulated gastric fluid (pH 4) for 2 h. After transferred into simulated small intestinal fluid for 14 h (pH 7.4), as much as 89.6% of the enzyme can be released from the beads. It is worthy to note that the activity of the released enzyme retained 76.0% of total enzyme activity. These unique properties of the hydrogel beads enabled the effectively maintenance of enzyme bioactivity and thus enhanced the enzyme delivery and therapeutic efficiency. The reported delivery system is an ideal oral delivery system for bioactive food compounds, especially for compounds that are unstable in gastric environment.
中文翻译:

一种新型多糖凝胶珠使口服酶在小肠中持续释放
摘要 我们报告了一种基于海藻酸钠/κ-角叉菜胶二元多糖凝胶珠的新型口服给药系统。选择β-半乳糖酶作为模型分子来评估珠作为递送系统的能力。酶包封后,水凝胶珠随后用κ-角叉菜胶(κ-CG)和e-聚赖氨酸(e-PL)包被。扫描电子显微镜 (SEM) 图像揭示了使用和不使用 e-PL 涂层合成的珠子之间的微观结构差异。傅里叶变换红外光谱 (FTIR) 光谱进一步证明了 e-PL 和 κ-CG 的成功涂层。释放研究表明,e-PL 涂层显着延长了酶的释放时间。体外实验表明,合成的水凝胶珠含有 0. 6%的e-PL在模拟胃液环境中稳定且致密,肿胀可忽略不计,可以有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。能有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。能有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。用模拟胃液(pH 4)处理2小时后可保留6%的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。用模拟胃液(pH 4)处理2小时后可保留6%的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。
更新日期:2018-11-01
中文翻译:

一种新型多糖凝胶珠使口服酶在小肠中持续释放
摘要 我们报告了一种基于海藻酸钠/κ-角叉菜胶二元多糖凝胶珠的新型口服给药系统。选择β-半乳糖酶作为模型分子来评估珠作为递送系统的能力。酶包封后,水凝胶珠随后用κ-角叉菜胶(κ-CG)和e-聚赖氨酸(e-PL)包被。扫描电子显微镜 (SEM) 图像揭示了使用和不使用 e-PL 涂层合成的珠子之间的微观结构差异。傅里叶变换红外光谱 (FTIR) 光谱进一步证明了 e-PL 和 κ-CG 的成功涂层。释放研究表明,e-PL 涂层显着延长了酶的释放时间。体外实验表明,合成的水凝胶珠含有 0. 6%的e-PL在模拟胃液环境中稳定且致密,肿胀可忽略不计,可以有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。能有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。能有效保护负载的酶。用模拟胃液 (pH 4) 处理 2 小时后,可保留 94.6% 以上的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。用模拟胃液(pH 4)处理2小时后可保留6%的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。用模拟胃液(pH 4)处理2小时后可保留6%的乳糖酶活性。转移到模拟小肠液中 14 小时 (pH 7.4) 后,可以从珠子中释放多达 89.6% 的酶。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。值得注意的是,释放的酶的活性保留了总酶活性的 76.0%。水凝胶珠的这些独特性质能够有效维持酶的生物活性,从而提高酶的传递和治疗效率。报道的递送系统是生物活性食物化合物的理想口服递送系统,特别是对于在胃环境中不稳定的化合物。











































 京公网安备 11010802027423号
京公网安备 11010802027423号