当前位置:
X-MOL 学术
›
ChemBioChem
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Substrate Binding Drives Active‐Site Closing of Human Blood Group B Galactosyltransferase as Revealed by Hot‐Spot Labeling and NMR Spectroscopy Experiments
ChemBioChem ( IF 2.6 ) Pub Date : 2018-04-14 , DOI: 10.1002/cbic.201800019 Sophie Weissbach 1 , Friedemann Flügge 1 , Thomas Peters 1
ChemBioChem ( IF 2.6 ) Pub Date : 2018-04-14 , DOI: 10.1002/cbic.201800019 Sophie Weissbach 1 , Friedemann Flügge 1 , Thomas Peters 1
Affiliation
|
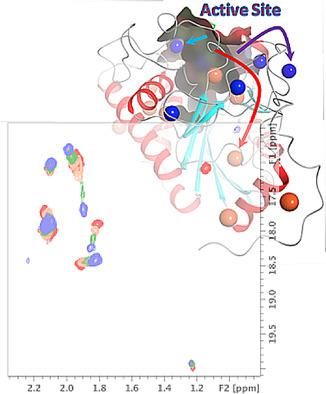
In a bind: Binding of substrates to the active site of human blood group B glycosyltransferase determines the timescales of conformational transitions, as reported by chemical‐shift perturbations of the methyl groups of Met residues and the side‐chain NH groups of Trp residues.

中文翻译:

底物结合驱动人类血型B组半乳糖基转移酶的主动位点关闭,热点标记和NMR光谱实验揭示了这一点
在结合中:底物与人血B型糖基转移酶活性位点的结合决定了构象转变的时间尺度,这是由Met残基的甲基和Trp残基的侧链NH基团的化学位移扰动所报告的。

更新日期:2018-04-14

中文翻译:

底物结合驱动人类血型B组半乳糖基转移酶的主动位点关闭,热点标记和NMR光谱实验揭示了这一点
在结合中:底物与人血B型糖基转移酶活性位点的结合决定了构象转变的时间尺度,这是由Met残基的甲基和Trp残基的侧链NH基团的化学位移扰动所报告的。












































 京公网安备 11010802027423号
京公网安备 11010802027423号