当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
The Effect of Water on Quinone Redox Mediators in Nonaqueous Li-O2 Batteries
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2018-01-18 , DOI: 10.1021/jacs.7b11007 Tao Liu 1 , James T. Frith 2 , Gunwoo Kim 1, 3 , Rachel N. Kerber 1 , Nicolas Dubouis 1 , Yuanlong Shao 3 , Zigeng Liu 1 , Pieter C. M. M. Magusin 1 , Michael T. L. Casford 1 , Nuria Garcia-Araez 2 , Clare P. Grey 1
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2018-01-18 , DOI: 10.1021/jacs.7b11007 Tao Liu 1 , James T. Frith 2 , Gunwoo Kim 1, 3 , Rachel N. Kerber 1 , Nicolas Dubouis 1 , Yuanlong Shao 3 , Zigeng Liu 1 , Pieter C. M. M. Magusin 1 , Michael T. L. Casford 1 , Nuria Garcia-Araez 2 , Clare P. Grey 1
Affiliation
|
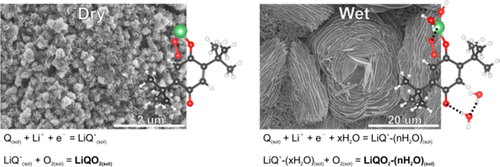
The parasitic reactions associated with reduced oxygen species and the difficulty in achieving the high theoretical capacity have been major issues plaguing development of practical nonaqueous Li-O2 batteries. We hereby address the above issues by exploring the synergistic effect of 2,5-di-tert-butyl-1,4-benzoquinone and H2O on the oxygen chemistry in a nonaqueous Li-O2 battery. Water stabilizes the quinone monoanion and dianion, shifting the reduction potentials of the quinone and monoanion to more positive values (vs Li/Li+). When water and the quinone are used together in a (largely) nonaqueous Li-O2 battery, the cell discharge operates via a two-electron oxygen reduction reaction to form Li2O2, with the battery discharge voltage, rate, and capacity all being considerably increased and fewer side reactions being detected. Li2O2 crystals can grow up to 30 μm, more than an order of magnitude larger than cases with the quinone alone or without any additives, suggesting that water is essential to promoting a solution dominated process with the quinone on discharging. The catalytic reduction of O2 by the quinone monoanion is predominantly responsible for the attractive features mentioned above. Water stabilizes the quinone monoanion via hydrogen-bond formation and by coordination of the Li+ ions, and it also helps increase the solvation, concentration, lifetime, and diffusion length of reduced oxygen species that dictate the discharge voltage, rate, and capacity of the battery. When a redox mediator is also used to aid the charging process, a high-power, high energy density, rechargeable Li-O2 battery is obtained.
中文翻译:

水对非水锂氧电池中醌氧化还原介质的影响
与氧物种减少相关的寄生反应和难以实现高理论容量一直是困扰实用非水锂氧电池发展的主要问题。我们在此通过探索 2,5-二叔丁基-1,4-苯醌和 H2O 对非水 Li-O2 电池中氧化学的协同作用来解决上述问题。水可以稳定醌单阴离子和二价阴离子,将醌和单阴离子的还原电位转移到更正的值(相对于 Li/Li+)。当水和醌一起用于(主要)非水 Li-O2 电池时,电池放电通过双电子氧还原反应形成 Li2O2,电池放电电压、倍率和容量均显着增加,并且检测到的副反应较少。Li2O2 晶体可以长到 30 μm,比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进放电时醌以溶液为主导的过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。
更新日期:2018-01-18
中文翻译:

水对非水锂氧电池中醌氧化还原介质的影响
与氧物种减少相关的寄生反应和难以实现高理论容量一直是困扰实用非水锂氧电池发展的主要问题。我们在此通过探索 2,5-二叔丁基-1,4-苯醌和 H2O 对非水 Li-O2 电池中氧化学的协同作用来解决上述问题。水可以稳定醌单阴离子和二价阴离子,将醌和单阴离子的还原电位转移到更正的值(相对于 Li/Li+)。当水和醌一起用于(主要)非水 Li-O2 电池时,电池放电通过双电子氧还原反应形成 Li2O2,电池放电电压、倍率和容量均显着增加,并且检测到的副反应较少。Li2O2 晶体可以长到 30 μm,比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进放电时醌以溶液为主导的过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。比单独使用醌或不使用任何添加剂的情况大一个数量级以上,这表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。表明水对于促进释放醌的溶液主导过程至关重要。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。醌单阴离子催化还原 O2 是上述吸引人的特征的主要原因。水通过氢键形成和 Li+ 离子的配位来稳定醌单阴离子,它还有助于增加还原氧物质的溶剂化、浓度、寿命和扩散长度,这些物质决定了电池的放电电压、速率和容量. 当氧化还原介质也用于辅助充电过程时,可以获得高功率、高能量密度、可充电的 Li-O2 电池。











































 京公网安备 11010802027423号
京公网安备 11010802027423号