南京大学在基于纳米模拟酶的生物活体分析领域取得新进展
纳米模拟酶(nanozyme)是一类具有与某些天然酶类似生物催化活性的纳米材料。随着近几年纳米技术的飞速发展,这类人工模拟酶开始引起科研人员的研究兴趣。这主要是因为与传统的基于环糊精类化合物、金属有机化合物或者分子印迹聚合物等人工模拟酶相比,纳米模拟酶具有易于大规模制备、成本低廉、催化性能相对稳定等优势。此外,由于纳米模拟酶本身又是一种纳米材料,因此它们又具有纳米材料自身的特点,如比表面高,具有特殊的光、电、磁等物理化学性质等。正是这些独特的性质,纳米模拟酶在生物传感、生物医学与成像以及环保等领域表现出得天独厚的优势。
金属有机骨架化合物(Metal-organic frameworks, MOFs)是近十年来迅猛发展的一类多孔化合物。它们往往通过不同金属离子/金属簇与配体之间的配位作用形成具有规则拓扑结构的无限网络骨架。由于配位金属离子/某些特殊配体本身还可以作为催化中心,因此MOFs在催化领域表现出广阔的应用前景。随着研究的深入,许多MOFs也发掘出纳米模拟酶的特性,从而赋予其更多的应用价值。但研究人员也发现许多制备的块体类MOFs生物催化活性并不是十分理想,主要是因为底物在这些块体类MOFs内部需要扩散较长的距离才能和催化中心发生反应。另一方面,块体类MOFs的比表面积往往不高,由此限制了研究人员通过调控其表界面化学的性质来设计高灵敏、高选择性的生物识别界面。
在该研究中,南京大学、南京大学鼓楼医院及湖南大学的研究人员密切合作,通过“自下而上”的方法,以4-羧基金属卟啉为配体,制备了一系列具有二维拓扑结构的MOFs纳米片,它们基本都具有类过氧化氢酶的生物催化活性。进一步的研究表明,这些MOFs纳米片普遍具有比块体MOFs材料更高的类过氧化氢酶催化活性。一方面,这类MOFs纳米片具有比块体MOFs更高的比表面积;另一方面,底物扩散至催化中心的距离相比于块体MOFs大大降低。课题组的成员还深入研究了这类MOFs纳米片的催化机制,发现其类过氧化氢酶的催化活性主要来源于材料内部的金属卟啉本身而非配位金属离子。此外,对于不同的金属卟啉,基于铁卟啉的MOFs纳米片生物催化活性最佳,可用于设计新型的生物识别界面。
研究人员发现这类MOFs纳米片的催化活性可以通过改变表面的电荷状态进行调控,而这一过程在块状MOFs材料或者单独的铁卟啉配体中难以进行。基于该原理,他们利用对肝素(heparin)具有选择性识别作用的多肽AG73调控MOFs纳米片的催化活性,并进一步建立一种肝素检测生物传感器。他们发现这种基于MOFs纳米片的生物传感器对于肝素的检测具有很好的灵敏度和选择性,完全可以用于生物体内肝素的检测。因此,他们将其应用于大鼠血液中肝素的检测,并进一步研究了大鼠体内肝素的代谢。
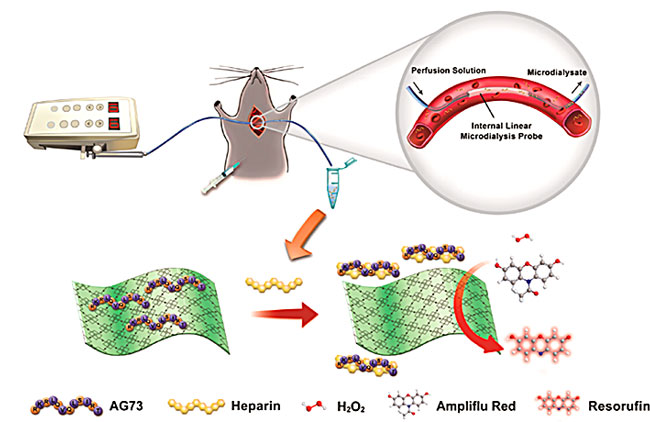
基于MOF纳米片过氧化物酶活性的大鼠体内肝素的检测
这一研究不仅为MOFs材料在生物医学领域的研究指明了新的方向和思路,也为临床肝素的检测发展了一种新的分析技术。该研究工作发表在近期的Analytical Chemistry 上。
该论文作者为:Hanjun Cheng, Yufeng Liu, Yihui Hu, Yubin Ding, Shichao Lin, Wen Cao, Qian Wang, Jiangjiexing Wu, Faheem Muhammad, Xiaozhi Zhao, Dan Zhao, Zhe Li, Hang Xing and Hui Wei
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Monitoring of Heparin Activity in Live Rats Using Metal-Organic Framework Nanosheets as Peroxidase Mimics
Anal. Chem., 2017, DOI: 10.1021/acs.analchem.7b02895
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号