Angew:治疗蛋白光响应可控释放的新突破
生物大分子药物载体的出现无疑是近年来疾病治疗领域的革命性技术突破;尤其是蛋白重组技术和单克隆抗体技术的出现,使得生物大分子成为来源广泛、高效的药物载体。如雷珠单抗、阿柏西普以及贝伐单抗已经作为一类安全、高效的抗血管生成治疗大分子药物广泛的应用于癌症、老年性黄斑变性(AMD)等疾病的治疗。但是,目前该类生物大分子药物在人体内易生物降解、体内半衰期短,在治疗过程中需要定期的通过静脉注射等方式进行药物补充,这使得在AMD等疾病的治疗过程中往往会引发一系列并发症状,不利于患者的康复。因此,急需开发一种药物缓释系统进行药物的可控释放,以达到持续治疗的目的。
刺激响应性水凝胶兼具与良好的人体生物相容性和智能可控性,是当前药物缓释领域的研究热点材料。对温度、pH、酶、光等不同外界刺激具有响应性的有机(如偶氮苯、螺吡喃等)/无机(如Fe3O4、GO等纳米材料)组分常被引入水凝胶体系中,用以制备蛋白缓释体系。其中,基于光的远程、精确、即时可控,光响应性水凝胶体系成为药物精确可控缓释的重要载体材料。
近日,澳大利亚的Timothy C. Hughes博士和北京化工大学谭天伟(Tianwei Tan)教授(点击查看介绍)研究团队在Angew. Chem. Int. Ed.发表文章,在温敏性琼脂糖水凝胶体系中引入聚合物包覆的金纳米颗粒(AuNPs),基于AuNPs的光热效应引发凝胶体系局部升温、水凝胶基体软化,实现了治疗药物的局部光控释放。
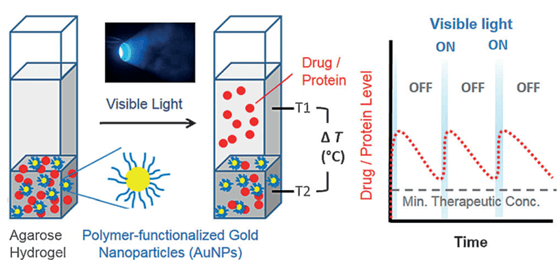
图1. AuNPs-琼脂糖水凝胶体系光控药物释放示意图。图片来源:Angew. Chem. Int. Ed.
AuNPs表面通过聚(甲基丙烯酰氧乙基三甲基氯化铵)(P(METAC))进行修饰后引入水凝胶体系,基于琼脂糖水凝胶较低的熔点(Tm ≤ 45℃)和AuNPs可见光范围内的优异光热效应,研究团队选用400-500 nm波段的可见光进行治疗蛋白的可控释放研究。在光照条件下(508 mW/cm2, 10 min)AuNPs-水凝胶体系局部温度升高(T:35 ℃→48 ℃),基体存储模量(G’)降低22%,从而显著提高了药物蛋白的扩散释放速率。
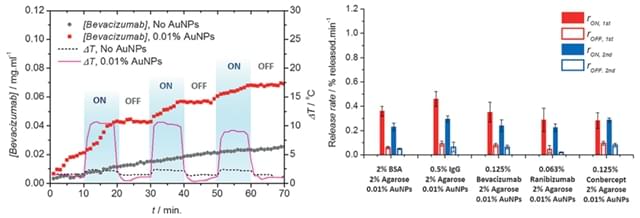
图2. AuNPs光热效应显著提高体系的药物释放速率。图片来源:Angew. Chem. Int. Ed.
AuNPs-琼脂糖水凝胶体系的药物蛋白释放速率能够通过调节AuNPs/琼脂糖浓度、光强及光照时间进行精确控制。更为重要的是,该光响应性凝胶体系经过长期的药物缓释循环后,仍能够维持贝伐单抗等药物的高活性,展现出优异的治疗效果。
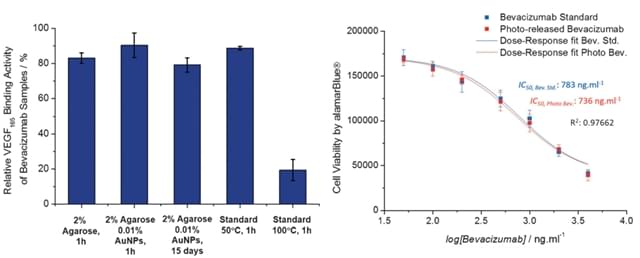
图3. 多个释放周期后药物蛋白仍维持其高活性和疗效。图片来源:Angew. Chem. Int. Ed.
研究团队进一步对AuNPs-琼脂糖水凝胶体系在实际治疗环境中的局部光热效应以及药物释放速率进行了详细的研究,研究表明该凝胶体系通过光控能够有效的实现眼组织部位药物的精确、局部可控释放。
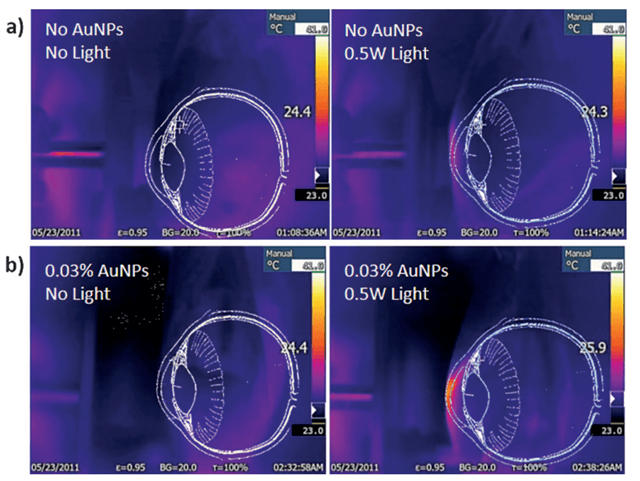
图4. AuNPs-琼脂糖水凝胶体系在实际治疗环境(牛眼)中应用(局部光热)效果。图片来源:Angew. Chem. Int. Ed.
—— 总结 ——
金纳米球、纳米壳、纳米棒等纳米材料在红外线照射下能够产生明显的光热效应,被广泛的应用于光响应性载药系统。不同于以往采用AuNPs与聚异丙基丙烯酰胺(P(NIPAAm))结合进行细胞吞噬/摄取、溶解酶素等药物缓释方面的研究;该论文将AuNPs进行表面修饰后引入温敏性的琼脂糖水凝胶体系中,制备了可见光响应性的高效普适性药物缓释系统。该体系局部药物释放速率能够通过调节AuNPs/琼脂糖含量、光照强度/时间等参数进行精确调控;而且,其多个释放周期后药物仍维持较高活性。基于该体系的低细胞毒性、药物普适性以及体系的远程药物释放可控性,该水凝胶药物缓释体系在眼部慢性疾病方面的治疗方面展现出广阔的应用前景。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Photo-Modulated Therapeutic Protein Release from a Hydrogel Depot Using Visible Light
Angew. Chem. Int. Ed., 2017, 56, 966-971, DOI: 10.1002/anie.201610618
导师介绍
谭天伟教授
http://www.x-mol.com/university/faculty/35088
(本文由甲子湖供稿)
