"点击化学"实现激酶活性低成本快捷检测
蛋白激酶在生物体内的能量转移过程中起到关键的作用,它可以控制细胞的分裂、生长和凋亡,同时也可以调节细胞的代谢途径甚至细胞通讯。如果蛋白激酶的活性失去控制,就可能导致某些疾病的发生,更严重的会诱发癌症。
许多抗癌药物研究的出发点就是以蛋白激酶作为药物的作用靶点,通过调节蛋白激酶的活性来控制癌细胞的增殖、侵袭和转移,从而达到治疗癌症的目的。目前,检测激酶活性的普遍方法是同位素检测,但是放射性同位素不但昂贵,而且保质期比较短。此外,由于放射性同位素的管制,这种方法的应用也有诸多不便。

近来,多伦多大学的Bernie Kraatz实验室研发出了一种新的化合物,可以更方便地检测蛋白激酶的活性,而且大大降低了检测成本。该研究团队合成了一种二茂铁(Fc)与ATP的共轭化合物,这种化合物在激酶的作用下,其γ-磷酸-Fc基团被转移到肽或者蛋白质上。首先,将肽或者蛋白质固定在N-羟基硫辛酸活性酯(LPA)改性的金表面,当加入这种化合物与激酶作用后,γ-磷酸-Fc基团被转移到了被固定的肽或者蛋白质,然后利用电化学方法,或使用二茂铁抗体通过免疫方法来检测这些被固定的肽或蛋白质上的γ-磷酸-Fc基团数目,就可以得出该激酶的活性。
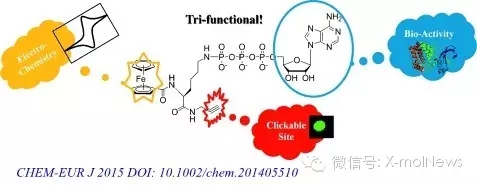
另外,该团队巧妙地利用点击化学,直接将荧光染料分子连接到激酶作用后的二茂铁化合物上,从而使激酶的活性检测变得更加方便快捷,也为临床医生测定激酶活性和筛选有效药物开辟了新道路。这项研究成果发表在《Chemistry-A European Journal》上。
http://onlinelibrary.wiley.com/doi/10.1002/chem.201405510/full
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号