匡华研究团队报道手性纳米组装体诱导细胞自噬的研究进展
自噬是真核细胞通过自身的溶酶体途径降解多余的细胞质蛋白或细胞器,从而实现营养物质循环利用的生命过程。自噬调控的紊乱与许多疾病的产生密切相关,因此精准调控自噬反应的过程对维持细胞正常生理功能具有重要的作用。近日,江南大学食品科学与技术国家重点实验室的匡华教授(点击查看介绍)研究团队率先发现了不同构型的手性纳米组装体能够选择性激活细胞内的自噬反应,并能够通过圆二色光谱以及上转换发光对自噬过程进行监测。相关成果发表在Nature Communications上。
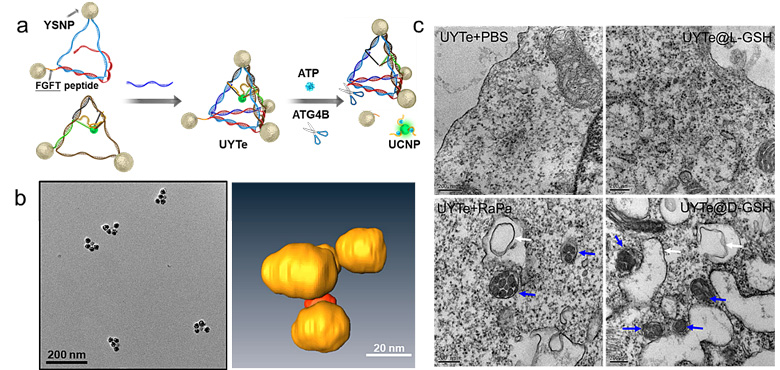
图1.(a)上转换纳米粒子内嵌的金核壳纳米粒子四面体组装的过程;(b)四面体的透射电镜图以及冷冻电镜的三维重构图;(c)D型或者L型谷胱甘肽修饰的四面体与细胞培养后的生物电镜图。
匡华教授团队利用DNA自组装技术,将核壳结构的金纳米粒子组装成手性四面体结构。其中一条的DNA末端修饰有能被自噬标志物ATG4B水解的多肽链,并且在四面体内部进一步采用ATP适配体组装上转换纳米粒子(图1a-b)。在组装体表面修饰D型或者L型谷胱甘肽时,四面体能够表现出可调控的圆二色光谱。有趣的是,当这种内嵌上转换纳米粒子的四面体与细胞进行培养时,D型谷胱甘肽修饰的四面体结构能够引起细胞产生强烈的自噬反应,而采用L型谷胱甘肽修饰的四面体并没有发现明显的自噬产生(图1c)。同时,当自噬发生时,四面体结构开始发生解离,使其手性信号降低,而内嵌于四面体内部的上转换纳米粒子能够发生解离,使猝灭的上转换发光能够恢复。
进一步的研究发现,D型谷胱甘肽修饰的四面体结构能够在细胞内大量富集,而L型谷胱甘肽修饰的四面体只有少部分发生聚集。与此同时,在与D型谷胱甘肽修饰的四面体培养的细胞内部能够检测到强烈的氧化应激产生,被认为是产生细胞自噬的主要原因。当自噬发生后,产生的ATG4B能够使细胞内的四面体解离。同时,自噬过程伴随着ATP的产生,使内嵌于四面体内部的上转换纳米粒子发生解离,从而使发光恢复。利用这一原理,细胞内的自噬程度可以被手性四面体原位激活,并通过圆二色信号以及上转换发光进行实时监测。最终这一手性四面体结构成功运用于活体肿瘤内的自噬激活与检测。
该研究诠释了手性组装体与细胞内自噬之间的关系,为进一步研究手性纳米材料与细胞内的代谢过程奠定基础。
博士后孙茂忠为该论文的第一作者,硕士生郝甜甜以及博士生瞿爱华为论文的共同第一作者,匡华教授为通讯作者。该工作在X射线小角散射方面得到了中科院上海应用物理研究所李晓芸博士的大力支持,并得到国家自然科学基金委优秀青年基金与重点基金等项目(21631005, 21673104, 21522102, 21503095)的资助。
该论文作者为:Maozhong Sun, Tiantian Hao, Xiaoyun Li, Aihua Qu, Liguang Xu, Changlong Hao, Chuanlai Xu & Hua Kuang
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Direct observation of selective autophagy induction in cells and tissues by self-assembled chiral nanodevice
Nat. Commun., 2018, DOI: 10.1038/s41467-018-06946-z
导师介绍
匡华
http://www.x-mol.com/university/faculty/49537
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号