厦大刘刚教授课题组JACS:肿瘤微环境响应超微量纳米药物发生器增强肿瘤传递和渗透
近年来,如何提高纳米药物的药物装载率并实现其有效运输、克服体内复杂的生物屏障是肿瘤治疗的难点,而肿瘤微环境响应的超小纳米药物产生体可能提供了较好的解决方案,厦门大学的刘刚教授(点击查看介绍)课题组前期基于吲哚菁绿ICG以及金属离子之间的配位发表了一系列的工作,如纳米药物的体内自组装(Adv. Mater., 2017, 29, 1605928)以及微泡内部原位形成Fe3+/ICG自组装纳米材料用于肝癌声动力治疗等(Nanoscale Horiz., 2018, DOI: 10.1039/C8NH00276B;申请专利号:201810461899.5)。近日,该课题组在J. Am. Chem. Soc.上发表文章,研究中将卟啉类光敏剂DVDMS和化疗药物阿霉素(DOX)以及三价铁离子经体外自组装,通过一锅法,迅速大规模地制备了具有超高药物装载率特点的纳米药物复合体,并发现该纳米药物复合体在肿瘤弱酸条件下,可以从起始140纳米大颗粒降解产生超小纳米药物(5-8纳米),有效增加纳米颗粒的肿瘤穿透性,促进纳米药物在肿瘤高间质压环境下的有效扩散,并获得了良好的肿瘤治疗效果。
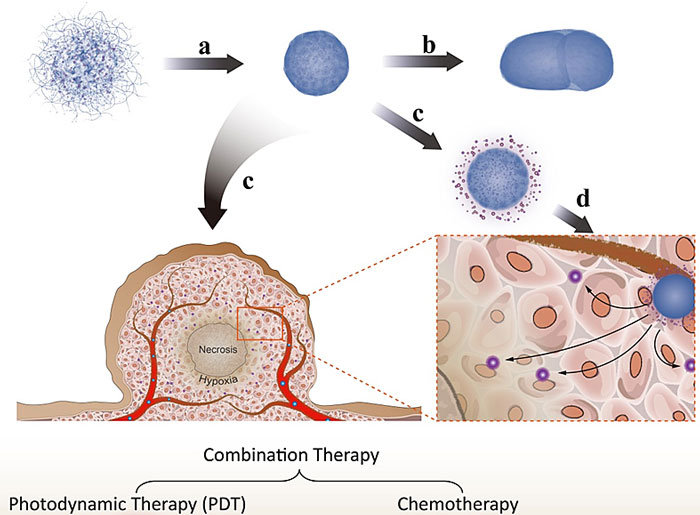
该工作也提出了相关多药物自组装的形成机制:负电荷的卟啉类光敏剂和三价铁离子(Fe3+)通过静电吸引形成长链状复合物,少量的化疗药物盐酸阿霉素(DOX-HCl)进一步与DVDMS-Fe3+长链状复合物配位,形成网格状超分子骨架中间体(SSI)。在此框架结构中,由于盐酸阿霉素氨基上的氢质子转移到光敏剂的羧酸盐,于是盐酸阿霉素由亲水性分子变成了疏水性分子阿霉素。强疏水的阿霉素通过芳香基团间的π-π堆积效应与卟啉类光敏剂的相互作用,沉积在已经形成的超分子骨架中间体(SSI)长链结构上。因此,DOX的沉积导致SSI中形成多个疏水性位点,最终随着大量阿霉素持续的装载,分布在SSI上的多个疏水位点作为强大的驱动力,促使SSI网格框架结构不断压缩形成紧密的球状纳米颗粒,从而实现DOX的高载药率与良好的水动力学稳定性。研究结果为利用多种临床药物自组装成无载体的纳米药物复合体提供了坚实的理论基础。由于该纳米药物复合体只利用药物分子和金属离子的配位构建,避免了其他无机纳米载体的使用,易于大规模生产,因此具有良好的临床转化潜力。
第一作者张鹏飞2013年加入刘刚课题组,在导师的悉心指导下进行纳米医学药物研究,上述研究工作得到科技部重大专项课题、973课题、国家自然科学基金委优秀青年基金等项目的支持。
该论文作者为:Pengfei Zhang, Junqing Wang, Hu Chen, Lei Zhao, Binbin Chen, Chengchao Chu, Heng Liu, Zainen Qin, Jingyi Liu, Yuanzhi Tan, Xiaoyuan Chen and Gang Liu
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Tumor Microenvironment-Responsive Ultrasmall Nanodrug Generators with Enhanced Tumor Delivery and Penetration
J. Am. Chem. Soc., 2018, DOI: 10.1021/jacs.8b09396
通讯作者简介
刘刚教授,博士生导师,中国生物医学工程学会青委会副主任委员、中华医学会放射学分会分子影像学组副组长。该团队主要从事药物递送系统及多功能分子影像探针的研发,自2012年入职厦门大学以来,刘刚教授以通讯或共同通讯作者身份在国际知名杂志发表SCI论文60余篇(Nature、Science子刊等影响因子高于10分的论文20余篇,PNAS等5-10分的论文30余篇),参编英文专著9部,申报中国发明专利10余项(已授权5项)并参与获得国家科技进步二等奖。
http://www.x-mol.com/university/faculty/39458
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号