JACS封面:仿生纳米载体实现蛋白的高效转运和肿瘤治疗
美国宾夕法尼亚州立大学的郑斯扬(Si-Yang Zheng)教授(点击查看介绍)课题组报道了仿生金属有机配位聚合物(MOF)纳米粒子转运功能酶和药物蛋白。该研究团队通过水相自组装将蛋白分子高效封装在MOF纳米粒子内,并进一步包裹一层同源肿瘤的外泌体膜(EV)构建仿生纳米载体,实现体内免疫逃离、肿瘤靶向和细胞内转运蛋白以抑制肿瘤生长。
作为细胞功能的执行者,蛋白质在细胞代谢、基因调控、信号传导和免疫反应等生理过程中扮演着十分重要的角色。向细胞内转运生物酶或药物蛋白质具有特异性高、毒性低、短期调控细胞功能、不改变遗传基因的优点。但是,蛋白质容易在血液中降解和变性,并很难穿透细胞膜。目前,向细胞内转运蛋白常用方法是在蛋白质修饰穿膜分子或者采用功能化的聚合物胶囊包裹转运蛋白质。然而,这些方法存在破坏蛋白活性、蛋白装载效率低或难以释放的缺点,而且在体内循环过程中纳米粒子容易被免疫系统中巨噬细胞识别清除而难以到达靶向区域。这些问题限制了蛋白质的临床应用,因此,如何安全有效地运送药物蛋白到肿瘤细胞内以实现肿瘤抑制是该领域亟待解决的难题。
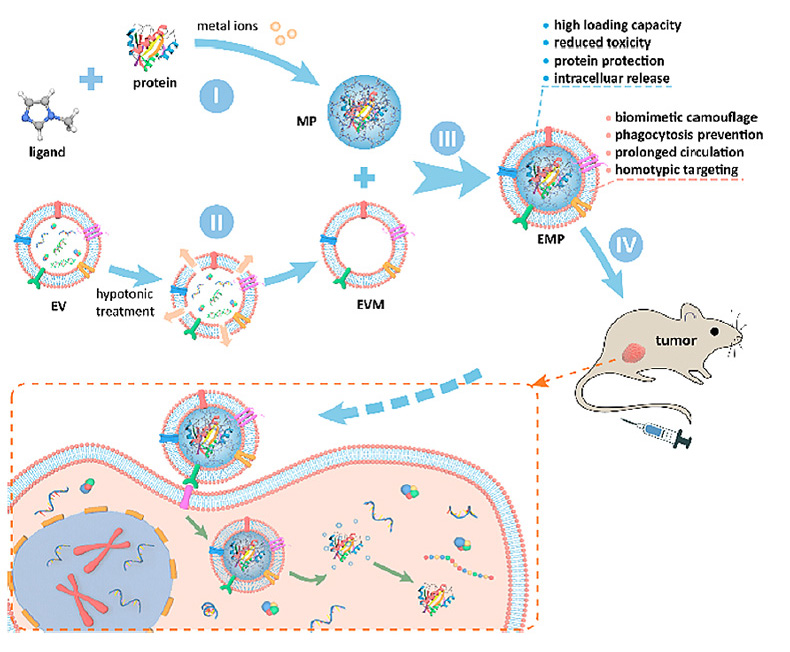
图1. 构建胞外囊泡膜包裹的EMP纳米运输器用于靶向和胞内转运蛋白质到同型细胞的示意图
金属有机框架(MOFs)材料因具有多孔性和结构多样性的特点,在生物医学领域受到广泛的关注。此外,MOFs的pH响应特性也使其成为安全优良的生物可降解性载体材料之一。天然的胞外囊泡(EV)表面含有整合素相关的跨膜蛋白CD47,可以介导“不要吃我”的信号,具有逃避吞噬的作用;同时,同一细胞来源的外泌体表面锚定分子也会增强同型细胞对其内吞的作用。基于以上构思,研究者设计了一种生物友好性的仿生纳米运送系统:选择ZIF-8纳米粒子装载治疗性蛋白质形成仿生纳米载体(MP),然后利用天然胞外囊泡膜(EVM)包裹MP纳米载体组装成EMP纳米运输器。不同于传统的脂质体载药模型,包裹胞外囊泡膜这一策略不仅能够有效地保护蛋白质免受血液中蛋白酶的降解和吞噬细胞的吞噬作用,而且可以协助穿透细胞膜障碍。乳腺癌来源的胞外囊泡膜可以辅助靶向乳腺肿瘤细胞,促进其对EMP运输器的内吞作用。当EMP纳米运输器被细胞内吞后,pH敏感的金属与有机配体共价键断裂。随着有机配体的逐步质子化微环境pH升高,溶酶体膜通透性增强,从而完成目标蛋白质释放到内体或者溶酶体中,进而实现系统有效地运送蛋白质到靶器官治疗肿瘤的作用。
这一成果以封面论文的形式发表在Journal of the American Chemical Society 上,论文的第一作者为程功博士,通讯作者为郑斯扬教授。
该论文作者为:Gong Cheng, Wenqing Li, Laura Ha, Xiaohui Han, Sijie Hao, Yuan Wan, Zhigang Wang, Fengping Dong, Xin Zou, Yingwei Mao and Si-Yang Zheng
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Self-Assembly of Extracellular Vesicle-like Metal–Organic Framework Nanoparticles for Protection and Intracellular Delivery of Biofunctional Proteins
J. Am. Chem. Soc., 2018, 140, 7282, DOI: 10.1021/jacs.8b03584
导师介绍
郑斯扬
http://www.x-mol.com/university/faculty/49892
课题组链接
https://www.bme.psu.edu/labs/zheng-lab/
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号