精确自组装纳米标记实现循环肿瘤靶标的高灵敏液体活检
近日,上海交通大学医学院分子医学研究院及仁济医院左小磊(点击查看介绍)团队在高灵敏液体活检方面取得重要进展,利用框架核酸(Framework Nucleic Acid,FNA)设计并构建了一种精确自组装纳米标记来定量放大微弱生物信号,实现了对循环肿瘤靶标的高灵敏检测。相关研究结果发表在Angew. Chem. Int. Ed.上。
通常,医生通过手术活检或穿刺活检对癌症病情做出判断。但随着对肿瘤研究的不断深入,传统活检技术在癌症的诊断和治疗过程中的局限性逐渐凸显。例如:局部的肿瘤组织并不能反应肿瘤的总体情况;不能实现病情实时监测;手术扰动加速转移风险等。循环肿瘤靶标是由肿瘤细胞释放到循环血液中的癌症标志物,携带与原发肿瘤组织高度一致的生物信息。因此,针对循环肿瘤靶标的液体活检成为目前最具发展潜力的早期诊断和实时监测手段,成为肿瘤精准治疗领域的新兴力量,相比于传统活检方法具有简便、无创、实时、信息全面等优点。然而,循环肿瘤靶标含量极低、所处血液环境复杂,必须依赖信号放大才能实现检测。
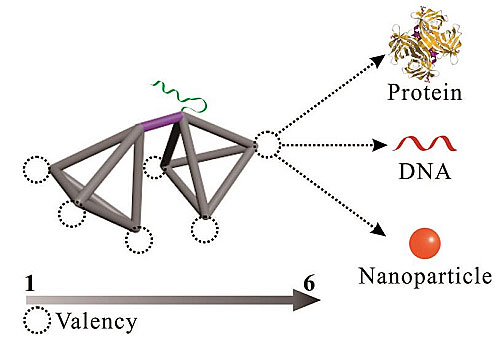
现有的信号放大探针往往存在均一性差的问题,难以实现微弱信号的定量放大,造成循环肿瘤靶标检测偏差大。因而,设计高度均一的精确纳米标记在提高液体活检的精准度方面尤为重要。针对这一挑战性问题,分子医学研究院左小磊研究员与中国科学院上海应用物理研究所樊春海研究员(点击查看介绍)合作,利用框架核酸结构的精确、可编程特点,构建了系列模块化的精确自组装纳米标记。通过引入核酸、酶、纳米颗粒等信号探针,他们实现了对生物信号放大的精确调控,提升了循环肿瘤靶标检测的灵敏度与准确性。这一研究为循环肿瘤靶标的高灵敏液体活检提供了新手段。
左小磊研究员团队在肿瘤液体活检方面进行了系统的研究,利用DNA纳米技术构建了高灵敏、多水平靶标液体活检平台(相关论文包括Angew. Chem. Int. Ed., 2017, 56, 16077; Nano Lett., 2017, 17, 5193; Nat. Protoc., 2016, 11, 1244; Adv. Mater., 2016, 28, 6860; Angew. Chem. Int. Ed., 2015, 54, 2151 等)。
该论文作者为:Qi Liu, Zhilei Ge, Xiuhai Mao, Guobao Zhou, Xiaolei Zuo, Juwen Shen, Jiye Shi, Jiang Li, Lihua Wang, Xiaoqing Chen, Chunhai Fan
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Valency‐Controlled Framework Nucleic Acid Signal Amplifiers
Angew. Chem. Int. Ed., 2018, DOI: 10.1002/anie.201802701
导师介绍
左小磊
http://www.x-mol.com/university/faculty/49555
樊春海
http://www.x-mol.com/university/faculty/39472
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号