氢键调控界面蛋白质的振动能量转移速率与途径
蛋白质分子能量转移对生化反应及生理功能的正常运作至关重要,许多重要的生理和细胞过程都依赖于蛋白质的超快能量转移过程,例如,构象变化传输和变构通讯与沿蛋白质骨架上的能量传输直接相关。快速且有效的能量转移是蛋白质维持在很窄温度范围内正常工作的重要保证。因而,理解生物膜界面蛋白质的能量转移过程是揭示膜蛋白质工作机制的关键。但是,迄今为止人们对蛋白质(特别是界面蛋白质)能量转移的了解十分有限。这主要是因为能量传递过程往往牵涉皮秒或更短时间尺度内的激发态动力学,而目前在理论和实验上对激发态动力学,尤其是界面激发态动力学的精确描述还缺乏行之有效的方法和数据积累。
针对这一难题,中国科学技术大学罗毅教授(点击查看介绍)研究团队叶树集研究员(点击查看介绍)小组最近独立搭建了振动态选择激发和频光谱探测的飞秒时间分辨测量系统。该系统技术指标达到当前国际最先进水平:时间分辨度100 fs,光谱分辨度≤5 cm-1,实现目前文献报导中最快的和频光谱采谱速度(最快18毫秒采集一光谱)。该系统的发展为深入研究界面超快构象变化和界面能量转移等动力学行为提供了重要工具。利用具有特定能量的飞秒红外脉冲选择激发生物膜上蛋白质的N-H基团,然后用飞秒和频光谱监控N-H基团的瞬态结构变化,首次成功测出水环境下生物膜上蛋白质N-H的振动能量驰豫速率(图1)。α-螺旋和β折叠结构中的NH驰豫时间分别是1.7和0.9皮秒。
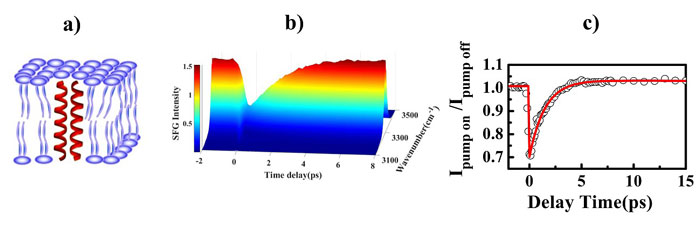
图1、a) 膜蛋白结构示意图;b) NH基团激发后,其瞬态和频光谱演化图;c) NH基团振动动力学特性图。
通过激发N-H基团,探测酰胺键C=O瞬态结构变化,该小组发现N-H到C=O的振动能量传递存在两种途径:一种是直接的NH-CO耦合作用(σNH-CO);另一种是N-H先驰豫到某中间态(记为X态),然后X态与C=O发生耦合作用(σX-CO)(图2)。系统研究表明C=O…N-H的氢键强弱决定N-H与C=O间两种耦合途径(σX-CO/σNH-CO)的比例。氢键越强,σX-CO 耦合的比例越高,成功揭示了氢键作用影响膜蛋白能量传递途径和速率的规律。
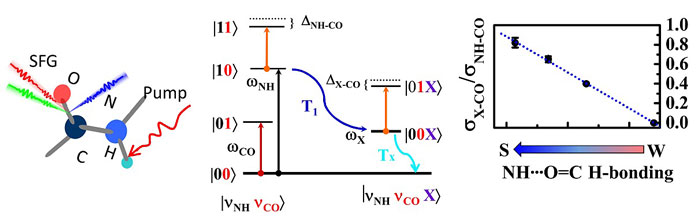
图2、N-H与C=O的耦合作用及N-H与C=O之间氢键强弱对耦合作用的影响。
研究成果发表在《德国应用化学》上,论文第一作者为谈军军博士。
该论文作者为:Junjun Tan, Baixiong Zhang, Yi Luo, Shuji Ye*
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Ultrafast Vibrational Dynamics of Membrane-Bound Peptides at the Lipid Bilayer/Water Interface
Angew. Chem. Int. Ed., 2017, 56, 12977-12981. DOI: 10.1002/anie.201706996
研究团队简介
针对缺乏表征界面复杂分子结构与动力学有效技术这一现状,叶树集小组一直致力于发展和完善具有时间、空间和能量分辨的高灵敏、免标记、快速识别的超快非线性光谱新技术,系统研究复杂体系的界面物理与化学问题,实现从模型体系到真实体系电子态和振动态的超快谱学精确测量。该小组从构建谱学模型开始,到发展谱学指纹区分辨技术到飞秒时间分辨技术,目前已形成了一套表征界面复杂分子结构、相互作用以及动力学的相对完整方法。近5年来,在J. Am. Chem. Soc., Angew. Chem. Int. Ed., Science Advances和J. Phys. Chem. Lett. 等著名期刊上发表系列高水平研究成果,成果“生物界面非线性光谱分析新方法的发展与应用”获2014年中国分析测试协会科学技术奖二等奖。因在化学动力学研究中的杰出表现,叶树集研究员荣获2017年度的“中国化学会张存浩化学动力学青年科学家奖”。
叶树集
http://www.x-mol.com/university/faculty/14863
罗毅
http://www.x-mol.com/university/faculty/14830
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号