目标物驱动诱导的催化发夹自组装和DNAzyme循环构建无酶、信号放大电化学传感器用于ATP检测
传统酶辅助的信号放大方法虽然能提高传感器灵敏度,但酶不稳定,易受环境温度、pH等影响,且价格昂贵,构建简单、灵敏且无酶传感器十分有必要。近日,西南大学电分析团队袁若教授(点击查看介绍)、袁亚利副教授(点击查看介绍)课题组基于目标物驱动的催化发夹自组装(CHA)和DNAzymes循环放大技术,构建了一种无酶、双重信号放大的电化学生物传感器高灵敏检测腺苷三磷酸(ATP)。
两条DNA同时与目标物ATP形成复合物,诱导CHA循环反应转化成大量的酶链(HP1-HP2),有效提高了ATP转化效率。接着,所形成的HP1-HP2与聚苯乙烯磁性微球上的底物链HP3杂交形成DNAzymes,在相应金属离子存在下催化剪切底物链,获得输出DNA片段S1,并释放酶链引发下一个剪切循环,进一步增加了ATP转换为S1的转化效率,提高了DNA放大效率。基于双循环放大,一个ATP可以产生多个S1,为ATP的检测提供了一种灵敏的方法。实验结果表明,该传感器的线性范围为0.001 nmol•L-1-50 nmol•L-1,检测限为0.45 pmol•L-1。电化学传感器检测ATP的原理如图1所示。
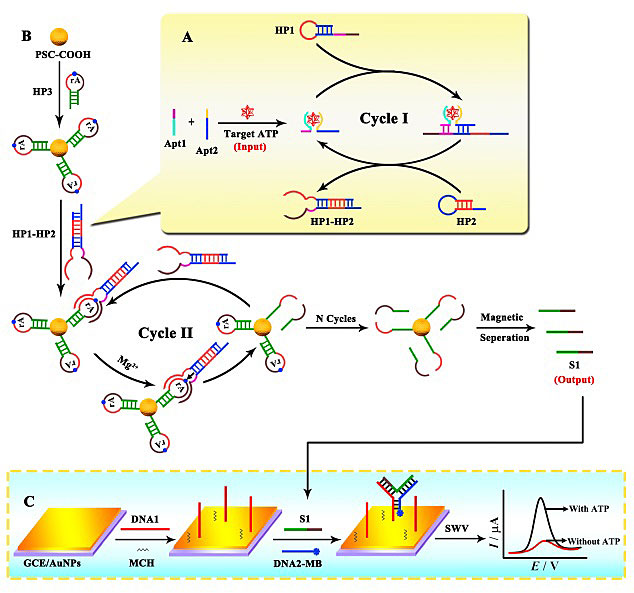
图1. 基于目标物驱动的催化发夹自组装和Mg2+-DNAzymes循环放大构建的电化学传感器用于检测ATP的原理示意图。
这种放大方法无需使用任何蛋白酶,为构建简单、无酶的电化学传感器检测小分子、DNA、蛋白质、重金属离子提供了一种新思路。这一研究结果发表在Chemical Communications 上。
该论文作者为:HuaXie, Ya-Qin Chai, Ya-Li Yuan, Ruo Yuan
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Highly effective molecule converting strategy based on enzyme-free dual recycling amplification for ultrasensitive electrochemical detection of ATP
Chem. Commun., 2017, 53, 8368-8371, DOI: 10.1039/C7CC03497K
导师介绍
袁若
http://www.x-mol.com/university/faculty/13979
袁亚利
http://www.x-mol.com/university/faculty/46721
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号