新加坡国立大学刘斌课题组Chem:基于自发光的AIE纳米工具,特异性示踪并杀伤肿瘤
肿瘤的体内特异性诊断以及精准治疗一直是生物医学、材料学以及临床医学等多个领域研究的热点。其中,光学成像近年来逐渐成为肿瘤示踪诊断中重要的研究工具。传统的荧光探针由于其自身穿透能力的限制,很难应用到活体深度肿瘤的示踪研究中。化学发光是一种在室温下将化学能转化为光能的化学现象,其反应体系多以草酸酯、过氧化氢(H2O2)以及荧光染料为主要组成部分,自发光波长通常由所采用的荧光染料的性质所决定。由于可以受H2O2激发产生自发荧光,这种发光体系逐渐引起疾病诊断领域的研究人员的极大关注。受此启发,新加坡国立大学(NUS)刘斌教授(点击查看介绍)课题组的研究人员开发了一种新颖的基于聚集诱导发光(AIE)光敏剂的化学发光纳米材料,并首次实现了动物体内肿瘤的自发光成像和药物协同治疗。相关研究发表于Chem 杂志,刘斌教授课题组的博士后研究员毛铎与武文博为论文的共同第一作者。

刘斌教授。图片来源:NUS
研究人员发现,与光辐射相似,光敏剂受到化学能激发同样可以产生单线态氧(1O2),杀伤肿瘤细胞。因此,通过合理的分子结构设计,研究人员合成了一种具有AIE性质的化学发光纳米粒子(C-TBD)。该纳米粒子由AIE光敏剂(TBD)、化学染料分子(CPPO)、F127聚合物以及豆油四部分组成(图1a),不但可以克服之前自发光纳米粒子中荧光染料聚集淬灭的缺点,同时经过化学能(H2O2)激发可以有效产生单线态氧以及近红外自发荧光(图1b/c)。
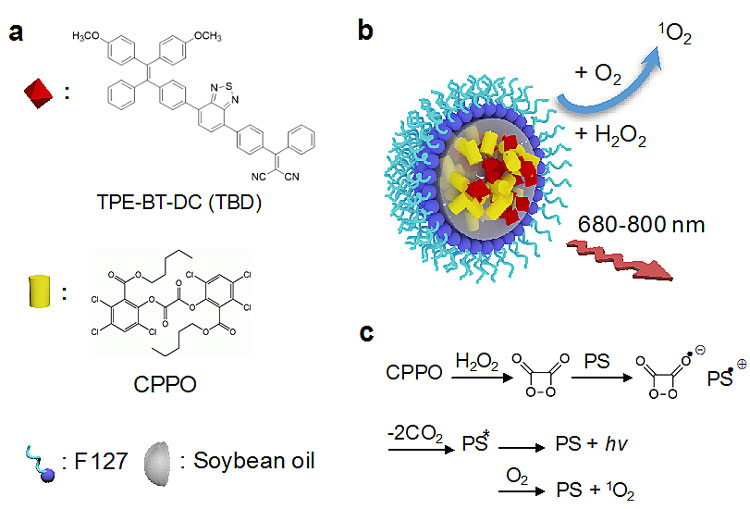
图1. 光敏剂化学结构、C-TBD纳米粒子结构以及化学发光产生单线态氧原理。图片来源:Chem
C-TBD纳米粒子可通过EPR效应富集在肿瘤组织中,而肿瘤微环境中H2O2水平较高,这样纳米粒子即可被特异性激活。为了验证这些想法,研究人员通过尾静脉注射将这种纳米粒子注入实验动物体内。实验结果表明C-TBD纳米粒子自发光成像打破了传统荧光肿瘤成像的组织深度的限制,精确的将腹腔转移微小肿瘤通过活体成像显影出来(图2)。
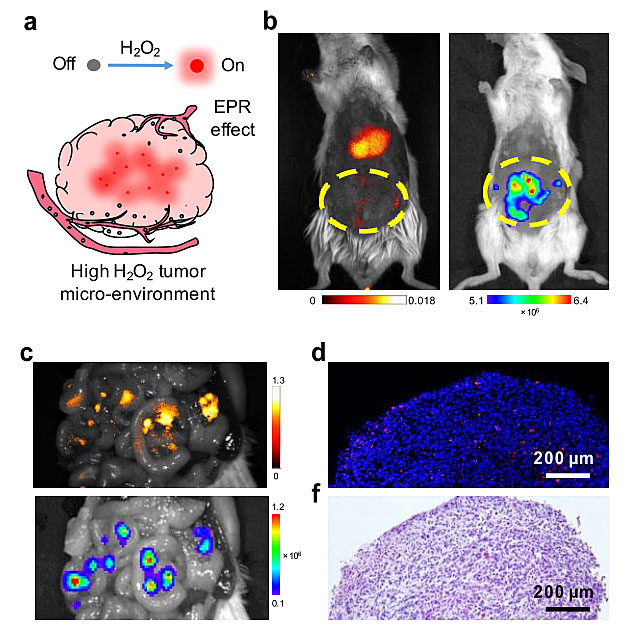
图2. C-TBD纳米粒子对腹腔转移肿瘤的自发光特异性成像。图片来源:Chem
同时研究人员筛选出了一种治疗肿瘤的临床用药FEITC,可以在不影响正常组织功能的情况下提高肿瘤微环境的H2O2浓度。FEITC与C-TBD纳米粒子联合使用,肿瘤的自发光信号的强度以及信噪比被进一步提高。与此同时,经过联合治疗过程,研究人员也观察到了明显的肿瘤体积缩小、肿瘤细胞凋亡等现象(图3)。
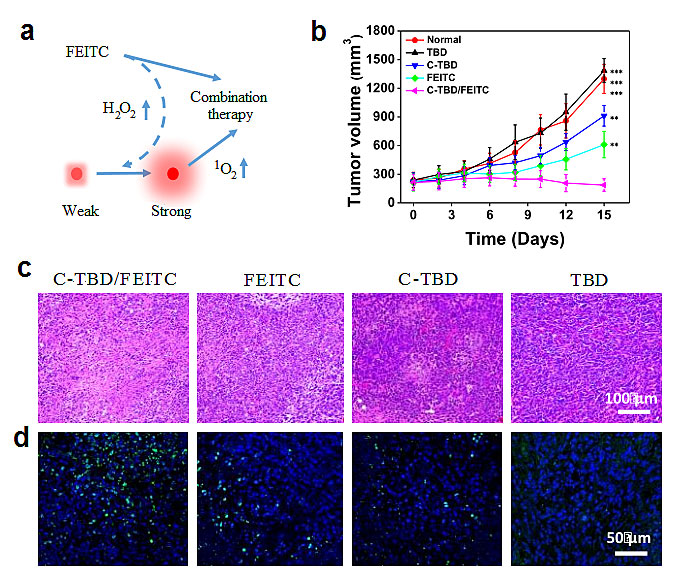
图3. C-TBD纳米粒子与抗癌药物FEITC联合诱导肿瘤细胞凋亡抑制肿瘤生长。图片来源:Chem
进一步的细胞数据揭示C-TBD纳米粒子受到FEITC作用产生大量的单线态氧,引起了细胞膜的脂质体氧化并同时打开了细胞内的凋亡途径。由于现今临床治疗肿瘤的手段如各种放疗化疗,普遍能引起肿瘤组织氧化水平的提升,这些肿瘤杀伤的证据可以充分证明C-TBD纳米粒子在增强传统临床抗肿瘤疗法方面具有巨大的应用潜力。
可以预见,这种基于AIE的自发光纳米材料可以为今后临床上的肿瘤精确定位、抗肿瘤治疗提供强大而有效的工具。也为疾病诊断示踪材料的设计提供新颖的思路。
该工作在完成过程中得到南开大学生命科学学院、药物化学生物学国家重点实验室、生物活性材料教育部重点实验室的大力支持。
该论文作者为:Duo Mao, Wenbo Wu, Shenglu Ji, Chao Chen, Fang Hu, Deling Kong, Dan Ding, Bin Liu
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Chemiluminescence-Guided Cancer Therapy Using a Chemiexcited Photosensitizer
Chem, 2017, DOI: 10.1016/j.chempr.2017.10.002
导师介绍
刘斌
http://www.x-mol.com/university/faculty/40437
(本稿件来自Chem)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号