胰岛素及相关神经肽的天然糖基化开拓糖尿病和神经肽研究的新方向
糖尿病作为一种慢性的代谢疾病是21世纪全球面临的最严重、最危急的健康问题之一。糖尿病患病人数逐年递增,并产生影响终生的并发症。目前,全球约4.15亿成年人患有糖尿病。2015年,大概有500万人死于糖尿病及其引起的并发症,相当于每6秒钟就会有1人死亡。作为一种因机体胰岛素分泌不足或利用缺陷而导致的慢性疾病,胰岛素就成为糖尿病研究和治疗的关键分子,多种人工合成或修饰的胰岛素及其类似物已广泛用于糖尿病的研究和治疗。胰岛素是一种神经肽类激素,然而相比于广泛存在的各种氨基酸残基的翻译后修饰,人们对天然发生的胰岛素翻译后修饰的认识长期停留在仅有的二硫键上。近日,美国威斯康星大学的李灵军教授(点击查看介绍)团队通过新一代的质谱技术对老鼠和人类胰岛素的靶向性进行研究,发现胰岛素还有多种多肽神经肽的天然O-糖基化位点以及位点上存在的多种糖型。这是第一次在哺乳类动物体内发现的可天然糖基化的神经肽,也是首次应用质谱手段进行高通量糖基化神经肽激素的发现性研究。此发现为未来的糖尿病及相关研究,同时也为神经肽组研究指明了新的方向。
近年来,随着科学技术的迅猛发展,高分辨质谱已经成为高通量蛋白质组鉴定最有效的方法之一。其高灵敏度和有效的二级谱碎裂方法已广泛应用于精确测定含量极低的多种翻译后修饰,如磷酸化、乙酰化等。然而,糖基化作为另一个广泛存在且能对蛋白质结构、功能起到关键影响的翻译后修饰,其研究却受制于没有合适的分析方法。在产生二级谱鉴别时,传统的碰撞诱导解离技术只能碎裂糖基侧链,而电子转移解离的方法只能裂解肽键,且受困于过低的反应效率。另外,区别于磷酸化等简单修饰,糖基化可由多种单糖成分组成,例如葡萄糖、乳糖、甘露糖等。加上各种排列组合可能性所带来的异质性和复杂性,单纯利用某一种二级谱碎裂技术显然不能完全解答成千上万种可能的糖侧链和氨基酸序列组合。传统的糖蛋白组学多用酶将糖侧链移除并收集,从而进行多肽链和糖链的分别测序,虽然方法成熟,但将糖和其多肽链母体的分离则使进一步对某个糖基位点上糖型多样性的研究变得更加困难。李灵军团队开发出一种结合高能碰撞诱导解离和电子转移解离优势的复合解离方法——电子转移高能碰撞解离,可在不分离糖和多肽母体的情况下同时鉴别两个部分的序列,有望实现大范围高通量地鉴定多肽氨基酸序列和糖侧链序列。
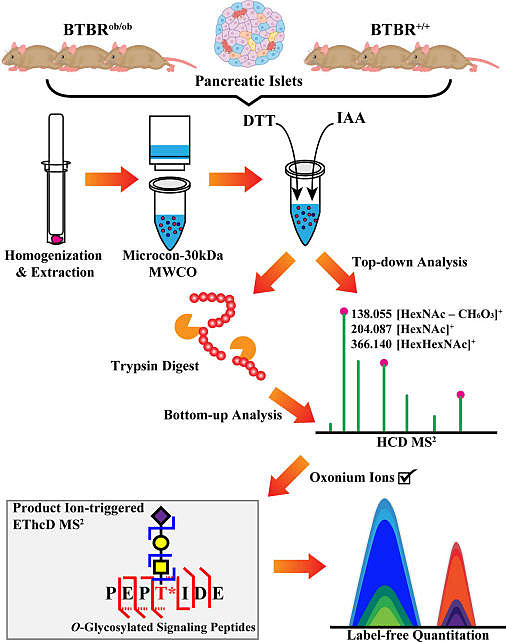
成功地应用此技术进行高通量蛋白质组的修饰研究之后,威斯康星大学的研究团队进一步完善该技术,并将其应用于更具有挑战性的神经肽组的研究。传统的鸟枪法蛋白组学以胰蛋白酶酶解产生长度较为均一的多肽段(平均为14个氨基酸)为研究对象,较方便地设定质谱参数。而神经肽长度分布范围极广,可为3–100个氨基酸,加上可长可短的糖链,对质谱功能和参数设定提出了更高要求。为提高二级谱的谱图质量和精确测序,该团队综合应用鸟枪法和自上而下(top-down)的方法分别分析酶解的神经肽片段和完整的神经肽,最后分析得出完整的神经肽链和修饰序列。神经肽的另一个特点是生物体内含量极低,糖基化修饰的部分含量更低。为避免过多的仪器时间不必要地浪费在非修饰的神经肽上,该团队巧妙地利用糖基化多肽能够产生特有的氧鎓离子,使仪器先进行快速的高能碰撞解离,并根据氧鎓离子的存在与否实时判断当前分子是否包含糖基化,仅对可能存在糖基修饰的目标离子进行进一步的电子转移高能碰撞解离,大大加速了仪器的运转,并提高针对糖基化神经肽分析鉴定的灵敏度和准确度。
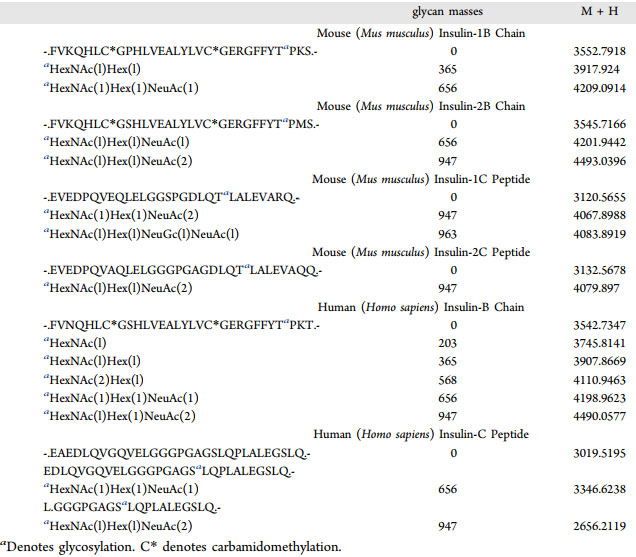
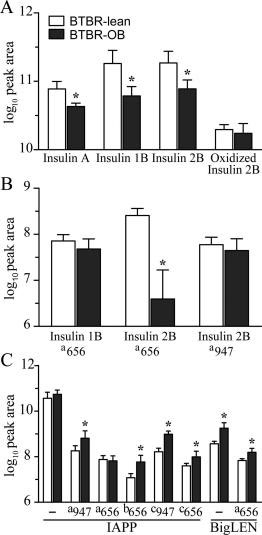
在对小鼠和人的胰岛分析中,该团队发现多种不同糖型跨物种保守性地修饰胰岛素B链碳端的苏氨酸残基。同时,在小鼠胰岛素C链中,他们糖基化修饰了靠近碳端的苏氨酸,而在人胰岛素C链中相似位点,苏氨酸被丝氨酸取代,并成为糖基化位点,进一步说明该修饰的跨物种保守性。发现的糖基化神经肽还包括胰岛淀粉样多肽、BigLEN等,其中多数都与胰岛素的合成和分泌相关,说明糖基化可能高度参与胰岛素及相关神经肽的功能调节。

在定性分析证明了糖基化可广泛存在于神经肽中后,初步的定量分析检验了健康小鼠和患有二型糖尿病的小鼠体内各神经肽的含量变化。相比于健康小鼠,未修饰的胰岛素在二型糖尿病小鼠体内明显减少,类似的降低趋势也体现在糖基化修饰的胰岛素上。反之,胰岛淀粉样多肽和BigLEN则在糖尿病小鼠中呈现上升趋势。
该质谱技术使完整测序糖基化神经肽变得简单可行,也首次证明了糖基化广泛存在于神经肽组中,为今后大范围鉴定糖基化神经肽及其深度功能性的研究奠定了基础。由于糖基化往往能显著影响多肽链的稳定性和生物活性,糖基化胰岛素及相关多肽的首次发现为糖尿病的研究和治疗提供了一个全新的角度。
这一成果近期发表在Analytical Chemistry 上,文章的第一作者是威斯康星大学麦迪逊分校的博士生余庆(现于哈佛大学医学院从事博士后研究),通讯作者为李灵军教授。
该论文作者为:Qing Yu, Alejandra Canales, Matthew S. Glover, Rahul Das, Xudong Shi, Yang Liu, Mark P. Keller, Alan D. Attie and Lingjun Li
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Targeted Mass Spectrometry Approach Enabled Discovery of O-Glycosylated Insulin and Related Signaling Peptides in Mouse and Human Pancreatic Islets
Anal. Chem., 2017, 89, 9184, DOI: 10.1021/acs.analchem.7b01926
李灵军教授简介

李灵军,2000年于美国伊利诺伊大学香槟分校获得化学博士学位,之后在美国太平洋西北国家实验室和布兰迪斯大学进行博士后研究,2002年起到美国威斯康星大学麦迪逊分校任教,现任威斯康星大学麦迪逊分校药学院和化学系双聘教授,获威斯康星大学Janis Apinis药物科学与化学教授和Vilas杰出成就教授称号。
李灵军教授致力于生物分析科学以及质谱相关技术的研究,主要涉及的领域有神经肽组学、蛋白质组学、代谢组学等,并应用这些尖端的分析方法和技术去解决神经生物学、基础和临床医学中的关键性问题。
李灵军课题组(已经毕业36位博士生,现有22位在读博士生,三位博士后)在生物分析化学领域的贡献主要为构建基于高灵敏度质谱的多维分析平台,并将此平台应用于新型神经肽组学的研究,在高水平杂志上发表论文200多篇,受邀学术报告180余场。李教授先后承担30多项科研项目,获得研究经费超过两千万美元。
李教授先后被授予分析化学个人成就奖(匹兹堡会议)、美国国家科学基金委生涯奖、美国质谱学会研究奖、斯隆基金会研究奖以及2014年Biemann Medal;2016年入选全球50位最有影响力的女分析化学家。李教授还获得中国教育部“长江学者奖励计划”讲座教授称号,先后担任美国质谱学会教育委员会成员、Asilomar会议委员、US HUPO 董事会成员、美国国家卫生研究院(NIH)基金评审委员会成员、美国国家自然科学(NSF)基金委员会、美国国家能源部(DOE)基金会、美国国家能源部环境分子科学实验室评审团成员、荷兰科学研究基金评审、马普合作基金评审,英国皇家化学学会Analytical Methods 副主编、JASMS 副主编、Analyst 咨询委员会成员及美国华人质谱学会会长,并先后为60多个学术期刊担任评审。
http://www.x-mol.com/university/faculty/80

本文第一作者余庆博士(右)与李灵军教授在ASMS(美国质谱年会)会议上的合影

李灵军教授及其在美国威斯康星大学的研究团队
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号