Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Mussel-inspired electroactive chitosan/graphene oxide composite hydrogel with rapid self-healing and recovery behavior for tissue engineering
Carbon ( IF 10.5 ) Pub Date : 2017-12-01 , DOI: 10.1016/j.carbon.2017.09.071 Xin Jing , Hao-Yang Mi , Brett N. Napiwocki , Xiang-Fang Peng , Lih-Sheng Turng
Carbon ( IF 10.5 ) Pub Date : 2017-12-01 , DOI: 10.1016/j.carbon.2017.09.071 Xin Jing , Hao-Yang Mi , Brett N. Napiwocki , Xiang-Fang Peng , Lih-Sheng Turng
|
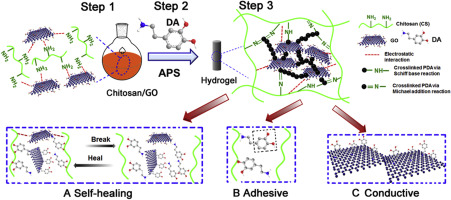
Abstract Hydrogels currently used in electroactive tissues (cardiac tissues, skeletal muscles, and nerves) have certain shortcomings such as a lack of electrical conductivity and adhesiveness, both of which play a key role in the success of hydrogels in biomedical applications. In this study, chitosan (CS)/graphene oxide (GO) composite hydrogels with self-adhesive and self-healing properties, as well as electrical conductivity, were prepared by the incorporation of the mussel-inspired protein polydopamine (PDA). During the oxidizing process of dopamine (DA), graphene oxide was reduced by PDA and dispersed into the hydrogel network to form electric pathways. The covalent bonds, supramolecular interactions, hydrogen bonding, and π-π stacking gave the CS/GO composite hydrogels high stability, strong mechanical behaviors, good adhesiveness, self-healing properties, and a fast recovery ability. The electrical conductivity of the CS/GO reached 1.22 mS/cm and the adhesive strength of the composite hydrogel increased by 300% compared to CS-DA hydrogels. Cell culture results demonstrated that the conductive CS/GO hydrogels enhanced the cell viability and proliferation of human embryonic stem cell-derived fibroblasts (HEF1) and cardiomyocytes (CMs) compared to CS-DA hydrogels. Moreover, CMs showed a faster spontaneous beating rate than those in the control groups. Our work demonstrates a simple approach to fabricating polydopamine-based, adhesive, conductive, self-healing, and fast-recovering hydrogels that have great potential in electroactive tissue engineering applications.
中文翻译:

具有快速自愈和恢复行为的贻贝电活性壳聚糖/氧化石墨烯复合水凝胶用于组织工程
摘要 目前用于电活性组织(心脏组织、骨骼肌和神经)的水凝胶存在一定的缺点,如缺乏导电性和粘附性,这两者对水凝胶在生物医学应用中的成功起着关键作用。在这项研究中,通过掺入受贻贝启发的蛋白质聚多巴胺 (PDA) 制备了具有自粘和自愈合性能以及导电性的壳聚糖 (CS)/氧化石墨烯 (GO) 复合水凝胶。在多巴胺(DA)的氧化过程中,氧化石墨烯被 PDA 还原并分散到水凝胶网络中形成电通路。共价键、超分子相互作用、氢键和 π-π 堆积使 CS/GO 复合水凝胶具有高稳定性、强机械性能、良好的粘附性、自愈特性和快速恢复能力。CS/GO 的电导率达到 1.22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。
更新日期:2017-12-01
中文翻译:

具有快速自愈和恢复行为的贻贝电活性壳聚糖/氧化石墨烯复合水凝胶用于组织工程
摘要 目前用于电活性组织(心脏组织、骨骼肌和神经)的水凝胶存在一定的缺点,如缺乏导电性和粘附性,这两者对水凝胶在生物医学应用中的成功起着关键作用。在这项研究中,通过掺入受贻贝启发的蛋白质聚多巴胺 (PDA) 制备了具有自粘和自愈合性能以及导电性的壳聚糖 (CS)/氧化石墨烯 (GO) 复合水凝胶。在多巴胺(DA)的氧化过程中,氧化石墨烯被 PDA 还原并分散到水凝胶网络中形成电通路。共价键、超分子相互作用、氢键和 π-π 堆积使 CS/GO 复合水凝胶具有高稳定性、强机械性能、良好的粘附性、自愈特性和快速恢复能力。CS/GO 的电导率达到 1.22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。22 mS/cm,与 CS-DA 水凝胶相比,复合水凝胶的粘合强度提高了 300%。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。细胞培养结果表明,与 CS-DA 水凝胶相比,导电 CS/GO 水凝胶增强了人胚胎干细胞衍生的成纤维细胞 (HEF1) 和心肌细胞 (CM) 的细胞活力和增殖。此外,CMs 显示出比对照组更快的自发搏动率。我们的工作展示了一种简单的方法来制造基于聚多巴胺的、粘性的、导电的、自修复的和快速恢复的水凝胶,这些水凝胶在电活性组织工程应用中具有巨大的潜力。










































 京公网安备 11010802027423号
京公网安备 11010802027423号