当前位置:
X-MOL 学术
›
ACS Chem. Biol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Multidimensional Control of Cas9 by Evolved RNA Polymerase-Based Biosensors
ACS Chemical Biology ( IF 3.5 ) Pub Date : 2017-08-22 00:00:00 , DOI: 10.1021/acschembio.7b00532 Jinyue Pu 1 , Kaitlin Kentala 1 , Bryan C. Dickinson 1
ACS Chemical Biology ( IF 3.5 ) Pub Date : 2017-08-22 00:00:00 , DOI: 10.1021/acschembio.7b00532 Jinyue Pu 1 , Kaitlin Kentala 1 , Bryan C. Dickinson 1
Affiliation
|
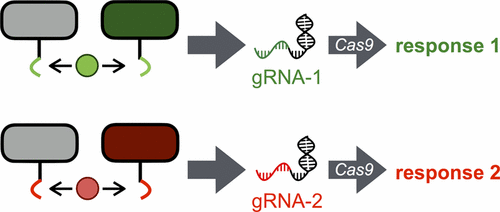
Systems to control Cas9 with spatial and temporal precision offer opportunities to decrease side effects, protect sensitive tissues, and create gene therapies that are only activated at defined times and places. Here, we present the design of new Cas9 controllers based on RNA polymerase (RNAP)-based biosensors that produce gRNAs, thereby regulating target knockout. After development and validation of a new abscisic acid-inducible biosensor to control Cas9, we lowered the background of the system using continuous evolution. To showcase the versatility of the approach, we designed biosensors that measure medically relevant protein–protein interactions to drive knockout. Finally, to test whether orthogonal RNAP biosensors could integrate multiple input signals to drive multiple gRNA-based outputs with a single Cas9 protein, we designed an “on-switch/off switch” controller. The addition of one input activates the “on switch” and induces knockout, while the addition of a second input activates the “off switch” and produces a gRNA that directs the Cas9 protein to degrade the “on switch” gRNA vector, thereby deactivating it. This combined activation and deactivation system displayed very low background and inducible target knockout using different combinations of small-molecule treatment. Our results establish engineered RNAP biosensors as deployable Cas9 control elements and open up new opportunities for driving genetic editing technologies by diverse input signals.
中文翻译:

基于进化的基于RNA聚合酶的生物传感器的Cas9多维控制。
以空间和时间精度控制Cas9的系统提供了减少副作用,保护敏感组织以及创建仅在定义的时间和位置激活的基因疗法的机会。在这里,我们提出了新的Cas9控制器的设计,该控制器基于产生gRNA的RNA聚合酶(RNAP)为基础的生物传感器,从而调节靶标敲除。在开发并验证了一种新的可诱导脱落酸诱导的生物传感器以控制Cas9之后,我们使用了连续进化降低了系统的背景。为了展示该方法的多功能性,我们设计了生物传感器来测量医学上相关的蛋白质之间的相互作用,以驱动基因敲除。最后,要测试正交RNAP生物传感器是否可以整合多个输入信号以使用单个Cas9蛋白驱动多个基于gRNA的输出,我们设计了一个“开/关开关”控制器。一个输入的添加激活“开关”并诱导敲除,而第二个输入的添加激活“关开关”并产生指导Cas9蛋白降解“开关” gRNA载体的gRNA,从而使其失活。 。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。同时添加第二个输入会激活“关闭开关”并产生一个gRNA,该gRNA指导Cas9蛋白降解“打开” gRNA载体,从而使其失活。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。同时添加第二个输入会激活“关闭开关”并产生一个gRNA,该gRNA指导Cas9蛋白降解“打开” gRNA载体,从而使其失活。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。
更新日期:2017-08-22
中文翻译:

基于进化的基于RNA聚合酶的生物传感器的Cas9多维控制。
以空间和时间精度控制Cas9的系统提供了减少副作用,保护敏感组织以及创建仅在定义的时间和位置激活的基因疗法的机会。在这里,我们提出了新的Cas9控制器的设计,该控制器基于产生gRNA的RNA聚合酶(RNAP)为基础的生物传感器,从而调节靶标敲除。在开发并验证了一种新的可诱导脱落酸诱导的生物传感器以控制Cas9之后,我们使用了连续进化降低了系统的背景。为了展示该方法的多功能性,我们设计了生物传感器来测量医学上相关的蛋白质之间的相互作用,以驱动基因敲除。最后,要测试正交RNAP生物传感器是否可以整合多个输入信号以使用单个Cas9蛋白驱动多个基于gRNA的输出,我们设计了一个“开/关开关”控制器。一个输入的添加激活“开关”并诱导敲除,而第二个输入的添加激活“关开关”并产生指导Cas9蛋白降解“开关” gRNA载体的gRNA,从而使其失活。 。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。同时添加第二个输入会激活“关闭开关”并产生一个gRNA,该gRNA指导Cas9蛋白降解“打开” gRNA载体,从而使其失活。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。同时添加第二个输入会激活“关闭开关”并产生一个gRNA,该gRNA指导Cas9蛋白降解“打开” gRNA载体,从而使其失活。使用小分子处理的不同组合,此组合的激活和失活系统显示出非常低的背景和可诱导的靶基因敲除。我们的结果建立了可工程化的RNAP生物传感器作为可部署的Cas9控制元件,并为通过各种输入信号驱动基因编辑技术开辟了新机遇。











































 京公网安备 11010802027423号
京公网安备 11010802027423号