当前位置:
X-MOL 学术
›
Eur. J. Pharm. Biopharm.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
Is rat a good model for assessment of particulate-based taste-masked formulations?
European Journal of Pharmaceutics and Biopharmaceutics ( IF 4.9 ) Pub Date : 2019-11-11 , DOI: 10.1016/j.ejpb.2019.11.001 Joseph Ali 1 , Manting Chiang 2 , Jong Bong Lee 2 , Gregory O Voronin 2 , Joanne Bennett 3 , Anne Cram 3 , Leonid Kagan 2 , Martin C Garnett 1 , Clive J Roberts 1 , Pavel Gershkovich 1
European Journal of Pharmaceutics and Biopharmaceutics ( IF 4.9 ) Pub Date : 2019-11-11 , DOI: 10.1016/j.ejpb.2019.11.001 Joseph Ali 1 , Manting Chiang 2 , Jong Bong Lee 2 , Gregory O Voronin 2 , Joanne Bennett 3 , Anne Cram 3 , Leonid Kagan 2 , Martin C Garnett 1 , Clive J Roberts 1 , Pavel Gershkovich 1
Affiliation
|
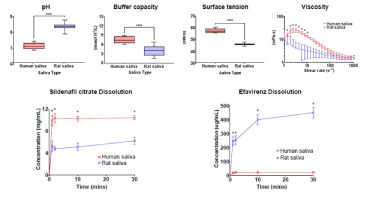
Recently there has been an increased interest to develop specialised dosage forms that are better suited to specific patient populations, such as paediatrics and geriatrics. In these patient populations the acceptability of the oral dosage form can be paramount to the products success. However, many Active Pharmaceutical Ingredients (APIs) are known to cause an aversive taste response. One way to increase the acceptability and to enhance the palatability of the formulation is to design coated taste-masked particulate-based dosage forms. The masking of poorly tasting drugs with physical barriers such as polymer coatings can be utilised to prevent the release of drug within the oral cavity, thus preventing a taste response. However, currently, there are few assessment tools and models available to test the efficiency of these particulate-based taste-masked formulations. The rat brief access taste aversion model has been shown to be useful in assessment of taste for liquid dosage forms. However, the applicability of the rat model for particulate-based taste masked formulations is yet to be assessed. It is not understood whether dissolution, solubility and thus exposure of the drug to taste receptors would be the same in rat and human. Therefore, rat saliva must be compared to human saliva to determine the likelihood that drug release would be similar within the oral cavity for both species. In this study rat saliva was characterised for parameters known to be important for drug dissolution, such as pH, buffer capacity, surface tension, and viscosity. Subsequently dissolution of model bitter tasting compounds, sildenafil citrate and efavirenz, in rat saliva was compared to dissolution in human saliva. For all parameters characterised and for the dissolution of both drugs in rat saliva, a substantial difference was observed when compared to human saliva. This discrepancy in saliva parameters and dissolution of model drugs suggests that preclinical taste evaluation of particulate-based taste-masked formulations suggests rat is not a good model for predicting taste of solid dosage forms or undissolved drug where dissolution is required. Alternative preclinical in vivo models in other species, or improved biorelevant in vitro models should be considered instead.
中文翻译:

大鼠是评估基于颗粒的掩味配方的好模型吗?
最近,人们对开发更适合特定患者群体(例如儿科和老年病患者)的专用剂型的兴趣日益浓厚。在这些患者人群中,口服剂型的可接受性对于产品成功至关重要。但是,已知许多活性药物成分(API)会引起厌恶的味觉反应。增加制剂的可接受性并增加其适口性的一种方法是设计包衣的掩味掩盖的基于颗粒的剂型。可以利用具有物理屏障(例如聚合物涂层)的口感较差的药物进行掩盖,以防止药物在口腔内释放,从而防止味觉反应。但是,目前,很少有评估工具和模型可用于测试这些基于颗粒的掩味配方的效率。已经证明大鼠短暂进入味觉厌恶模型可用于评估液体剂型的味觉。但是,大鼠模型对基于颗粒的掩味制剂的适用性尚待评估。尚不了解在大鼠和人类中,药物的溶解度,溶解度以及因此与味觉受体的接触是否相同。因此,必须将大鼠的唾液与人的唾液进行比较,以确定两种物种在口腔内药物释放相似的可能性。在这项研究中,大鼠唾液的特征在于已知对药物溶解很重要的参数,例如pH值,缓冲液容量,表面张力和粘度。随后将模型苦味化合物柠檬酸西地那非和依非韦伦在大鼠唾液中的溶解与在人唾液中的溶解进行比较。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。
更新日期:2019-11-11
中文翻译:

大鼠是评估基于颗粒的掩味配方的好模型吗?
最近,人们对开发更适合特定患者群体(例如儿科和老年病患者)的专用剂型的兴趣日益浓厚。在这些患者人群中,口服剂型的可接受性对于产品成功至关重要。但是,已知许多活性药物成分(API)会引起厌恶的味觉反应。增加制剂的可接受性并增加其适口性的一种方法是设计包衣的掩味掩盖的基于颗粒的剂型。可以利用具有物理屏障(例如聚合物涂层)的口感较差的药物进行掩盖,以防止药物在口腔内释放,从而防止味觉反应。但是,目前,很少有评估工具和模型可用于测试这些基于颗粒的掩味配方的效率。已经证明大鼠短暂进入味觉厌恶模型可用于评估液体剂型的味觉。但是,大鼠模型对基于颗粒的掩味制剂的适用性尚待评估。尚不了解在大鼠和人类中,药物的溶解度,溶解度以及因此与味觉受体的接触是否相同。因此,必须将大鼠的唾液与人的唾液进行比较,以确定两种物种在口腔内药物释放相似的可能性。在这项研究中,大鼠唾液的特征在于已知对药物溶解很重要的参数,例如pH值,缓冲液容量,表面张力和粘度。随后将模型苦味化合物柠檬酸西地那非和依非韦伦在大鼠唾液中的溶解与在人唾液中的溶解进行比较。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。对于所有表征的参数以及两种药物在大鼠唾液中的溶出度,与人唾液相比均观察到实质性差异。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。唾液参数和模型药物溶出度的这种差异表明,基于颗粒的掩味制剂的临床前味觉评价表明,大鼠不是预测需要溶解的固体剂型或未溶出药物的味道的好模型。相反,应考虑使用其他物种的替代临床前体内模型,或改善的生物相关体外模型。

























 京公网安备 11010802027423号
京公网安备 11010802027423号