当前位置:
X-MOL 学术
›
Nat. Rev. Clin. Oncol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
From state-of-the-art treatments to novel therapies for advanced-stage pancreatic cancer.
Nature Reviews Clinical Oncology ( IF 78.8 ) Pub Date : 2019-11-08 , DOI: 10.1038/s41571-019-0281-6 Christopher Nevala-Plagemann 1 , Manuel Hidalgo 2 , Ignacio Garrido-Laguna 1, 3
Nature Reviews Clinical Oncology ( IF 78.8 ) Pub Date : 2019-11-08 , DOI: 10.1038/s41571-019-0281-6 Christopher Nevala-Plagemann 1 , Manuel Hidalgo 2 , Ignacio Garrido-Laguna 1, 3
Affiliation
|
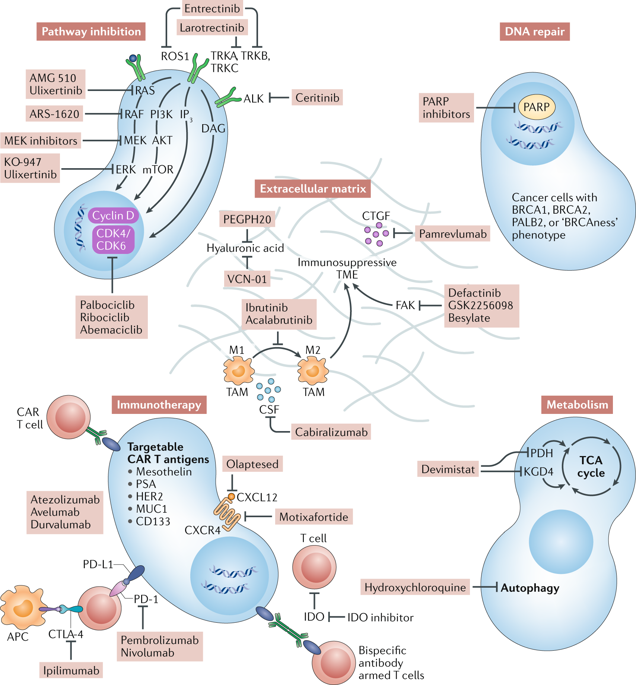
Improvements in the outcomes of patients with pancreatic ductal adenocarcinoma (PDAC) have lagged behind advances made in the treatment of many other malignancies over the past few decades. For most patients with PDAC, cytotoxic chemotherapy remains the mainstay of treatment. For patients with resectable disease, modified 5-fluorouracil, leucovorin, irinotecan and oxaliplatin (mFOLFIRINOX) is the standard-of-care adjuvant therapy, although data from several randomized trials have shown improved outcomes with neoadjuvant treatment strategies. For patients with advanced-stage or metastatic disease, comprehensive genomic profiling has revealed several potentially actionable alterations in small subsets of patients and the feasibility of implementing such strategies is beginning to be confirmed. Novel therapies targeting certain aberrations, most notably BRCA1/2 mutations, mismatch repair (MMR) deficiencies or NTRK1-3 fusions, have shown considerable activity in clinical trials, and larotrectinib, entrectinib and pembrolizumab have received FDA approval for the treatment of patients with tumours harbouring NTRK fusions and MMR deficiencies, respectively, regardless of primary tumour histology. In this Review, we describe the available data on the activity of these and other agents in patients with PDAC. Our discussion is structured according to the acronym 'PRIME' to organize the various treatment strategies currently undergoing evaluation in clinical trials: Pathway inhibition, alteration of DNA Repair pathways, Immunotherapy, cancer Metabolism and targeting the Extracellular tumour microenvironment.
中文翻译:

从最先进的治疗方法到晚期胰腺癌的新疗法。
在过去的几十年中,胰腺导管腺癌 (PDAC) 患者预后的改善落后于许多其他恶性肿瘤的治疗进展。对于大多数 PDAC 患者,细胞毒性化疗仍然是主要的治疗方法。对于可切除疾病的患者,改良的 5-氟尿嘧啶、亚叶酸、伊立替康和奥沙利铂 (mFOLFIRINOX) 是标准的辅助治疗,尽管来自几项随机试验的数据显示新辅助治疗策略可以改善结果。对于晚期或转移性疾病患者,全面的基因组分析揭示了一小部分患者可能发生的一些可操作的改变,实施此类策略的可行性开始得到证实。针对某些畸变的新疗法,最值得注意的是 BRCA1/2 突变、错配修复 (MMR) 缺陷或 NTRK1-3 融合,在临床试验中显示出相当大的活性,并且 larotrectinib、entrectinib 和 pembrolizumab 已获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,分别与原发性肿瘤组织学无关。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。在临床试验中显示出相当大的活性,无论原发性肿瘤组织学如何,larotrectinib、entrectinib 和 pembrolizumab 已分别获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。在临床试验中显示出相当大的活性,无论原发性肿瘤组织学如何,larotrectinib、entrectinib 和 pembrolizumab 已分别获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。entrectinib 和 pembrolizumab 已分别获得 FDA 批准,用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,无论原发肿瘤组织学如何。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。entrectinib 和 pembrolizumab 已分别获得 FDA 批准,用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,无论原发肿瘤组织学如何。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。
更新日期:2019-11-08
中文翻译:

从最先进的治疗方法到晚期胰腺癌的新疗法。
在过去的几十年中,胰腺导管腺癌 (PDAC) 患者预后的改善落后于许多其他恶性肿瘤的治疗进展。对于大多数 PDAC 患者,细胞毒性化疗仍然是主要的治疗方法。对于可切除疾病的患者,改良的 5-氟尿嘧啶、亚叶酸、伊立替康和奥沙利铂 (mFOLFIRINOX) 是标准的辅助治疗,尽管来自几项随机试验的数据显示新辅助治疗策略可以改善结果。对于晚期或转移性疾病患者,全面的基因组分析揭示了一小部分患者可能发生的一些可操作的改变,实施此类策略的可行性开始得到证实。针对某些畸变的新疗法,最值得注意的是 BRCA1/2 突变、错配修复 (MMR) 缺陷或 NTRK1-3 融合,在临床试验中显示出相当大的活性,并且 larotrectinib、entrectinib 和 pembrolizumab 已获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,分别与原发性肿瘤组织学无关。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。在临床试验中显示出相当大的活性,无论原发性肿瘤组织学如何,larotrectinib、entrectinib 和 pembrolizumab 已分别获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。在临床试验中显示出相当大的活性,无论原发性肿瘤组织学如何,larotrectinib、entrectinib 和 pembrolizumab 已分别获得 FDA 批准用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。entrectinib 和 pembrolizumab 已分别获得 FDA 批准,用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,无论原发肿瘤组织学如何。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。entrectinib 和 pembrolizumab 已分别获得 FDA 批准,用于治疗具有 NTRK 融合和 MMR 缺陷的肿瘤患者,无论原发肿瘤组织学如何。在这篇综述中,我们描述了这些药物和其他药物在 PDAC 患者中的活性的可用数据。我们的讨论是根据首字母缩写词“PRIME”来组织目前正在临床试验中评估的各种治疗策略:通路抑制、DNA 修复通路的改变、免疫治疗、癌症代谢和靶向细胞外肿瘤微环境。


























 京公网安备 11010802027423号
京公网安备 11010802027423号