当前位置:
X-MOL 学术
›
Acc. Chem. Res.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
An Oculus to Profile and Probe Target Engagement In Vivo: How T-REX Was Born and Its Evolution into G-REX
Accounts of Chemical Research ( IF 18.3 ) Pub Date : 2020-11-23 , DOI: 10.1021/acs.accounts.0c00537 Marcus J C Long 1 , Chloé Rogg 2 , Yimon Aye 2
Accounts of Chemical Research ( IF 18.3 ) Pub Date : 2020-11-23 , DOI: 10.1021/acs.accounts.0c00537 Marcus J C Long 1 , Chloé Rogg 2 , Yimon Aye 2
Affiliation
|
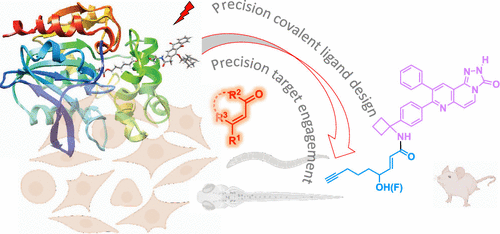
Here we provide a personal account of innovation and design principles underpinning a method to interrogate precision electrophile signaling that has come to be known as “REX technologies”. This Account is framed in the context of trying to improve methods of target mining and understanding of individual target–ligand engagement by a specific natural electrophile and the ramifications of this labeling event in cells and organisms. We start by explaining from a practical standpoint why gleaning such understanding is critical: we are constantly assailed by a battery of electrophilic molecules that exist as a consequence of diet, food preparation, ineluctable endogenous metabolic processes, and potentially disease. The resulting molecules, which are detectable in the body, appear to be able to modify function of specific proteins. Aside from potentially being biologically relevant in their own right, these labeling events are essentially identical to protein–covalent drug interactions. Thus, on what proteins and even in what ways a covalent drug will work can be understood through the eyes of natural electrophiles; extending this logic leads to the postulate that target identification of specific electrophiles can inform on drug design. However, when we entered this field, there was no way to interrogate how a specific labeling event impacted a specific protein in an unperturbed cell. Methods to evaluate stoichiometry of labeling, and even chemospecificity of a specific phenotype were limited. There were further no generally accepted ways to study electrophile signaling that did not hugely disturb physiology.
中文翻译:

概述和探查目标参与度的Oculus:T-REX的诞生方式及其演变为G-REX
在这里,我们对创新和设计原理进行了个人介绍,为询问精密亲电信号的方法奠定了基础,该方法已被称为“ REX技术”。此帐户的背景是尝试改进目标挖掘的方法,以及对特定天然亲电试剂对单个目标配体参与的理解以及此标记事件在细胞和生物体中的影响。我们从实际的角度开始解释为什么收集这样的理解是至关重要的:由于饮食,食物制备,不可避免的内源性代谢过程和潜在的疾病而导致的一系列亲电子分子不断困扰我们。在体内可检测到的所得分子似乎能够修饰特定蛋白质的功能。除了自身可能具有生物学相关性外,这些标记事件与蛋白质-共价药物相互作用基本相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入这个领域时,没有办法询问一个特定的标记事件如何影响一个不受干扰的细胞中一个特定的蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。这些标记事件基本上与蛋白质-共价药物相互作用相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入这个领域时,没有办法询问一个特定的标记事件如何影响一个不受干扰的细胞中一个特定的蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。这些标记事件基本上与蛋白质-共价药物相互作用相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。通过天然亲电试剂的眼睛可以了解哪些蛋白质甚至共价药物将以何种方式起作用;扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。通过天然亲电试剂的眼睛可以了解哪些蛋白质甚至共价药物将以何种方式起作用;扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。
更新日期:2020-11-23
中文翻译:

概述和探查目标参与度的Oculus:T-REX的诞生方式及其演变为G-REX
在这里,我们对创新和设计原理进行了个人介绍,为询问精密亲电信号的方法奠定了基础,该方法已被称为“ REX技术”。此帐户的背景是尝试改进目标挖掘的方法,以及对特定天然亲电试剂对单个目标配体参与的理解以及此标记事件在细胞和生物体中的影响。我们从实际的角度开始解释为什么收集这样的理解是至关重要的:由于饮食,食物制备,不可避免的内源性代谢过程和潜在的疾病而导致的一系列亲电子分子不断困扰我们。在体内可检测到的所得分子似乎能够修饰特定蛋白质的功能。除了自身可能具有生物学相关性外,这些标记事件与蛋白质-共价药物相互作用基本相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入这个领域时,没有办法询问一个特定的标记事件如何影响一个不受干扰的细胞中一个特定的蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。这些标记事件基本上与蛋白质-共价药物相互作用相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入这个领域时,没有办法询问一个特定的标记事件如何影响一个不受干扰的细胞中一个特定的蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。这些标记事件基本上与蛋白质-共价药物相互作用相同。因此,可以通过天然亲电试剂的眼睛了解什么蛋白质甚至共价药物将以什么方式起作用。扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。通过天然亲电试剂的眼睛可以了解哪些蛋白质甚至共价药物将以何种方式起作用;扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。通过天然亲电试剂的眼睛可以了解哪些蛋白质甚至共价药物将以何种方式起作用;扩展这种逻辑导致假定特定亲电试剂的靶标鉴定可以影响药物设计。但是,当我们进入该领域时,没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。没有办法询问特定标记事件如何影响未受干扰的细胞中的特定蛋白质。评估标记化学计量,甚至特定表型的化学特异性的方法受到限制。此外,还没有普遍接受的方法来研究不会严重干扰生理的亲电信号。


























 京公网安备 11010802027423号
京公网安备 11010802027423号