当前位置:
X-MOL 学术
›
ChemBioChem
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
Millisecond Allosteric Dynamics of Activated Ras Reproduced with a Slowly Hydrolyzable GTP Analogue
ChemBioChem ( IF 3.2 ) Pub Date : 2020-11-02 , DOI: 10.1002/cbic.202000698 Xiaomin Chen 1 , Hexuan Gao 1 , Dong Long 1, 2
ChemBioChem ( IF 3.2 ) Pub Date : 2020-11-02 , DOI: 10.1002/cbic.202000698 Xiaomin Chen 1 , Hexuan Gao 1 , Dong Long 1, 2
Affiliation
|
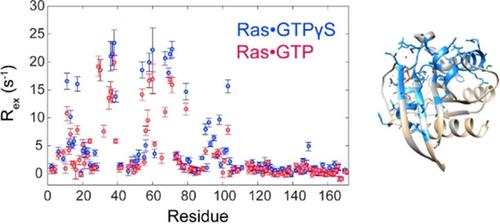
Slowly does it: The correlated internal motions of GTPγS‐bound Ras have been quantified using relaxation dispersion NMR spectroscopy with site‐specific details, demonstrating its accurate preservation of the physiological dynamics network critical for the binding of allosteric ligands.

中文翻译:

用可缓慢水解的 GTP 类似物再现活化 Ras 的毫秒变构动力学
慢慢来:GTPγS 结合的 Ras 的相关内部运动已使用具有位点特定细节的弛豫色散 NMR 光谱进行量化,证明其准确保存了对变构配体的结合至关重要的生理动力学网络。

更新日期:2020-11-02

中文翻译:

用可缓慢水解的 GTP 类似物再现活化 Ras 的毫秒变构动力学
慢慢来:GTPγS 结合的 Ras 的相关内部运动已使用具有位点特定细节的弛豫色散 NMR 光谱进行量化,证明其准确保存了对变构配体的结合至关重要的生理动力学网络。



























 京公网安备 11010802027423号
京公网安备 11010802027423号