当前位置:
X-MOL 学术
›
Cell Prolif.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
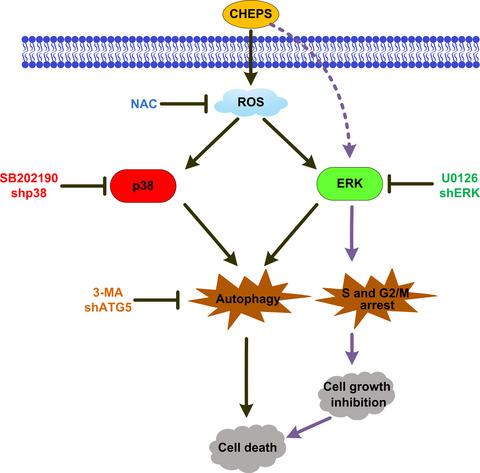
Exopolysaccharide from Cryptococcus heimaeyensis S20 induces autophagic cell death in non‐small cell lung cancer cells via ROS/p38 and ROS/ERK signalling
Cell Proliferation ( IF 8.5 ) Pub Date : 2020-06-29 , DOI: 10.1111/cpr.12869 Yao Hao 1 , Yao Huang 2 , Jingyi Chen 1 , Jiadai Li 1 , Yuncong Yuan 1 , Mingzhen Wang 1 , Lingling Han 1 , Xiu Xin 3 , Hailong Wang 1 , Danqing Lin 2 , Fang Peng 2, 4 , Fang Yu 5 , Congyi Zheng 1, 4 , Chao Shen 1, 4
Cell Proliferation ( IF 8.5 ) Pub Date : 2020-06-29 , DOI: 10.1111/cpr.12869 Yao Hao 1 , Yao Huang 2 , Jingyi Chen 1 , Jiadai Li 1 , Yuncong Yuan 1 , Mingzhen Wang 1 , Lingling Han 1 , Xiu Xin 3 , Hailong Wang 1 , Danqing Lin 2 , Fang Peng 2, 4 , Fang Yu 5 , Congyi Zheng 1, 4 , Chao Shen 1, 4
Affiliation
|
Abstract Objectives Cryptococcus heimaeyensis S20 is found in Antarctica and can produce exopolysaccharides (CHEPS). Here, we explore the anti‐tumour effects of CHEPS on non‐small cell lung cancer (NSCLC). Materials and methods Cell viability was assessed by CCK8 and colony formation assays. Flow cytometry was used to analyse the cell cycle, cell apoptosis and reactive oxygen species (ROS). Cell autophagy was detected by EGFP‐LC3 puncta assay, Lyso‐Tracker Red staining and transmission electron microscopy. mRNA and protein levels were analysed by qRT‐PCR and Western blot. Related mechanisms were confirmed using appropriate inhibitors or shRNA. In vitro results were further confirmed by a tumour xenograft study. Results CHEPS inhibited the proliferation of NSCLC cells by inducing S‐ and G2/M‐phase arrest and autophagic cell death, but not apoptosis. CHEPS was less toxic to normal human embryonic lung fibroblasts. CHEPS activated the MAPK pathway in NSCLC cells, and p38 and ERK promoted CHEPS‐induced cell death. Further studies showed that p38 and ERK promoted CHEPS‐induced NSCLC cell autophagy and ERK promoted CHEPS‐induced S‐ and G2/M‐phase arrest. ROS were induced by CHEPS. A ROS scavenger attenuated CHEPS‐induced p38 and ERK activation, autophagy and cell death. Finally, CHEPS reduced orthotopic lung tumour growth without organ‐related toxicity. CHEPS also induced ROS, activated p38 and ERK, and triggered autophagy in vivo. Conclusions CHEPS induces autophagic cell death and S‐ and G2/M‐phase arrest in NSCLC cells via ROS/p38 and ROS/ERK signalling.
中文翻译:

黑麦隐球菌S20胞外多糖通过ROS/p38和ROS/ERK信号诱导非小细胞肺癌细胞自噬性细胞死亡
摘要 目的 黑麦隐球菌 S20 发现于南极洲,可产生胞外多糖(CHEPS)。在这里,我们探讨了 CHEPS 对非小细胞肺癌 (NSCLC) 的抗肿瘤作用。材料和方法通过CCK8和集落形成分析评估细胞活力。流式细胞术用于分析细胞周期、细胞凋亡和活性氧(ROS)。通过 EGFP-LC3 斑点测定、Lyso-Tracker Red 染色和透射电子显微镜检测细胞自噬。通过 qRT-PCR 和蛋白质印迹分析 mRNA 和蛋白质水平。使用适当的抑制剂或 shRNA 证实了相关机制。肿瘤异种移植研究进一步证实了体外结果。结果 CHEPS 通过诱导 S 期和 G2/M 期阻滞和自噬细胞死亡来抑制 NSCLC 细胞的增殖,但不抑制细胞凋亡。CHEPS 对正常人胚胎肺成纤维细胞的毒性较小。CHEPS 激活 NSCLC 细胞中的 MAPK 通路,p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。
更新日期:2020-06-29
中文翻译:

黑麦隐球菌S20胞外多糖通过ROS/p38和ROS/ERK信号诱导非小细胞肺癌细胞自噬性细胞死亡
摘要 目的 黑麦隐球菌 S20 发现于南极洲,可产生胞外多糖(CHEPS)。在这里,我们探讨了 CHEPS 对非小细胞肺癌 (NSCLC) 的抗肿瘤作用。材料和方法通过CCK8和集落形成分析评估细胞活力。流式细胞术用于分析细胞周期、细胞凋亡和活性氧(ROS)。通过 EGFP-LC3 斑点测定、Lyso-Tracker Red 染色和透射电子显微镜检测细胞自噬。通过 qRT-PCR 和蛋白质印迹分析 mRNA 和蛋白质水平。使用适当的抑制剂或 shRNA 证实了相关机制。肿瘤异种移植研究进一步证实了体外结果。结果 CHEPS 通过诱导 S 期和 G2/M 期阻滞和自噬细胞死亡来抑制 NSCLC 细胞的增殖,但不抑制细胞凋亡。CHEPS 对正常人胚胎肺成纤维细胞的毒性较小。CHEPS 激活 NSCLC 细胞中的 MAPK 通路,p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。p38 和 ERK 促进 CHEPS 诱导的细胞死亡。进一步的研究表明,p38 和 ERK 促进 CHEPS 诱导的 NSCLC 细胞自噬,ERK 促进 CHEPS 诱导的 S 期和 G2/M 期阻滞。ROS 是由 CHEPS 诱导的。ROS 清除剂减弱了 CHEPS 诱导的 p38 和 ERK 激活、自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。自噬和细胞死亡。最后,CHEPS 减少了原位肺肿瘤的生长,而没有器官相关毒性。CHEPS 还诱导 ROS,激活 p38 和 ERK,并在体内触发自噬。结论 CHEPS 通过 ROS/p38 和 ROS/ERK 信号传导诱导 NSCLC 细胞的自噬细胞死亡和 S 期和 G2/M 期阻滞。


























 京公网安备 11010802027423号
京公网安备 11010802027423号