全新磷酸酶募集嵌合体实现靶蛋白精准去磷酸化调控
蛋白的磷酸化修饰是重要的翻译后修饰之一,在蛋白正常生物功能的行使中起到重要的调控作用,其调控异常往往与多种疾病密切关联。那么如何实现致病靶标蛋白的磷酸化精准调控呢?近日,中国药科大学王磊(点击查看介绍)/尤启冬(点击查看介绍)团队通过设计磷酸酶募集嵌合体(PhoRC)拉近蛋白磷酸酶PP5和底物蛋白ASK1相互作用,实现了ASK1的去磷酸化精准调控。
该研究工作以共伴侣蛋白PP5的磷酸酶功能为基础,通过将PP5和底物蛋白ASK1的小分子配体通过化学连接链相连,发现了PhoRC磷酸酶募集嵌合体多特异性小分子DDO3711,可特异性将p-ASK1T838去磷酸化,解决了胃癌细胞中因 ASK1 的过度磷酸化而导致的细胞异常增殖问题。DDO3711能够以直接结合并拉近 ASK1 和 PP5 的方式来促进p-ASK1T838的去磷酸化调控,进而抑制ASK1下游信号通路JNK、p-38的激活以及细胞周期相关蛋白CDK4/6、cyclin D1的表达,最终实现了显著的抗胃癌细胞增殖效果。以上研究充分利用了共伴侣蛋白PP5的磷酸酶功能,巧妙地设计小分子调控剂将其与过度磷酸化的底物蛋白相连,在不影响底物蛋白表达的同时,实现了对其磷酸化过程的精准调控,为小分子调控蛋白的翻译后修饰过程提供了重要研究思路与范例。
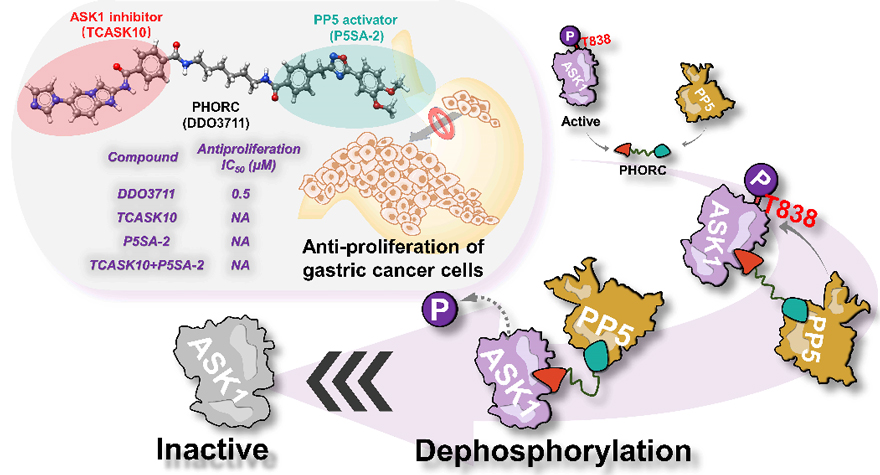
分子设计原理
这一成果近期发表在国际著名期刊Journal of the American Chemical Society,中国药科大学王磊副教授、尤启冬教授、张连山教授为本论文的通讯作者,博士后张秋月为本文的第一作者,中国药科大学为本论文的第一通讯单位。该工作获得了国家自然科学基金重点项目、面上项目、青年项目(82173741, 82003582, 81930100),江苏省自然科学基金青年项目(BK20190559)以及中国科协青年人才托举工程项目(2021QNRC001)的资助。
近年来,王磊/尤启冬团队围绕靶向分子伴侣系统复杂蛋白相互作用的小分子药物设计开展了大量研究工作,基于伴侣系统与底物识别机制提出了多种分子设计新策略并取得了多项重要研究成果(J. Med. Chem. 2022, 65, 8144-8168; J. Med. Chem. 2022, 65, 10809-10847; J. Med. Chem. 2022, 65, 8091-8112; J. Med. Chem. 2021, 64, 8916-8938; J. Med. Chem. 2020, 63, 1281-1297; Acta. Pharm Sin. B. 2020, 10, 1904-1925; Sci. Adv. 2019, 5, eaax2277)。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Protein Phosphatase 5-Recruiting Chimeras for Accelerating Apoptosis-Signal-Regulated Kinase 1 Dephosphorylation with Antiproliferative Activity
Qiuyue Zhang, Xuexuan Wu, Hengheng Zhang, Qiuyu Wu, Min Fu, Liwen Hua, Xinyue Zhu, Yuqi Guo, Lianshan Zhang*, Qidong You*, and Lei Wang*
J. Am. Chem. Soc., 2022, DOI: 10.1021/jacs.2c10759
导师介绍
王磊
https://www.x-mol.com/university/faculty/296757
尤启冬
https://www.x-mol.com/university/faculty/49905
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号