铑催化不对称Satoh–Miura反应构建轴手性化合物
过渡金属催化芳香化合物通过两次碳–氢键活化实现与炔烃的增环反应(Satoh–Miura反应),是构建稠环芳香体系的一类重要的策略。然而,发展不对称Satoh–Miura反应需要实现对高张力环金属物种反应路径的精准调控,具有极大的挑战性。目前文献已知的该类反应极少(汪君等,Angew. Chem. Int. Ed. 2019, 58, 6732)(图1a, b)。
中国科学院上海有机化学研究所游书力研究员(点击查看介绍)团队一直致力于通过过渡金属催化的不对称碳氢键活化反应构建平面手性、轴手性和螺旋手性分子(Acc. Chem. Res. 2017, 50, 351; J. Am. Chem. Soc. 2021, 143, 14025)。2021年,该团队利用手性环戊二烯基铑络合物(SCpRh)为催化剂实现了1-芳基异喹啉类衍生物与炔烃的碳–氢键活化增环反应,实现了一类手性氮杂螺烯盐的高对映选择性合成(J. Am. Chem. Soc. 2021, 143, 114)(图1c, eq 1)。最近该团队发现该反应体系中铑催化剂的抗衡阴离子对于调控环铑物种的反应路径起到关键作用。当使用具有较强碱性和配位能力的醋酸根作为抗衡阴离子时,生成氮杂螺烯盐的反应路径被完全抑制。在该条件下环铑物种与两分子炔烃发生Satoh–Miura反应,高对映选择性地生成轴手性稠环多芳基化合物(图1c, eq 2)。
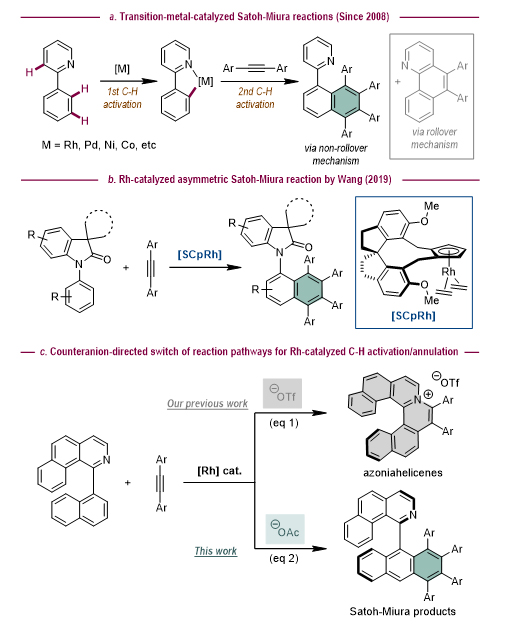
图1. 过渡金属催化的碳–氢键活化/增环反应
研究人员考察了一系列螺二氢茚衍生的手性环戊二烯基铑配合物催化1-萘基苯并异喹啉与二苯基乙炔反应的活性,发现环戊二烯基上的取代基对反应效果有显著的影响,其中叔丁基取代的环戊二烯基铑配合物为最优催化剂。在醋酸铜为氧化剂和体系抗衡阴离子主要来源时,一系列芳基异喹啉衍生物1与二芳基乙炔2可以顺利发生Satoh–Miura反应,以优秀的收率(up to 85%)和对映选择性(up to 96% ee)获得轴手性稠环多芳基化合物3(图2)。

图2. 底物普适性考察
在控制实验中,研究人员使用银盐(AgX)为体系唯一抗衡阴离子来源,证实了铑催化剂的抗衡阴离子对于反应路径的显著影响(图3)。使用具有较强碱性及配位能力的阴离子有助于得到Satoh–Miura反应产物3aa;而使用弱碱性和非配位性阴离子则易于得到氮杂螺烯盐6。密度泛函理论(DFT)计算揭示了抗衡阴离子调控环铑中间体反应路径的机制。醋酸阴离子促进了该环铑中间体中铑–氮键的断裂和第二次碳–氢键活化/环化过程,进而得到Satoh–Miura反应产物;而三氟甲磺酸阴离子则促进环铑中间体直接碳–氮键还原消除,得到氮杂螺烯盐产物。
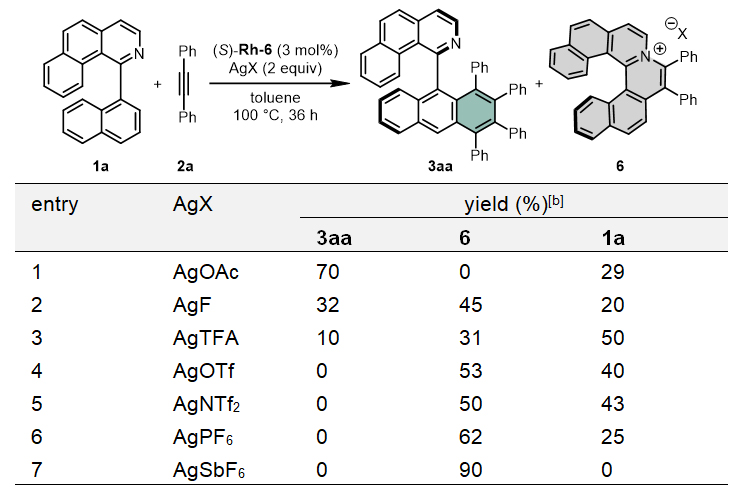
图3. 控制实验
小结
游书力研究员团队报道了铑催化1-萘基苯并异喹啉与二苯基乙炔的不对称Satoh–Miura反应,揭示了抗衡阴离子调控环铑中间体反应路径的机制,为不对称碳–氢键活化反应的设计提供了新的思路。相关研究结果以通讯形式发表在近期的Angew. Chem. Int. Ed.杂志上。文章的第一作者是博士生张文文,通讯作者是郑超副研究员和游书力研究员。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

(SCp)Rhodium-Catalyzed Asymmetric Satoh–Miura Reaction for Buildingup Axial Chirality: Counteranion-Directed Switching of Reaction Pathways
Wen-Wen Zhang, Qiang Wang, Su-Zhen Zhang, Chao Zheng, Shu-Li You
Angew. Chem. Int. Ed., 2022, DOI: 10.1002/anie.202214460
导师介绍
游书力
https://www.x-mol.com/university/faculty/15598
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号