计算机模拟用于设计核酸修复酶的纳米荧光探针
核酸修复酶参与维持基因组完整性,与多种疾病的发生发展密切相关,是多种治疗疗法开发的关键靶标。核酸修复酶的细胞内分布和动态变化为我们了解它们在细胞信号通路中的生理功能和作用提供了重要信息。采用以核酸修复酶的水解底物为骨架的DNA探针是实现核酸修复酶体内外可视化的重要手段。然而,常规设计和优化探针的方法依赖于开发者的经验,费时费力。因此,如何快速有效的设计对目标蛋白灵敏、特异的探针,是一个需要解决的难题。
广州中医药大学翟筠秋所在团队利用计算机模拟研究发现核酸修复酶与其底物的相互作用机制,并基于此进行有效的探针设计。核酸修复酶与其产物之间普遍存在产物抑制问题,即积累的切割产物可以与底物竞争导致反应速率下降,这显著影响了DNA探针的灵敏度。团队从具有代表性的核酸修复酶(脱嘌呤脱嘧啶核酸修复酶1,APE1)出发,采用计算机对APE1及其不同底物进行分子模拟,发现了APE1与其反应底物的相互作用机制,并在此基础上合理设计了产物解离速度快的新型结构DNA探针。进一步实验结果表明,该探针成功消除了产物抑制效应,并显著提高了的灵敏度,表明分子模拟在探针设计中的可行性。以该DNA探针为基础组装得到的DNA纳米探针可以灵敏、专一的对细胞内的APE1进行响应,有效区分多种癌细胞与正常细胞,还可以动态观察不同药物对APE1活性的影响。这项工作为快速有效开发核酸修复酶及其它目标物的探针提供了新方法,也为APE1在活细胞内的动态监测提供平台。
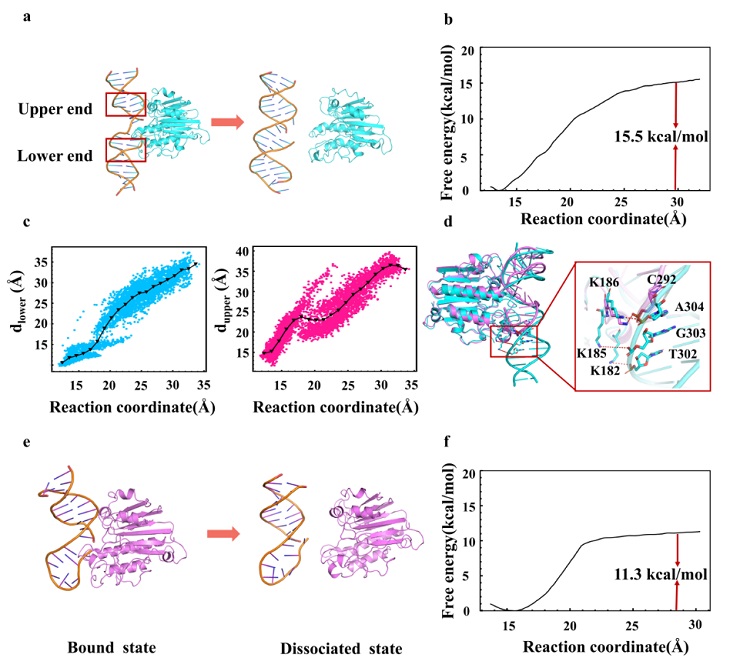
图1. 使用计算机模拟方法探究探针与DNA修复酶(APE1)的相互作用机制。(a) APE1-dsDNA 产物系统的解离。(b) 表征APE1和dsDNA从结合态到解离态的结合自由能分布图。(c) dsDNA 上端和下端相对于反应坐标的解离,由 APE1 与 dsDNA 上/下端之间的距离表示。(d) 通过减少与APE1的相互作用以设计Probe N。dsDNA-APE1 复合物用青色显示,Probe N-APE1 复合物用紫色显示。Probe N 与 K182 、K185 没有相互作用。(e) APE1-Probe N产物系统的解离。(f) Probe N 产物从 APE1 解离的结合自由能分布图。
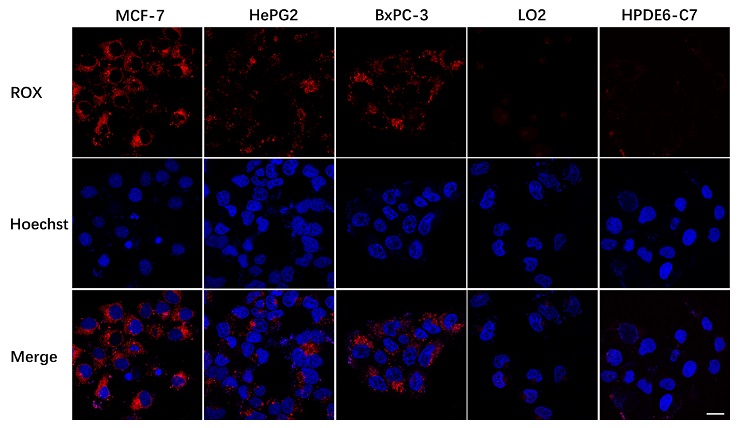
图2. DNA纳米探针对癌细胞和正常细胞的区分。DNA纳米探针对不同细胞中APE1活性的荧光成像(标尺:20 μm)。
本文发表在Biosensors and Bioelectronics 期刊,通讯作者为广州中医药大学杏林青年学者翟筠秋。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Computer simulation and design of DNA-nanoprobe for fluorescence imaging DNA repair enzyme in living cells
Cheng Tian, Guangzhong Liang, Chunyi Wang, Ruikai He, Keni Ning, Zhe Li, Runduo Liu, Yan Ma, Shixia Guan, Jiewei Deng, Junqiu Zhai
Biosens. Bioelectron., 2022, 211, 114360, DOI: 10.1016/j.bios.2022.114360
通讯作者简介
翟筠秋,博士,硕士生导师,广州中医药大学“杏林青年学者”,广东省生物医药专业委员会委员。研究方向为肿瘤生物标志物的检测方法及其介导的药物递送系统。以第一或通讯作者(共同)在JACS、NAR、ACS Nano、BB、ACS AMI等期刊上发表SCI论文十余篇。主持国家级、省部级等基金5项。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号