Adv. Mater.:用于克服肿瘤多药耐药的钌配合物自组装纳米粒
肿瘤多药耐药 (MDR) 即肿瘤细胞对一种抗肿瘤药物产生耐药性的同时,对许多结构和功能完全不同的抗癌药产生交叉耐药性,如阿霉素和靶向药,是一种广谱的耐药现象。肿瘤MDR存在于化疗、靶向治疗、免疫治疗等过程中,是临床上肿瘤治疗的重点和难点。临床统计数据显示:90%以上肿瘤患者死因都与MDR有关。例如,临床常用的顺铂、米托蒽醌、阿霉素和三氧化二砷等抗肿瘤药物都面临肿瘤MDR问题。MDR产生的可能机制包括多种,其中通过降低细胞内的药物积累的ABC转运蛋白是被认为是最为经典和公认的机制。目前,临床上应用的对抗ABC转运蛋白介导MDR的药物种类、数量有限,有待开发。
最近,中山大学潘逸航、巢晖、曾乐立研究团队和美国圣约翰大学陈哲生团队在Advanced Materials 上在线发表研究性论文,经过多年潜心研究,在克服肿瘤MDR的抗肿瘤药物领域取得重要研究进展。作者通过巧妙的配体结构设计,设计了具有较好共轭平面配体的环金属化钌配合物,该钌配合物可在水介质中发生分子自组装,形成自组装纳米粒子。通过单晶结构解析和核磁共振图谱分析,该配合物可通过π-π及C-H键形成聚集体。研究结果显示,该配合物可在ABCB1和ABCG2均高表达的耐药肿瘤细胞内大量富集。通过体外实验和计算机模拟计算结果推测,ABCB1和ABCG2蛋白对该配合物的结合作用较弱,无法有力对配合物进行外排作用;同时钌配合物自组装形成纳米颗粒通过内吞方式进入细胞,可降低ABC转运蛋白的作用,从而实现钌配合物在耐药肿瘤细胞内的高浓度富集。通过进一步的机制实验发现,钌配合物可作用肿瘤细胞的有氧呼吸和糖酵解途径,能有效抑制肿瘤细胞的能量代谢途径,从而切断细胞的能量供应,这可进一步通过抑制ABC转运蛋白的泵出效率而维持钌配合物的胞内浓度,并且能导致肿瘤细胞死亡。该钌配合物被发现在多达28种亲本肿瘤细胞及7种耐药肿瘤细胞均表现出优异的抗肿瘤效果,并且在动物实验中也证实具有良好的抗肿瘤活性和生物安全性。
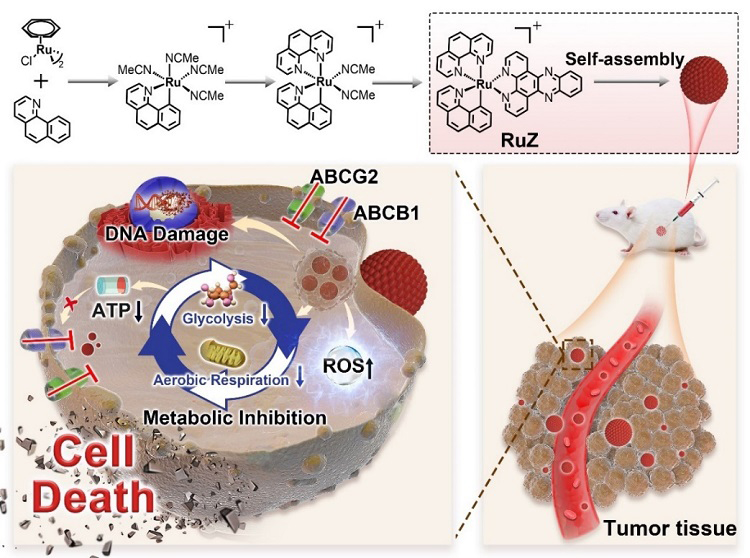
图片源自Adv. Mater.论文
相关研究成果已经在Advanced Materials 期刊上发表,并获中国发明专利授权一项。文章的通讯作者为中山大学附属第七医院的潘逸航研究员和曾乐立副研究员以及中山大学化学院巢晖教授和美国圣约翰大学Zhe-Sheng Chen(陈哲生)教授,第一作者为中山大学博士后李佳博士与曾乐立副研究员(共同一作)。研究成果得到了国家重点研发计划、国家自然科学基金青年项目、广东省消化系统恶性肿瘤防治研究重点实验室及广东省自然科学基金等项目资金的支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cycloruthenated Self-Assembly with Metabolic Inhibition to Efficiently Overcome Multidrug Resistance in Cancers
Jia Li, Leli Zeng, Zheng Wang, Hengxing Chen, Shuo Fang, Jinquan Wang, Chao-Yun Cai, Enming Xing, Xinxing Liao, Zhi-Wei Li, Charles R. Ashby Jr, Zhe-Sheng Chen, Hui Chao, Yihang Pan
Adv. Mater., 2022, 34, 2100245, DOI: 10.1002/adma.202100245
导师介绍
巢晖
https://www.x-mol.com/university/faculty/15309
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号