暨南大学药学院丁克教授团队采用构象限制策略发现大环类EGFR四代抑制剂
肺癌是发病率和死亡率增长最高,对人群健康和生命威胁最大的恶性肿瘤之一,因此针对肺癌的治疗手段是抗肿瘤药物的一大研究重点。其中,由于表皮生长因子受体(EGFR)为主要的肺癌驱动因子(突变占比超过20%,且更倾向于亚洲人群),开发EGFR抑制剂对肺癌患者进行靶向治疗,受到药物研究者的广泛关注。目前,已有五个小分子抑制剂,共三代药物批准上市。
尽管目前EGFR抑制剂在临床上得到广泛运用,但用药一段时间后往往会产生耐药性的问题,使患者的有效生存期未能得到明显改善。而对于目前治疗效果突出的三代药物奥西替尼(Osimertinib),目前临床上仍缺乏对抗耐药性的手段,急需开发新一代的药物。
近日,暨南大学丁克教授团队联合中科院上海药物所谢华研究员/丁健院士团队针对奥西替尼耐药的EGFR C797S耐药突变体,通过构象限制、优势片段杂交等药物化学优化策略,发现了一系列具有良好成药性前景的大环类EGFR四代抑制剂, 可为克服奥西替尼耐药的抗肺癌药物研究提供新的先导化合物和研究思路。相关研究成果近期在线发表于Journal of Medicinal Chemistry。
为寻找合适的先导化合物,研究人员首先根据奥西替尼与ALK抑制剂布加替尼(前期文献报道具有EGFR C797S突变体抑制活性)的结构和作用模式,设计并合成了一系列采用二者优势片段杂交的化合物(图1)。结果表明,针对耐药突变体,设计的化合物在酶水平上表现出优秀的抑制活性以及对EGFR突变体的选择性,其中,化合物17g在EGFRL858R/T790M/C797S中的IC50值为4.3 nM,显著优于阳性药布加替尼(表1)。
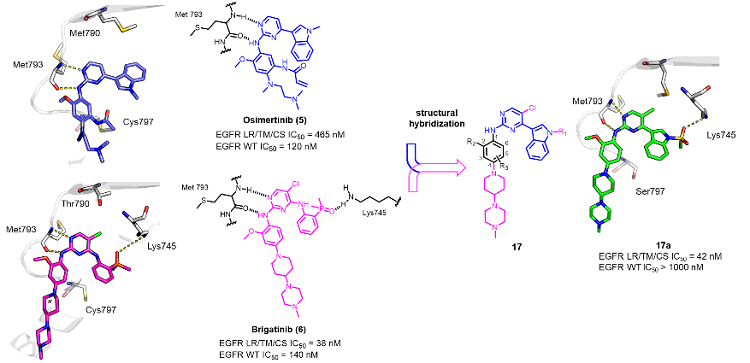
图1. 优势片段杂交的设计思路。图片来源:J. Med. Chem.
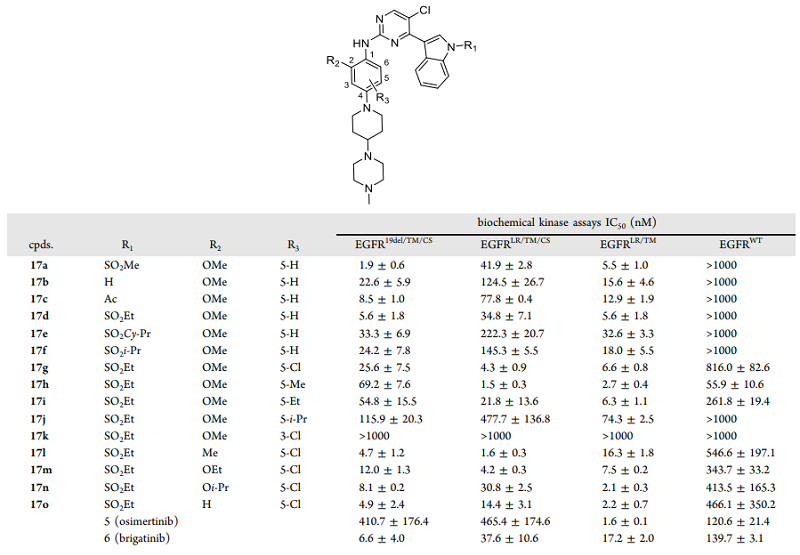
表1. 优势片段杂交化合物的构效关系。图片来源:J. Med. Chem.
然而,在进一步的实验中,研究人员发现化合物在细胞水平上的抑制效果不佳。研究人员认为该现象可能由于EGFR突变体与其抑制剂竞争性底物ATP的结合能力较高,以及在测试中细胞水平的ATP浓度远高于酶水平。为解决这一问题,研究人员结合化合物17g与EGFR的复合物结晶结构中的“U型构象”,设想通过构象限制策略,以构建大环固定活性构象,降低结合过程中熵增加导致的结合自由能损失,从而提高化合物在细胞水平的抑制效果。
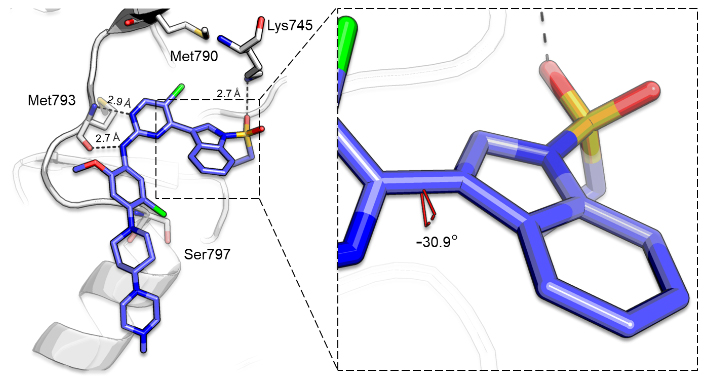
图2. 化合物17g与EGFR的复合物结构。图片来源:J. Med. Chem.
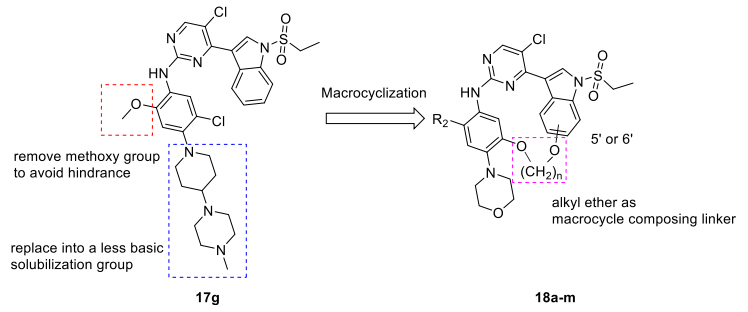
图3. 构象限制策略。图片来源:J. Med. Chem.
根据设计的思路,研究人员合成并测试了一系列连接位置、长度等不同的化合物在酶水平和细胞水平的抑制活性。结果表明,化合物18c在细胞水平的抑制活性上有很大的提高:对于Ba/F3 EGFRL858R/T790M/C797S的耐药细胞模型的生长抑制IC50为16 nM,活性相较于17g 提高了近200倍,同时在酶水平上也保持了较好的抑制效果,IC50 = 6.2 nM。研究人员进一步通过化合物18c与EGFR的复合物结晶结构,确认了18c保留了与17g类似的结合模式与构象,不同之处仅在于醚连接链固定了其“U型构象”。以上结果验证了构象限制策略提高抑制活性的设想。

表2. 构象限制后化合物的构效关系。图片来源:J. Med. Chem.
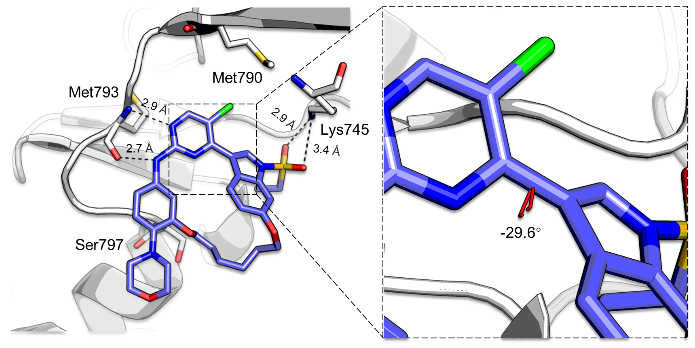
图4. 化合物18c与EGFR的复合物结构。图片来源:J. Med. Chem.
但化合物18c对于无EGFR突变的Ba/F3亲本细胞同样具有较高的生长抑制活性,提示其具有较高对正常细胞的毒性。因此,研究人员进一步在化合物18c的基础上进行药物化学改造,得到了化合物18j。其保留对EGFR突变细胞高活性的同时(IC50 = 36 nM),显著地降低了对Ba/F3亲本细胞的毒性(IC50 = 2.08 μM)。化合物18j的细胞抑制效果和选择性还在耐药的肿瘤细胞得到验证,同时,也验证了其机制是通过阻断EGFR的磷酸化以及其下游的信号通路而实现的。
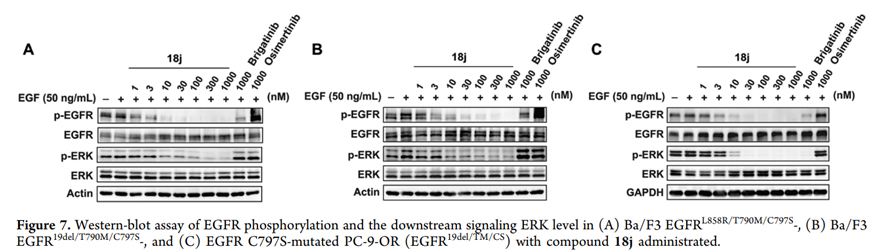
图5 在肿瘤细胞中,化合物18j剂量依赖性地阻断EGFR的磷酸化以及其下游的信号通路。图片来源:J. Med. Chem.
总之,该研究通过构象限制、优势片段杂交等药物化学优化策略,发现了一系列成药性良好的新型第四代EGFR抑制剂,代表性化合物18j在体外具有较好的抑制效果,可为克服奥西替尼/吉非替尼耐药的药物研究提供新的先导化合物和研究思路。该研究近日发表于J. Med. Chem.。论文第一作者为暨南大学药学院博士研究生陈灏,中科院上海药物所博士研究生赖梦珍,通讯作者为暨南大学药学院丁克教授和陆小云研究员,以及上海药物研究所谢华研究员。该研究得到了国家自然科学基金和国家科技重大专项新药创制等项目的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Conformational Constrained 4-(1-Sulfonyl-3-indol)yl-2-phenylaminopyrimidine Derivatives as New Fourth-Generation Epidermal Growth Factor Receptor Inhibitors Targeting T790M/C797S Mutations
Hao Chen, Mengzhen Lai, Tao Zhang, Yuqing Chen, Linjiang Tong, Sujie Zhu, Yang Zhou, Xiaomei Ren, Jian Ding, Hua Xie*, Xiaoyun Lu*, and Ke Ding*
J. Med. Chem., 2022, DOI: 10.1021/acs.jmedchem.2c00168
导师介绍
丁健
https://www.x-mol.com/university/faculty/21539
丁克
https://www.x-mol.com/groups/ding_ke
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号