Nano Res.│中山大学张旭东副教授课题组:基因工程细胞膜囊泡表达PD-1单链抗体用于肿瘤免疫治疗
本篇文章版权为 张旭东课题组所有,未经授权禁止转载。
背景介绍
近年来,癌症免疫疗法取得了令人瞩目的临床效果。其中,单克隆抗体免疫检查点疗法利用单克隆抗体阻断T细胞上的负性检查点,进而阻断肿瘤细胞对T细胞活性的抑制,从而靶向清除肿瘤细胞。目前针对PD-1/PD-L1检查点的研究最为广泛,多种PD-1单克隆抗体药物已经在临床治疗中取得了显著的疗效。然而,PD-1单抗疗法存在临床响应率低、易引发自身免疫攻击等毒副作用。因此,开发新型抗体递送和癌症免疫疗法仍具有迫切的临床需求。
在肿瘤微环境中,肿瘤细胞和调节性T细胞异常高表达CD39和CD73,在缺氧和高代谢环境下,催化ATP产生大量的腺苷并聚集在肿瘤部位。高浓度的腺苷与T细胞表面的A2a受体结合,抑制CD4+和CD8+ T细胞的功能,增强调节性T细胞的转录。因此,抑制腺苷与T细胞A2a受体结合可增强T细胞的抗肿瘤效应。
细胞膜囊泡是利用细胞膜制备的仿生外泌体纳米囊泡,具有良好的生物相容性和组织穿透力。通过基因工程手段制备表达特定蛋白的稳定细胞株,可以大量制备表达生物大分子(如蛋白质和核酸药物)的细胞膜囊泡。基于此,中山大学医学院张旭东副教授团队利用细胞膜囊泡递送PD-1单链抗体,并携载A2aR拮抗剂CPI-444,靶向PD-1阻止T细胞耗竭,用于肿瘤免疫治疗。
成果简介 中山大学医学院张旭东副教授团队报道了一种利用新型细胞膜囊泡抗体靶向活化T细胞的方法。利用基因工程改造小鼠巨噬细胞使其表达PD-1单链抗体,提取细胞膜制备细胞膜囊泡,同时装载A2aR拮抗剂CPI-444。PD-1单链抗体细胞膜囊泡在体外与T细胞上的PD-1结合,并可增强T细胞的活性。在荷瘤小鼠模型中,接受CPI-444-PD-1-scFv细胞膜囊泡治疗的小鼠,显著抑制了肿瘤的进展。通过对治疗小鼠的肿瘤组织的免疫细胞检测分析,CPI-444-PD-1-scFv细胞膜囊泡能够促进肿瘤特异性T细胞在肿瘤组织的富集,并显著增强CD8+T细胞的活性。活化的T细胞抑制肿瘤的生长,延长了小鼠的生存期。细胞膜囊泡抗体为靶向免疫细胞调节和肿瘤靶向治疗提供了新的思路。 图1. CPI-444-aPD-1-scFv细胞膜囊泡的制备及其用于肿瘤治疗的示意图 课题组简介 课题组介绍:张旭东现任中山大学医学院“百人计划”副教授,博士生导师,深圳市海外高层次人次。2015年获清华大学生命科学学院博士学位,2015~2018年在美国南加州大学、北卡大学教堂山分校、加州大学洛杉矶分校从事药物递送、癌症免疫治疗和糖尿病治疗相关研究。课题组在Advanced Materials, Nano Letters, ACS Nano, Biomaterials, Journal of Controlled Release, Nano Research ,Theranostics等国际著名学术期刊发表SCI论文30余篇。课题组获得了国家自然科学基金面上项目,广东省自然科学基金面上项目,深圳市优秀科技创新人才培养项目(优青项目),深圳市基础研究重点项目,中山大学青年教师重点培育等项目的资助。 课题组网站:http://zhangxdilab.com BioMed iLab-Zhang Group at Sun Yat-sen University。 文章信息 Tianyuan Xue, Zhirang Zhang, Tianliang Fang, Baoqi Li, Yuan Li, Liyan Li, Yanghua Jiang, Fangfang Duan, Fanqiang Meng*, Xin Liang* & Xudong Zhang*. Cellular vesicles expressing PD-1-blocking scFv reinvigorate T cell immunity against cancer. Nano Research https://doi.org/10.1007/s12274-022-4182-0. 识别二维码或点击左下角“阅读原文”可访问全文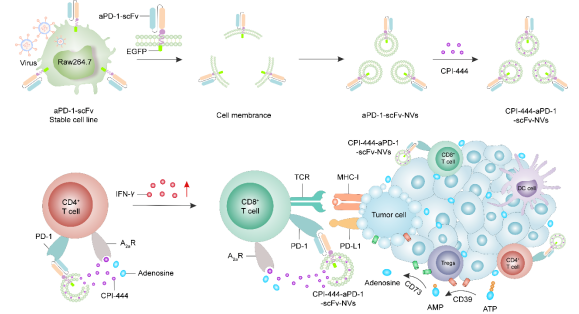


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号