南京大学黄硕团队ACS Sensors:纳米孔测序实现顺铂诱导DNA损伤的单分子准确识别
20世纪70年代,B. Rosenberg等人偶然发现铂电极的电解产物对大肠杆菌存在细胞毒性。随后,该过程的活性因子顺铂(cisplatin)被确定结构,并逐渐用于人睾丸癌和卵巢癌等癌症的治疗中,随即成为了20世纪无机化疗领域的里程碑级药物(图1a)。铂类药物的成功极大的催使了相关领域的蓬勃发展。早期的一些观念认为顺铂似乎会与细胞DNA非选择性的结合,然而最近的研究进展表明,由于核切除修复和组蛋白的稀缺性,顺铂病变在线粒体DNA中更为普遍。[1] 另外,对鸡红细胞核与非洲蛙(Xenopus borealis)5S rRNA基因的研究显示,顺铂偏好于对核小体间DNA连接区进行结合。[2] 毋容置疑,该结合结果会潜在影响铂类药物的化疗疗效,并有可能恶化癌症患者的生存预后。但若加以合理利用,也可以为设计定性靶标的铂类药物提供理论依据。
详细了解顺铂各类分子机制的前提是使用可靠的DNA测序方法准确识别顺铂损伤。现存报道可以利用第一代及第二代DNA测序技术通过成熟的工作流程识别位于DNA上的顺铂损伤。[3] 不过,这些测序技术固有地存在着如“需额外化学标记”、“需PCR扩增程序”和“无法排除其他DNA损伤干扰”等问题,这不仅使绘制基因组级别的顺铂损伤图谱费时费力,还可能产生遗漏及错读等问题。相比之下,被称为第三代测序技术的“纳米孔测序(nanopore sequencing)”则能通过低成本、无需化学标记及PCR扩增程序的途径直接读取待测核酸分子的物理化学性质,并成为解析DNA上顺铂损伤的理想技术。近日,南京大学化学化工学院仿生纳米技术课题组黄硕教授(点击查看介绍)团队通过纳米孔测序实现顺铂诱导DNA损伤的单分子准确识别。
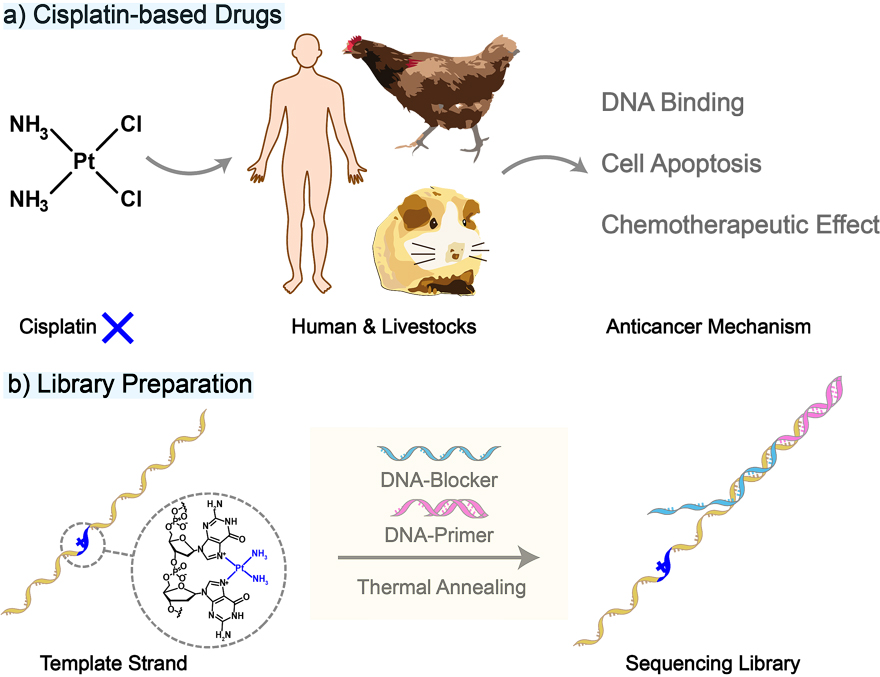
图1. 顺铂的作用机理及纳米孔测序文库的构建
作者团队首先利用耻垢分歧杆菌孔蛋白A(MspA)的静态传感实验(immobilization assay)作为纳米孔测序的概念验证(proof-of-concept)。结果表明,被固定在MspA孔道限制区域(constriction)内相差单个顺铂加合物的两条单链DNA可以引起高度可辨认的阻塞电流差异,这表明了通过纳米孔测序来识别顺铂损伤的可行性。随后,作者团队将单个顺铂损伤引入测序文库的模板链中(图1b),并利用先前报道的“酶棘轮策略(enzymatic ratcheting strategy)”[4] ,通过MspA成功构建了纳米孔测序平台(图2a)。实验中,含有顺铂损伤的测序文库的结果表现出令人惊奇的“高频噪音”特征(图2b,蓝色阴影),这是在先前纳米孔测序中从未被报道过的信号类型;进一步通过高通滤波(high-pass filter)处理后,该高频噪音信号几乎被完全保留,且能同其余核苷酸引发的电流平台产生极为清晰的区分(图2b);相比之下,先前工作中利用相似策略对DNA、RNA损伤的报道仅讨论了其低频信号改变,[5] 而该则结果表明了一种通过将纳米孔测序结果直接高通滤波处理以实现顺铂损伤特异性定位的简单方法。
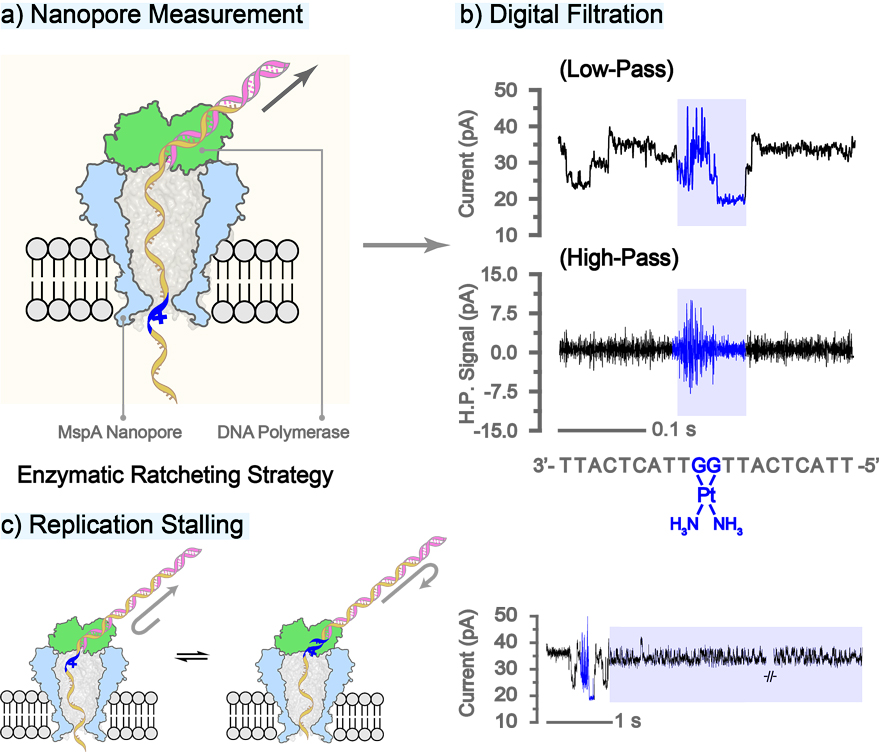
图2. 纳米孔测序中顺铂损伤引发的高频噪音及复制障碍
受益于纳米孔极强的时空分辨率,作者团队设想可以用该技术实现顺铂损伤-聚合酶相互作用的首次单分子观察。宏观研究显示,顺铂损伤会阻碍或逮捕处于前进状态的DNA或RNA聚合酶分子,并与多种机制共同引发细胞凋亡。[6] 纳米孔平台的观测结果表明,当顺铂损伤被棘轮化牵引至聚合酶的合成位点处时,其会阻挡聚合酶对模板序列的进一步牵引,并在纳米孔测量中表现出水平反复的电流平台切换(图2c)。进一步通过宏观凝胶电泳的观测同样印证了顺铂损伤对于聚合酶前进作用的阻碍。因此,作者团队相信纳米孔技术可以被用于定量研究铂类化疗药物的分子机制,并可用于启发新的化疗策略。
该工作发表在ACS Sensors 期刊。其中,南京大学化学化工学院硕士生马伏波为本文的第一作者,黄硕教授为论文的通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nanopore Sequencing Accurately Identifies the Cisplatin Adduct on DNA
Fubo Ma, Shuanghong Yan, Jinyue Zhang, Yu Wang, Liying Wang, Yuqin Wang, Shanyu Zhang, Xiaoyu Du, Panke Zhang, Hong-Yuan Chen, and Shuo Huang*
ACS Sens., 2021, DOI: 10.1021/acssensors.1c01212
导师介绍
黄硕
https://www.x-mol.com/university/faculty/56491
http://hysz.nju.edu.cn/bionano/
参考文献:
[1] a) Angew. Chem. Int. Ed., 2016, 55 (46), 14246-14249.; b) Angew. Chem. Int. Ed., 2019, 58 (14), 4638-4643.
[2] a) Biochim. Biophys. Acta, 1991, 1089 (3), 377-385.; b) Biochemistry, 2000, 39 (51), 16046–16055.
[3] a) J. Am. Chem. Soc., 1981, 103 (15), 4620-4622.; b) Proc. Natl. Acad. Sci. U. S. A., 2016, 113 (41), 11507-11512.
[4] Nat. Biotechnol., 2012, 30 (4), 349-353.
[5] a) J. Am. Chem. Soc., 2014, 136 (47), 16582-16587.; b) Angew. Chem. Int. Ed., 2019, 58 (25), 8432-8436.; c) Nat. Methods, 2017, 14 (4), 411-413.
[6] a) Proc. Natl. Acad. Sci. U. S. A., 1995, 92 (12), 5356-5360.; b) Nat. Struct. Mol. Biol., 2007, 14 (12), 1127-1133.
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号