Nano Today:杂合RNA拟病毒纳米粒子用于肿瘤免疫治疗
免疫疗法是肿瘤治疗领域最具前景的发展方向之一。虽然以T细胞为核心的免疫疗法对多种肿瘤有效,但是其总体响应率较低。近年来,通过外源性病毒RNA类似物激活肿瘤组织中的固有免疫应答的方法代表了一类很有潜力的抗癌策略。然而,肿瘤独特的代谢特征所创造的乏氧和微酸的肿瘤微环境会诱导细胞中感应外源性病毒RNA的信号分子陷入休眠状态,造成固有免疫不响应。近日,上海交通大学医学院公共卫生学院宋海云研究员(点击查看介绍)、化学化工学院樊春海院士(点击查看介绍)以及上海师范大学陈楠研究员(点击查看介绍)等人合作设计了一种杂合RNA拟病毒纳米粒子,通过平行地提供内源性逆转录病毒信号和外源性病毒信号引发协同性的固有免疫应答,利用装载RNA的纳米助推器的微环境重塑能力对免疫信号进行放大,并进一步诱导T细胞的活化和长期记忆,产生多层次、高效和长效的抗肿瘤免疫效应。
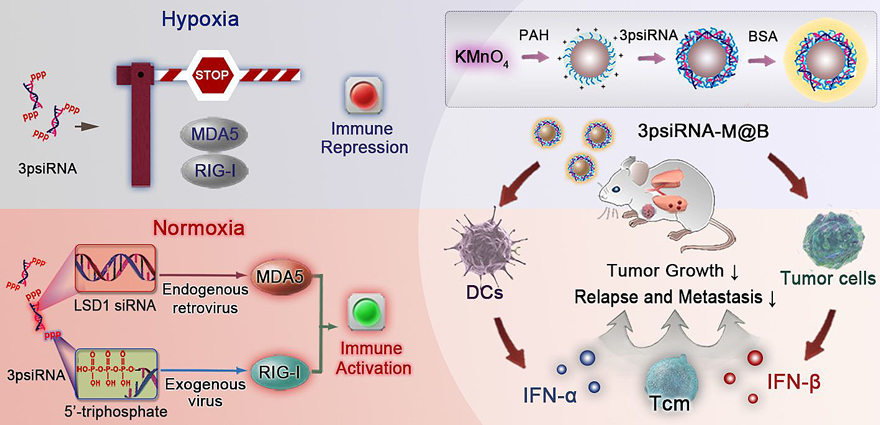
杂合RNA拟病毒纳米粒子的抗肿瘤机制。图片来源:Nano Today
拟病毒纳米粒子装载的杂合RNA分子传递了两类信号:中间序列为靶向组蛋白去甲基化酶LSD1的siRNA,能够诱导肿瘤细胞基因组中逆转录病毒元件的表达,形成内源性病毒RNA信号;两端的三磷酸序列模拟了外源性病毒RNA信号。两种RNA信号共同作用于模式识别受体MDA5和RIG-I信号通路,在促进I型干扰素表达、树突状细胞成熟和癌细胞凋亡方面表现出协同性的增效作用。而作为RNA载体的纳米推助器具有肿瘤微环境响应性,在递送杂合RNA分子进入细胞的同时,能够缓解乏氧和微酸性的肿瘤微环境,放大病毒RNA产生的免疫信号。
在小鼠肝癌及乳腺癌模型中,杂合RNA拟病毒纳米粒子通过激活固有免疫反应,能够促进CD8+细胞毒性T细胞活化和降低调节性T细胞活性,抑制肿瘤的发展进程。此外,在乳腺癌肿瘤切除模型中,杂合RNA拟病毒纳米粒子能够有效抑制肿瘤的术后复发及转移,并诱导中央记忆型T细胞的产生,促进机体形成长效的抗肿瘤免疫记忆。这项研究发展了一种借助双重拟病毒信号激活和放大抗肿瘤免疫反应的新策略,并且为肿瘤的联合治疗方针提供了新思路。
该成果近日发表于Nano Today,博士后刘唱和副研究员周炎烽为该论文的并列第一作者,宋海云研究员、樊春海院士和陈楠研究员为该论文的共同通讯作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Nanobooster-encapsulated hybrid RNA as anti-tumor viral mimicry
Chang Liu, Yanfeng Zhou, Xiaoyuan Ji, Hui Xie, Xingjie Hu, Min Yin, Nan Chen, Chunhai Fan, Haiyun Song
Nano Today, 2021, 38, 101211, DOI: 10.1016/j.nantod.2021.101211
导师介绍
宋海云
https://www.x-mol.com/university/faculty/270445
樊春海
https://www.x-mol.com/university/faculty/188467
陈楠
https://www.x-mol.com/university/faculty/143186
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号