室温下铁催化烯烃的Wacker型氧化
酮类化合物是一类重要的生物活性分子,不仅广泛存在于药物分子和天然产物中(图1),而且是有机合成和工业界的通用中间体。目前,合成酮的常用方法是钯催化的烯烃底物的氧化,也就是我们广为熟知的Wacker氧化法。尽管Wacker氧化自发现以来得到了广泛的应用,但是该反应需要催化量的贵金属钯催化剂和铜盐(氧化剂)。此外,该催化体系也存在一定的局限性,例如内烯和缺电子烯烃的氧化效率较低。然而,随着贵金属价格的剧烈波动以及绿色、可持续发展战略的推广,对于廉价金属(如地球储量丰富的第一过渡金属)在有机合成化学中的需求越来越强烈,如何将廉价金属代替贵金属已经成为一个热点话题。其中最重要的要数铁催化剂,这是因为铁化合物具有如下优势:地壳中的丰富度、可持续性、廉价、高反应性和低毒性。
2018年,德国德累斯顿工业大学的Hans-Joachim Knölker教授课题组在十六氟酞菁铁络合物(FePcF16)为催化剂、三乙基硅烷(Et3SiH)为添加剂、氧气为唯一氧化剂的条件下,实现了烯烃向酮的转化(Angew. Chem. Int. Ed., 2018, 57, 1222‒1226)。近日,他们利用简单易得的Fe(dbm)3或FeCl2(II)/neocuproine为催化剂、PhSiH3为还原性添加剂、空气为唯一氧化剂,实现了烯烃的Wacker型氧化。该反应不仅条件温和、操作简单、官能团耐受性好,而且所有反应均在室温下有效进行。相关成果于近期发表在Angew. Chem. Int. Ed. 上。

图1. 代表性的含酮活性化合物。图片来源:Angew. Chem. Int. Ed.
首先,作者选择2-乙烯基萘(1a)为模板底物,在PhSiH3为还原性添加剂、乙醇为溶剂、空气为氧化剂的条件下筛选了一系列铁催化剂(图2),发现Fe(acac)3仅能以低产率得到2-乙酰基萘(2a)。进一步,作者通过引入甲基、叔丁基和甲氧基,研究了芳基部分取代基对相应铁络合物催化活性的位阻和电性影响(图2)。结果显示当使用Fe(ba)3作为催化剂时,2a的收率显著提高(72%);当使用三(二苯甲酰甲基)铁(III) [Fe(dbm)3] 时,2a的收率高达79%,同时得到8%的醇3a;另外值得一提的是,将催化剂负载量从10 mol%降低到3 mol%时,2a的收率几乎没变化。此外,催化剂Fe(dbm)3还可以用于克级规模合成,1a(6.5 mmol)在标准条件下反应5 h,便能得到80%的2-乙酰基萘(2a)和11%的醇3a。对照实验表明,在不存在Fe(dbm)3或PhSiH3或空气的情况下,反应无法进行。
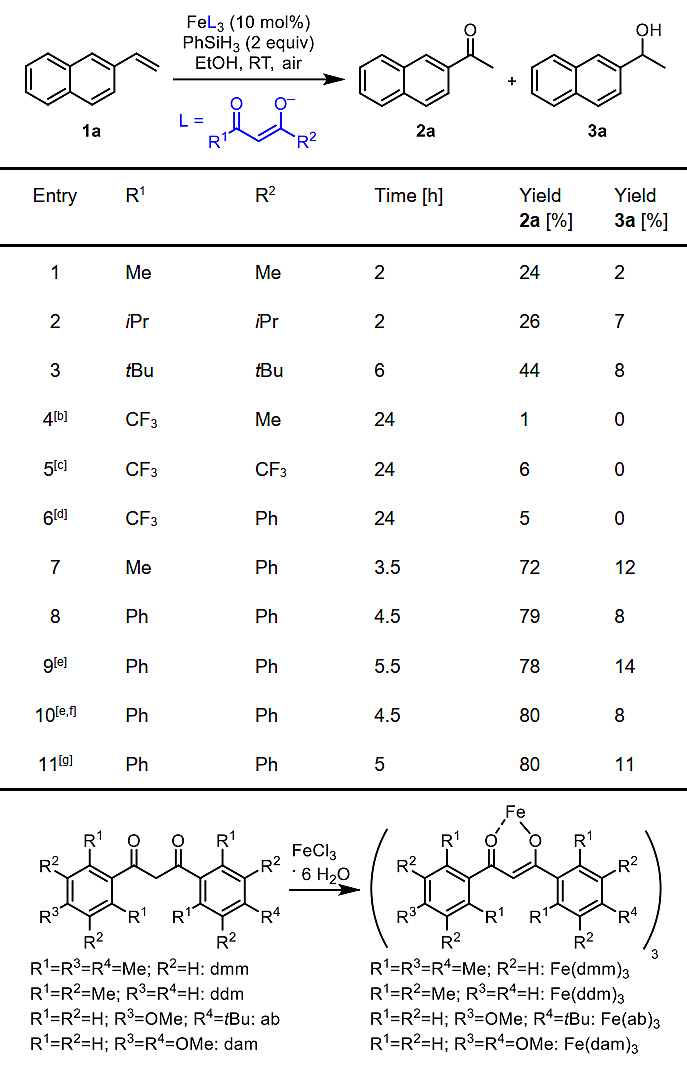
图2. 配体筛选及铁(III)络合物的合成。图片来源:Angew. Chem. Int. Ed.
接着,作者在其它条件不变的情况下研究了一系列简单铁化合物的催化活性(图3),结果显示氯化铁(II)或氯化铁(III)盐和简单易得的离子液体[bmim][FeCl4]能以中等的产率(59‒69%)得到2a,而其它铁化合物的效率则较低。为了避免底物1a的分解,作者选择FeCl2为催化剂筛选了各种配体,发现neocuproine的效果最好。当1a在FeCl2/neupuproine(各3 mol%)、PhSiH3(2当量)和乙醇的反应条件下于室温进行反应时,能以76%的收率得到2a。此外,该反应条件还能用于克级规模合成,从2-乙烯基萘(1.0 g,6.5 mmol)出发,以83%的收率得到了2-乙酰基萘(2a)。
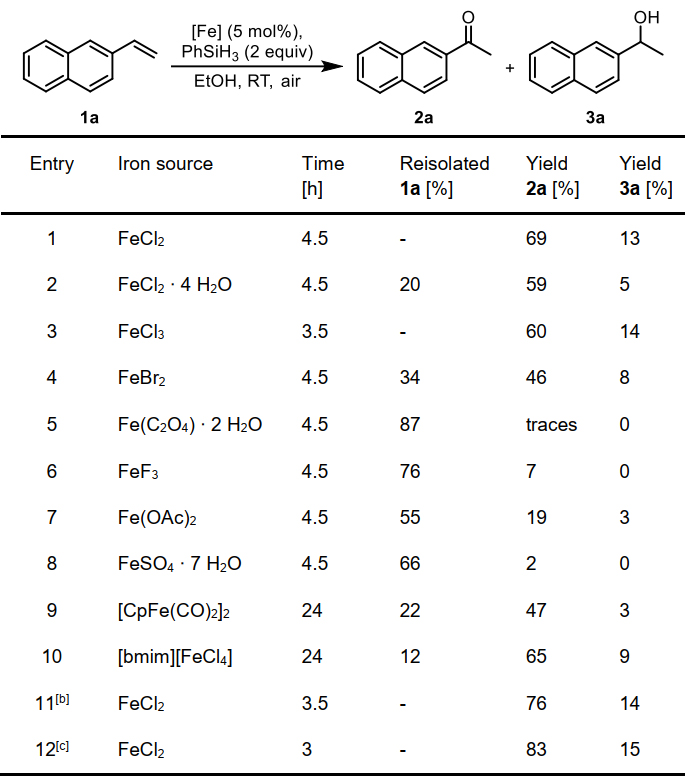
图3. 反应条件优化。图片来源:Angew. Chem. Int. Ed.
在两组优化条件下(method A :Fe(dbm)3(3 mol%);method B:FeCl2/neocuproine(各3 mol%)),作者考察了该反应的底物范围。此外,为了显示neocuproine配体对铁催化的作用,作者还尝试单独使用FeCl2(3 mol%)为催化剂(method C),并发现neocuproine配体可以缩短反应时间、减少底物分解,这归因于配体加速的催化(ligand-accelerated catalysis)。如图4所示,一系列末端苯乙烯衍生物(1a‒1f)都能够有效地转化为相应的芳基甲基酮(2a‒2f),不仅收率高达97%,而且醇(3a-3f)是唯一的副产物。类似地,非末端苯乙烯衍生物(1g-1j)和色烯(1k和1l)也能兼容该反应,以较好的收率(74-87%)得到相应的苄基酮(2g-2l),其中底物1h在Fe(ba)3的催化下效果更好。值得一提的是,即使提高催化剂负载量(3 mol%→10 mol%)并且延长反应时间(48 h),底物1j的转化率仍很低(收率:35%,原料剩余:49%)。然而,当使用三(苯甲酰丙酮基)铁(III)(3 mol%)为催化剂时,反应6.5 h后便能以81%的收率提供产物2j,且没有副产物醇3j。脂肪族端烯或内部烯烃(1m-1o)也能实现这一转化,以中等的收率(35-62%)得到相应的酮(2m-2o),不过,副产物醇(3m-3o)的比例却有多增加(14-47%)。亚氨基芪1p在Fe(dbm)3的催化下反应非常缓慢,但是当使用Fe(ba)3(3 mol%)为催化剂时,能以70%的收率获得2p,后者是抗癫痫药奥卡西平的合成前体。最后,作者证明了该方法对天然产物合成的适用性。在method A下,吉九里香碱(1q)能以54%的收率转化为天然产物euchrestifoline(2q),同时得到43%的醇(3q),而在method B和method C下反应却无法进行。
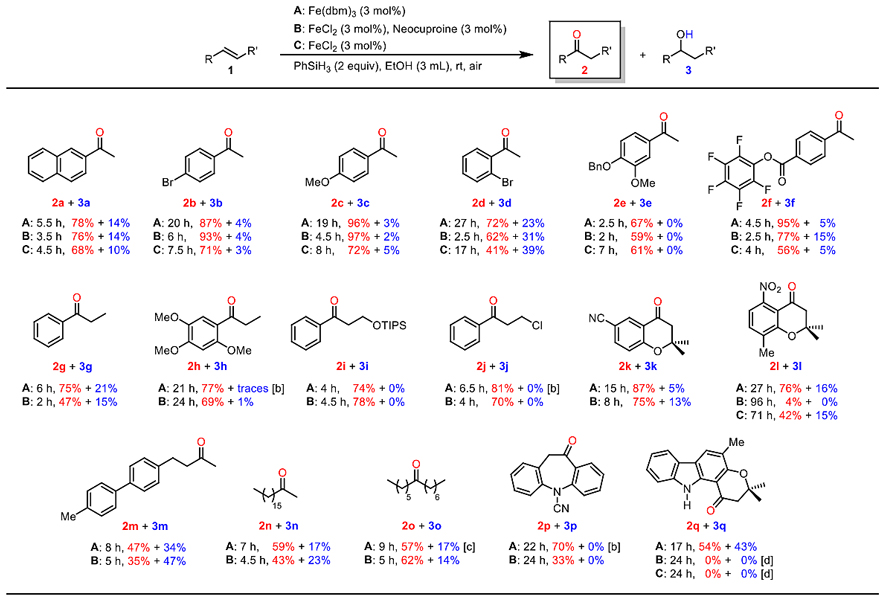
图4. 底物范围。图片来源:Angew. Chem. Int. Ed.
为了进一步研究反应机理,作者进行了一系列机理实验。当1a在全氘代乙醇(EtOD-[D5])中进行反应时,产物中并未掺入氘;当使用PhSiD3为还原性添加剂时,酮2a和醇3a中的甲基氘代率为97%。此外,在氩气气氛下进行反应并没有形成产物;而在18O2气氛下进行反应时,method A下两种产品的18O掺入率为92%,而method B下掺入率为95%,证实了酮和醇中的氧原子均来自空气。当使用α-位氘代的2-乙烯基萘(1a-[α-D1],92% D)进行反应时,得到了未标记的酮2a和苄位氘代的3a-[α-D1](92% D),这表明醇3a不是通过铁催化酮2a的还原形成的。鉴于底物在TEMPO(2当量)存在下进行反应时并未生成任何产物,因此作者提出了铁催化的Wacker型氧化的自由基机理。如图5所示,FeIIIX3与乙醇进行配体交换生成X2FeIII-OEt,后者与PhSiH3反应生成X2FeIII-H物种和PhSiH2(OEt)。接着,X2FeIII-H与烯烃进行氢原子转移(HAT)生成碳自由基和FeIIX2物种,它们与Fe (III)-烷基络合物处于平衡状态,后者也可以通过将烯烃直接插入X2FeIII-H中(加氢金属化)得到。随后,Fe (III)-烷基络合物捕获O2生成Fe (III)-过氧烷基络合物,接着经O-O键断裂和C-H键断裂便可得到酮和X2FeIII-OH,后者与乙醇反应便可再生X2FeIII-OEt;或者与PhSiH3进行转金属化得到X2FeIII-H物种和副产物苯甲硅烷醇;或者将羟基自由基转移至烷基自由基得到副产物醇。另外,通过中间体Fe (III)-过氧烷基络合物与PhSiH3的金属交换进行的Mukaiyama水合反应也可产生X2FeIII-H物种和甲硅烷基过氧烷基化合物,后者经重排、与乙醇反应也能产生醇。
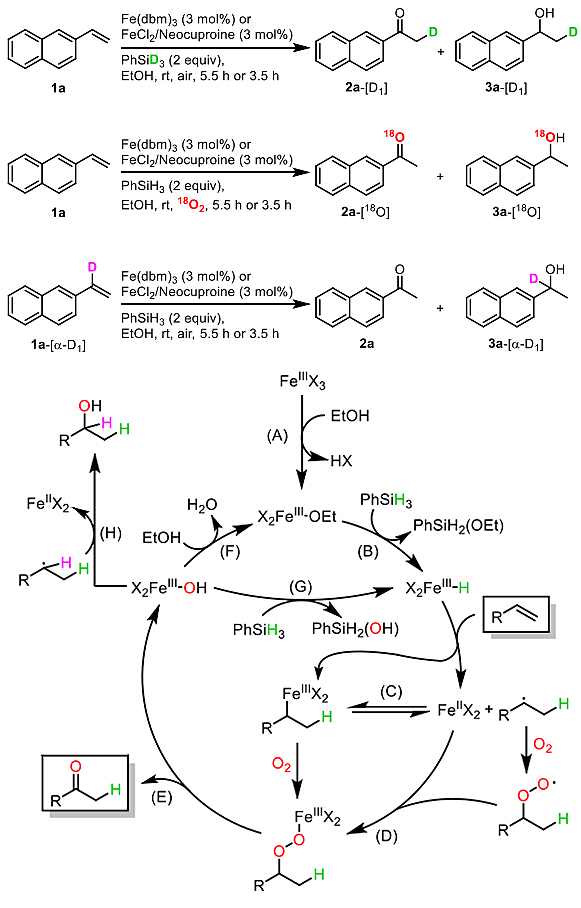
图5. 相关实验及可能的机理。图片来源:Angew. Chem. Int. Ed.
总结
Hans-Joachim Knölker教授课题组开发了两种方案,即使用苯基硅烷(PhSiH3)为还原性添加剂和简单易得的Fe(dbm)3或FeCl2(II)/neocuproine为催化剂,实现了烯烃的Wacker型氧化。这两种方案均在室温下进行,并且仅需要空气作为唯一氧化剂。标记实验表明氢硅烷添加剂是末端碳原子上其它氢原子的来源,而空气中的氧是羰基的来源。可以预见,该方法将用于生物活性化合物和天然产物的合成。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Iron-Catalyzed Wacker-type Oxidation of Olefins at RoomTemperature with 1,3-Diketones or Neocuproine as Ligands
Florian Puls, Philipp Linke, Olga Kataeva, Hans-Joachim Knölker
Angew. Chem. Int. Ed., 2021, DOI: 10.1002/anie.202103222
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号