Angew:仿生双铜体系引发的蛋白质巯基亚硝基化反应
非正常的蛋白质巯基亚硝基化反应会引发蛋白质的错误折叠,进而导致一些神经退行性疾病,比如阿尔茨海默症、帕金森症。理解生物体内酶的金属活性中心是如何参与和引发蛋白质的巯基亚硝基化反应是这个领域的核心难题,对相关疾病的治疗也会非常重要。已有的生物化学和仿生无机化学工作表明包含多铜活性中心的血浆铜蓝蛋白可以催化巯基亚硝基化反应,表明多铜活性中心很可能对此反应有重要影响。近日,俄亥俄州立大学的张世誉教授课题组发现了双铜体系引发的氧化还原中性的巯基亚硝基化反应。这一新颖的反应途径可以帮助理解血浆铜蓝蛋白催化的巯基亚硝基化反应的生活活性。

以苯乙硫醇作为模板底物,作者对双铜引发的巯基亚硝基化反应进行了研究。一价态的双铜配合物1与过量的一氧化氮在低温下反应生成了中间体2,此中间体的桥连氧原子可以与两当量的苯乙硫醇发生酸碱中和反应,生成的铜硫醇盐与过量一氧化氮反应最终生成中间体3。对照试验发现中间体3的紫外可见光谱与双铜配合物1和两当量亚硝基苯乙硫醇的反应产物相同。
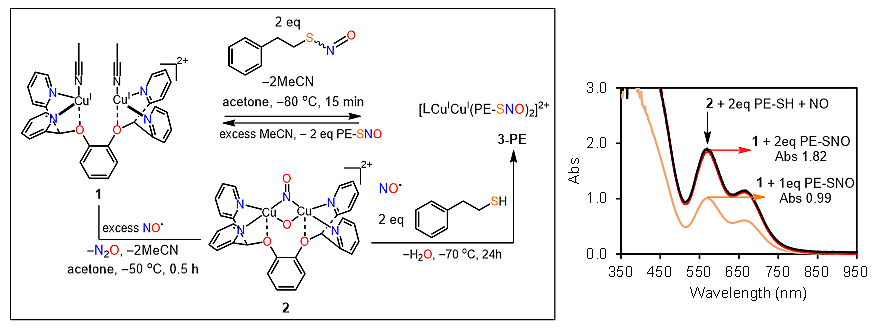
过量的乙腈在低温下可以与中间体3反应释放两当量的亚硝基苯乙硫醇和双铜配合物1。通过低温的氢谱和15氮谱核磁实验、原位红外实验以及DFT理论计算,中间体3的具体配位结构得到了确认。
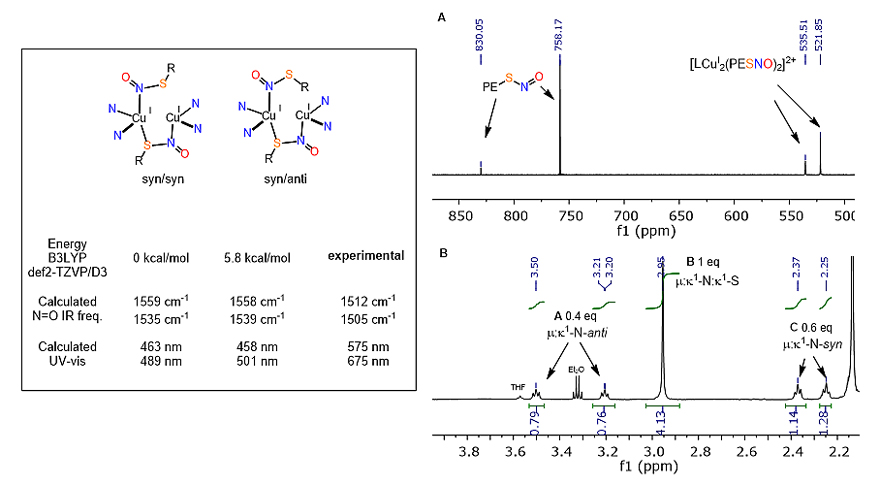
在该工作中,作者首次发现仿生的双铜体系可以通过中间体2引发氧化还原中性的巯基亚硝基化反应,这一反应途径可以作为仿生模拟体系较好地解释血浆铜蓝蛋白催化的生物活性。发展催化的体系以及其他活性中间体的研究会是下一步工作的方向。

论文发表于Angew. Chem. Int. Ed.,文章的第一作者是博士后陶闻杰,通讯作者是张世誉教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Redox‐neutral S‐nitrosation Mediated by a Dicopper Center
Wenjie Tao, Curtis E. Moore, Shiyu Zhang
Angew. Chem. Int. Ed., 2021, DOI: 10.1002/anie.202102589
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号