刘国生团队Nat Catal:钯催化非活性端烯的不对称双乙酰氧化反应
光学纯1,2-二醇是一类重要的有机结构单元,不仅广泛存在于天然产物和药物分子中,而且是一类非常有价值的有机合成砌块。目前,制备这类化合物的主要方法之一是烯烃的不对称双羟基化反应,并且已经取得了许多里程碑式的研究进展,例如Sharpless发展的锇/金鸡纳碱衍生物催化的顺式不对称双羟基化反应,除此之外,其它过渡金属(如Ru、Mn、Fe)也成功用于顺式邻二醇的合成(图1a)。类似地,关于反式不对称双羟基化反应也有大量研究,即先进行不对称环氧化再开环(图1b)。纵观这些反应,多取代烯烃是主要研究对象,相比之下,针对端烯尤其是单取代的非活性端烯的研究却相对较少,例如位阻很小的丙烯和1-丁烯,用目前已知的方法得到的1,2-二醇仅具有中等的对映选择性。同时,简单烯烃(如C3-C10)是非常重要的基础化工产品,其高附加值转化具有非常重要的意义。
尽管消旋的钯催化烯烃双乙酰氧化反应早有报道(J. Am. Chem. Soc., 2008, 130, 2962),但后来的研究证实该类反应是高活性的阳离子钯催化剂由于其强路易斯酸性能活化PhI(OAc)2而引发的三价碘参与的反应(J. Am. Chem. Soc., 2011, 133, 3658)。由于此强背景反应的困扰,钯催化烯烃的不对称双乙酰氧化反应研究一直没有进展。中国科学院上海有机化学研究所刘国生(点击查看介绍)课题组通过对手性吡啶-噁唑啉配体(Pyox)进行修饰,完美地解决了这个问题:在Pyox配体中的吡啶C-6位引入一个位阻适中的基团来提高中性Pd(OAc)2的催化活性,实现烯烃的分子间氧钯化过程,从而避免阳离子钯的使用,消除了三价碘的背景反应;Pyox中手性噁唑啉可以实现反应的对映选择性控制。近日,他们报道了Pd(II)催化的端烯的不对称双乙酰氧化反应(图1c),底物就包括极具挑战性的丙烯和1-丁烯。与先前报道不同的是,该反应的启动步是不对称氧钯化,对手性吡啶恶唑啉类配体(Pyox)的修饰能够促进这一过程。此外,该催化体系不仅官能团耐受性好,而且对单取代的端烯具有非常显著和专一的识别能力。相关结果发表在Nature Catalysis 上,第一作者是中科院上海有机所博士后田兵,通讯作者为中科院上海有机所刘国生研究员。
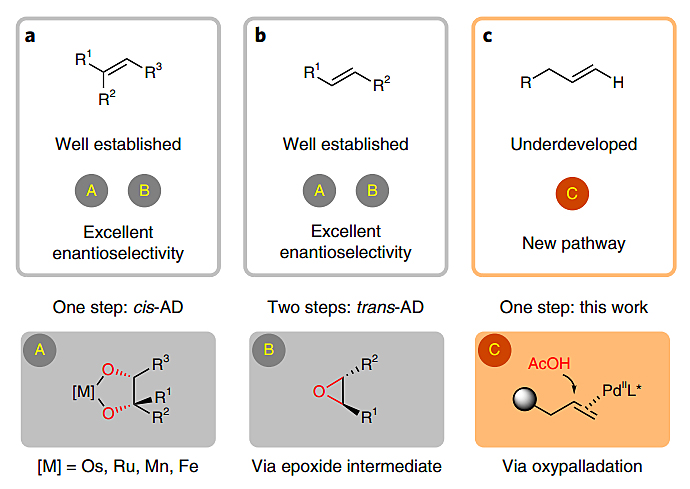
图1.烯烃的不对称双氧化反应。图片来源:Nat. Catal.
首先,作者选取1a作为模板底物,在Pd(OAc)2为催化剂、PhI(OAc)2为氧化剂的条件下进行反应(图2b),没有监测到双乙酰基化产物2。然后,作者向体系中加入Pyox类配体,发现L3无效,但L1和L2有催化效果,并且在L2的催化下,反应能有81%的收率和72%的ee值。对反应条件进一步优化后,发现在乙醚作为溶剂和2.5当量醋酸存在的条件下,对映选择性能提高到88%。对配体的进一步筛选表明L4(Et)、L5(nPr)、L7(CH2Cy)(91-92%ee)的对映选择性要优于L2(图2c、2d),而L6(iPr)、L8(Bn)(89%和85%ee)和L2相当。值得注意的是,当吡啶环上带有位阻适中的取代基时(L4和L5),反应活性更好(> 80%收率)。对照实验表明没有醋酸,反应不会发生,这表明醋酸对氧钯化启动至关重要。而且反应只有在Pyox配体存在的情况下才会发生,这进一步证实了作者提出的有关配体加速效应的假设。
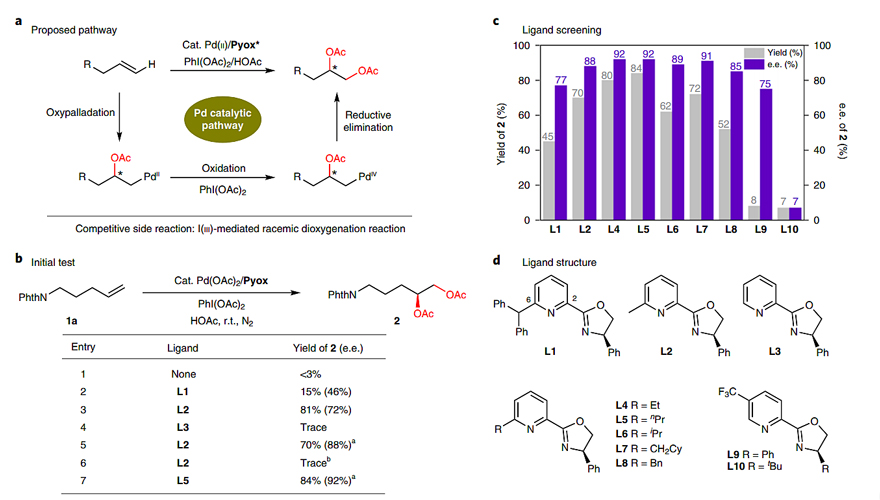
图2.Pd/Pyox催化烯烃的不对称双乙酰氧化反应。图片来源:Nat. Catal.
在最佳反应条件下,作者开始了底物普适性的研究(图3)。首先考察的是结构最简单但是反应难度最大的丙烯和1-丁烯,结果显示双乙酰氧化产物3和4都具有优异的对映选择性(94%和95% ee),证实了该手性钯催化剂对简单双键的潜手性面识别具有极好的控制力。其它简单烯烃(如1-戊烯、1-己烯等)都能以不错的收率和优秀的对映选择性(90–93% ee)完成转化。值得一提的是,该反应还能够耐受多种官能团,如卤素(12-14)、烯丙基醚(15)、烯丙基酯(16)、醇(17)、羧酸(18)、磺酸酯(19)、硅醚(20)、N-Ts烯丙胺(21)、酰亚胺(2和22)、氰基(23)、硝基(24)、苯磺酰基(25)、羧酸酯(26)、芳基卤化物(27和28)、芳基硼酸(29)、芳基醛(30)以及杂环化合物(32-36),且能以中等到优秀的收率(42–86%)和优异的对映选择性(87–95% ee.)实现这一转化,特别是2还能以克级规模进行。此外,双烯(37)类、烯炔类(38)以及衍生自复杂分子(39-46)的底物参与反应时,均表现出专一的化学选择性(即反应都专一地发生在单取代非活性双键上),以良好的收率(46–86%)和优秀的对映选择性(89–94% ee 或de)得到目标产物。
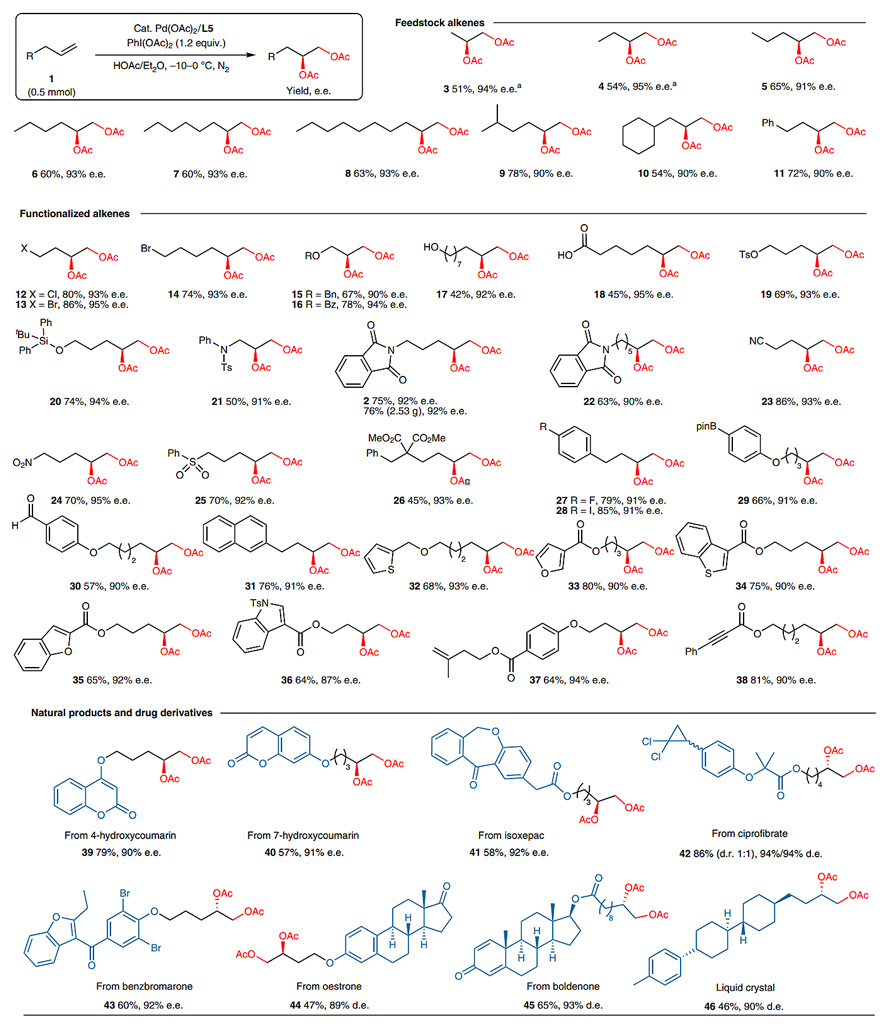
图3.底物范围研究。图片来源:Nat. Catal.
在锇催化的非活化烯烃的不对称双羟基化反应中,电子效应对化学选择性的影响胜过位阻效应。相反,本文中钯催化的不对称双乙酰氧化反应只受位阻影响(图4a)。例如多烯(47)在Sharpless反应条件下会以5:1的区域选择性得到一对混合物(48'和49'),而在本篇报道的钯催化条件下,反应只会发生在位阻较小的末端双键上,以72%的收率和92%的ee值得到产物49。再比如更复杂的多烯分子50,其反应结果也类似。若采用Sharpless条件,反应会得到51'和52'(2.2:1 r.r.)的混合物;如若采用钯催化条件,则会得到单一的产物52(收率:66%,ee 值:93%)。此外,分别带有富电子和吸电子苯乙烯基团的端烯底物53和56,在Sharpless的不对称双羟基化反应体系下,会得到相应的二醇54'和57';而在钯催化的不对称双乙酰基化反应中,则得到55和58(92%-93%ee)。两者的区别在于前者是苯乙烯中的乙烯基参与反应,后者则是端烯参与反应。这些结果表明本文发展的钯催化不对称双乙酰氧化化反应能够实现优秀的化学选择性和对映选择性,与锇催化的sharpless不对称双羟基化反应形成互补。
除此之外,携带两个端烯基的底物同样能顺利发生反应,以优异的对映选择性直接高效地得到四醇类化合物(图4b)。从简单易得的1,5-己二烯(59)出发,可以80%的收率、98% ee值得到四酯类化合物(60),后者能以95%的收率转化成(2S,5S)-1,2,5,6-四醇60'(手性膦配体61和四氢吡咯类化合物62的重要前体)。药效基团SPIKET-P(65)对癌细胞具有有效的细胞毒性,可从二烯63出发经三步转化而来,其中钯催化的不对称双乙酰基化反应直接合成四酯类化合物(64)是关键步(收率:65%,ee 值:94%),而先前的方法则需从环氧化物(66)出发经11步合成。此外,简单的二烯(67)能以58%的收率和95%的ee 值转化成四酯(68)。值得一提的是,将本文发展的钯催化不对称双乙酰基化反应和水解反应一锅法进行,便可以克级规模制备有机合成中有价值的手性1,2-二醇(图4c)。例如二氢醉椒素和抗青光眼药物拉坦前列素的合成中间体1,2-二醇-(S)-11'就能用该方法高效合成,而先前的方法则通过L-苹果酸和D-甘露醇来合成。二醇(S)-11'还能经过各种官能团化得到手性叠氮醇(69和70)、环氧化物(71)和脂肪族二级醇(72)。不仅如此,作者又将(R)-11'转化成化合物73,后者是制备血管紧张素转换酶抑制剂盐酸贝那普利74的关键中间体。类似地,重要的合成中间体内酯77也能从市售的烯烃75反应得到(收率:85%,ee 值:91%)。

图4.多烯的反应研究以及手性1,2-双醋酸酯的合成应用。图片来源:Nat. Catal.
为了深入了解反应机制,作者从该反应的立体化学着手研究(图5)。如图5a所示,氘代底物E-1a-d1在标准条件下进行反应时,会高对映选择性地得到一对异构体(threo-2-d1和erythro-2-d1)。随着反应时间的延长,两种异构体的比例会下降。当反应8h后,2的收率是18%且非对映选择性较好(threo-2-d1:erythro-2-d1> 20:1)。反应48h后,2的收率达到71%但非对映选择性下降(threo-2-d1:erythro-2-d1=7:1)。关于threo-2-d1的生成有两条可能的路径(图5c)。其一是cis-氧钯化过程先启动反应,接着int-I被氧化为Pd(IV)物种int-II,后者直接还原消除生成syn-1,2-二乙酰基产物。其二是反应经历trans-氧钯化过程,并伴随Pd(IV)物种int-IV的SN2消除。
有趣的是,向trans-1a-d1的反应体系中加入一当量水时,反应会以17%的收率和93% ee值(dr>20:1)得到threo-2-d1。,其主要产物是1:1的threo-78-d1和threo-79-d1(图5b)。将这对单乙酰基保护的双醇混合物酯化后,能以76%的收率和81%的ee值(dr=20:1)得到单一的异构体threo-2-d1。这些结果表明手性纯的threo-78-d1和threo-79-d1是由以下反应路径得到的:Pd(IV)物种int-IV先发生分子内乙酰基对邻位碳的SN2亲核进攻(图5c,path b),生成的环状中间体int-V再水解(图5c,path c)。或者Pd(IV)物种int-IV进行SN2还原消除后也会生成threo-2-d1(图5c,path a)。因此反应初期观察到的高非对映选择性揭示了该反应遵从的路径是先trans-氧钯化再SN2还原消除。而非对映选择性随着时间延长逐渐下降的可能原因是中间体int-V会发生SN2开环形成erythro-2-d1(图5c,path d),而不是直接还原消除。相反,当体系中有水时,环状中间体int-V会很快水解(图5c, k3> k2),从而促使了threo-78-d1和threo-79-d1的生成(图5b)。另外,尽管水的用量比醋酸少,但反应的时间进程表明78/79的生成速率远快于2的生成速率(图5d)。这些数据说明烷基-Pd(IV)物种int-IV倾向于经历先还原消除成环(图5c,pathb)再水解(图5c,pathc)的路径生成78/79,而不是通过SN2还原消除生成2(图5c,k3>k1)。图5a中主要生成了threo-2-d1表明该反应中烷基-Pd(IV)物种int-IV的还原消除比int-V的开环速率快(k1> k2)。需要指出的是,反应中观察到显著的水效应。增加水的用量能够加快78/79的生成速率(图5e),这说明int-V的水解可能是图5b中 1a反应的决速步。此外,基于Pd(IV)物种int-IV的SN2还原消除速率比水解速率慢这一事实,作者认为Pd(IV)物种int-IV的SN2还原消除是不对称双乙酰氧化反应的决速步,这也能解释配体效应(L5>L7>L1,图5f)。再者,使用L1时,醋酸参与的SN2亲核进攻相比于L5更难,所以大位阻配体会减慢反应速率(图5g)。

图5.反应机制研究。图片来源:Nat. Catal.
总结
上海有机所刘国生研究员团队发展了Pd(II)催化的非活性端烯的不对称双乙酰氧化反应。该反应具有优异的对映选择性(typically> 90% ee)、宽广的底物普适性、极好的官能团耐受性以及专一的化学选择性,可快速高效地实现各种手性1,2-二醇的大量制备。作者通过配体的精心设计,底物的细致考察以及深入的机理研究,使反应更加全面详实,既富有科学意义又具备实用价值。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Palladium-catalysed enantioselective diacetoxylation of terminal alkenes
Bing Tian, Pinhong Chen, XuebingLeng, Guosheng Liu
Nat.Catal., 2021, 4, 172–179, DOI:10.1038/s41929-021-00574-5
导师介绍
刘国生
https://www.x-mol.com/university/faculty/15593
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号