深圳大学张学记教授团队近年来代表性工作概览
张学记教授,深圳大学副校长,党委常委,北京精准医疗与健康研究院执行院长,中国生物检测监测产业技术创新战略联盟理事长、俄罗斯工程院外籍院士,美国医学与生物工程院院士,英国皇家化学学会会士,欧洲科学院院士,东京大学特聘教授,301医院临床生化部副主任,中组部国家人才评审巡察小组组长。近年来,主持国家重点研发计划,重点仪器研发专项,中国自然科学基金等多项研究课题。已在重要国际刊物Chem. Rev., J. Am. Chem. Soc., Adv. Mater., ACS Nano,Chem. Sci., Anal. Chem等发表论文500余篇,获得专利100余项,分别在Elsevier、Springer、科学出版社出版中英文专著8部。已有30余项技术产业化,创建了10个高科技公司,产品在全球100多个国家得到广泛应用。获首届全国创新争先奖,获首都劳动奖章;教育部高等学校自然科学二等奖、中国分析测试协会(CAIA)一等奖,国务院特殊贡献专家,当选科学中国人年度人物。现任Am. J. Biomed. Sci.主编,Front. Biosci.副主编,Archi. Med. Sci.副主编及Biosens. Bioelectron.等24个国际期刊编委。

张学记教授。图片来源:深圳大学官网
张学记教授团队长期从事生物传感及仪器与诊疗研究,在分析化学领域取得了系统性创新成果。他的研究引领并推动了生物传感及仪器与诊疗技术的发展。本文将重点介绍近年张学记教授课题组的一些有代表性的工作。
(一)肿瘤标志物高效检测新方法
围绕疾病精准早期诊断方法及仪器开发的研究,该团队以肿瘤miRNA标志物高效检测新方法及癌症疗效评估为目标,在体外、细胞及活体层面的核酸传感分子识别、信号放大与传感新策略研究中取得了系列成果。
1. 肿瘤miRNA标志物检测(图1)
利用氧化石墨烯纳米材料作为淬灭剂,结合链置换信号放大策略,张学记教授团队发展了体外高灵敏、多元miRNA检测方法(Anal. Chem., 2012, 84, 4587)。设计了一种DNA“纳米车轮”结构,实现对胞内肿瘤miRNA“一对多”的荧光信号放大检测(Anal. Chem., 2019, 91, 9828)。开发了基于DNA水凝胶热可逆和毛细作用原理的毛细管凝胶膜制备方法,实现了对目标生物分子的高灵敏、高选择的定量分析(Nat. Commun., 2019, 10, 1036)。将肿瘤成像和miRNA标志物分子检测相结合,实现了活体层面对肿瘤的精确诊断(Adv. Funct. Mater., 2017, 27, 1605592)。受邀在Chem. Rev.撰写首篇miRNA检测相关综述文章,出版miRNA检测专著2本,肿瘤miRNA精准诊断方法的系列研究成果在国内外产生广泛影响。
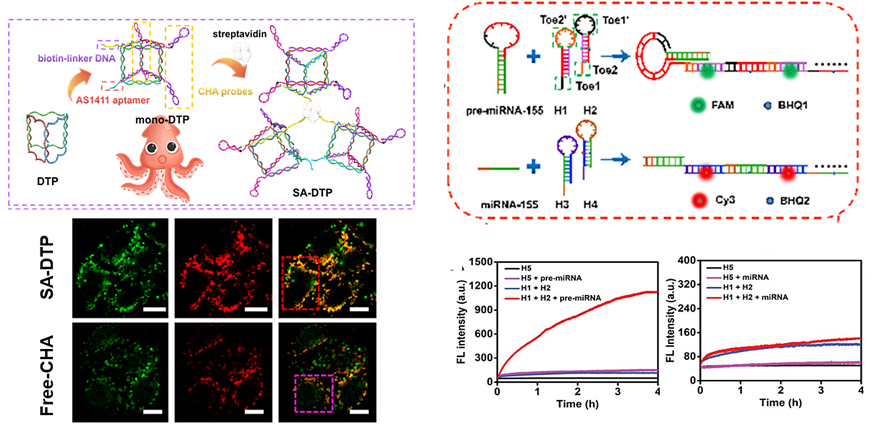
图1, 肿瘤miRNA标志物高效检测新方法
2. 金簇传感分析
该团队研究了纳米金簇的修饰及固定化,发展了一种纳米金簇荧光薄膜传感器的制备方法,用于铜离子的测定(Biosens. Bioelectron., 2013, 4, 16)。研究了半胱胺、半胱氨酸和谷胱甘肽对纳米金簇的刻蚀作用,发现半胱氨酸和谷胱甘肽能够一定程度地增强纳米金簇的荧光发射(Biosens. Bioelectron., 2015, 66, 155)。利用半胱胺刻蚀纳米金簇的方法制备了不含金核的配体壳,研究了纳米金簇合成过程中其配体壳的结构变化(J. Phys. Chem. C, 2015, 119, 12065)。TCEP刻蚀纳米金簇的反应可以用于发展比率型的荧光检测TCEP的方法 (Anal. Chem., 2016, 88, 11193)。将纳米金簇的刻蚀化学延伸到聚集诱导发光(AIE)效应领域的研究,并实现铜离子的可视化高灵敏检测(Anal. Chem., 2016, 88, 6071),以及高灵敏半胱胺酸检测(Nanoscale, 2019, 11, 294),并设计了一种具有AIE性能的pH响应型金(I)-二硫化物纳米粒子(NPs)用于对胃酸进行监测(Chem. Sci., 2020, 11, 6472),还制备了AIE活性的Au(I)-半胱氨酸纳米复合物用于Fe3+的检测(Anal. Chem., 2020, 92, 6785)。
(二)即时快速检测技术
以快速即时检测为目的,张学记教授团队结合层析技术、界面技术以及可穿戴技术发展了多种生物分子即时检测新方法。
1. 层析快速传感
在开发侧流层析传感器与传感新策略研究方面,该团队结合侧流层析传感器的便利性、Y形DNA探针的设计灵活性以及核酸内切酶辅助靶标循环扩增的增强能力,开发了一种简单快速的microRNA检测策略(Anal. Bioanal. Chem., 2016, 408, 8195)并利用磁场富集目标物后快速、灵敏的检测血液中兔IgG(Anal. Chim. Acta, 2017, 993, 79)、胰腺癌标志物蛋白碳水化合物抗原19–9(Microchim. Acta., 2017, 184, 4287)。基于三螺旋DNA(THD)功能化的碳纳米管(CNT)上和目标诱导的分子开关,开发了快速可视同时检测核酸和蛋白质的侧流层析核酸生物传感器(Chem. Commun., 2020, 56, 13657)。将超声富集作为一种样品预处理方法,与侧流层析传感器集成在一起,开发了一种快速通用的血液中蛋白质检测平台(Anal. Chem., 2021, 93, 2996)。发表侧流层析传感器综述文章(Microchim. Acta., 2020, 187, 70)。
2. 界面生物传感
开发出一种超亲水和超疏水界面的即时检测平台(图2),在超亲水的孔里实现了对金属离子的比色检测(ACS Nano, 2017, 11, 621),并开发了一种可重复利用的亲疏水芯片(Sens. Actuator B Chem., 2018, 258, 715),多信号输出的超浸润芯片(Chem. Commun., 2019, 55, 1742),可便携穿戴胶带超浸润传感器用于原位的重金属离子检测(Anal. Chem., 2018, 90, 14105)以及核酸和蛋白质(ACS Sens., 2018, 3, 72;Nanoscale, 2018, 10, 20990)等。制备了微柱阵列,实现智能高通量分析和合成(Talanta, 2020, 218, 121206; Biosens. Bioelectron., 2020, 149, 111845; Biosens. Bioelectron., 2020, 162, 112253; Adv. Funct. Mater., 2020, 30, 1910329; Nanoscale, 2021, 13, 739),并撰写综述文章“Bioinspired superwettable micropatterns for biosensing”,详细阐述了超浸润界面分析方法的实际应用(Chem. Soc. Rev., 2019, 48, 3153)。
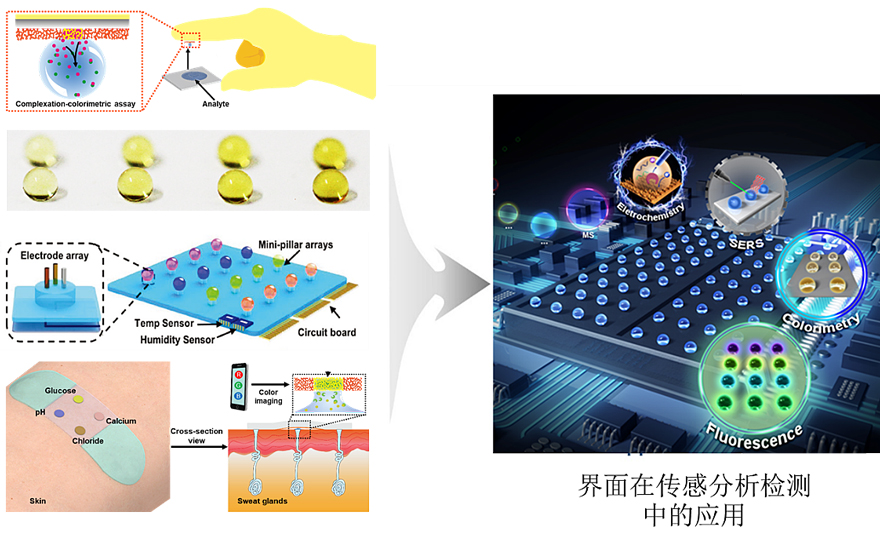
图2. 界面分析传感
3. 可穿戴传感
在可穿戴领域取得一系列进展,制备了超浸润微阵列,为汗液的收集提供了精确的采集位点,通过与智能手机结合实现了汗液的即时分析和定量检测(Anal. Chem., 2019, 91, 4296; ACS Sens., 2020, 5, 1548-1554;Talanta, 2020, 212, 120801),该类工作受到了ACS Weekly PressPac, Phys.org, ScienceDaily等杂志的亮点报道。此外还开发了超拉伸的导电石墨烯纤维用于应力传感(Nano Lett., 2019, 19, 6592)和自感应和自冷却集成智能服装(ACS Nano, 2020, 14, 559-567)。并撰写智能传感综述文章Artificial intelligence biosensors: Challenges and prospects,阐述了未来智能传感的发展方向(Biosens. Bioelectron., 2020, 165, 112412.)。
(三)多功能纳米诊疗平台
张学记教授团队围绕多功能纳米诊疗平台的构建,以肿瘤个性化精准诊疗为目标,在有机融合多模态成像及光学治疗手段的研究中取得系列成果(图3)。实现体内肿瘤部位光动力疗法应用(Angew. Chem. Int. Ed., 2020, 59, 4354)。开创性地利用藻类提取物“插层”方法,发展了尺寸可控、环保、高产的V2C纳米片制备手段,得到具有良好光热性质的“多效合一”单层V2C纳米片,对肿瘤进行近红外光热、光声和磁共振多模式精准诊断及光热治疗(Angew. Chem. Int. Ed., 2020, 59, 6601)。构建了一种红细胞与癌细胞膜杂化仿生细胞膜,用于修饰纳米载药颗粒,赋予纳米颗粒长的血液循环时间和肿瘤同源靶向能力,实现了高效的黑色素瘤的光热/化学协同治疗(ACS Nano, 2018, 12, 5241,高被引论文,ESI, 1%)。构筑了不对称尿素酶驱动的血小板仿生递药系统,直接将内源性的酶与细胞相结合,实现在尿素燃料存在下长时间的自主运动,提高了载药血小板的靶向治疗效果(Sci. Robot., 2020, 5, eaba6137)。提出“开源节流”自由基(ROS)治疗新策略,此纳米探针通过增加肿瘤微环境的ROS生成并减少ROS消耗,在体外和体内都可以有效抑制肿瘤生长,为ROS用于癌症治疗提供新策略(Nat. Commun., 2020, 11, 1735)。
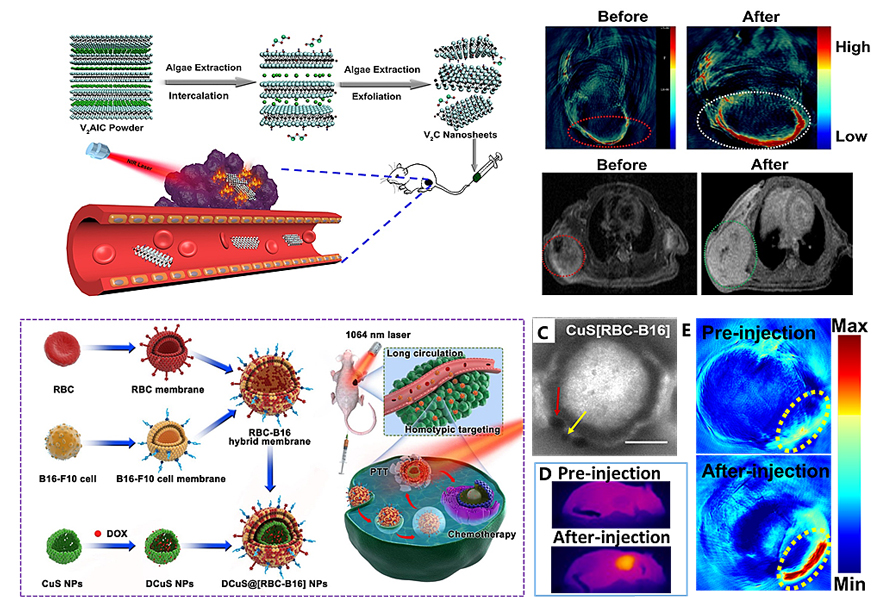
图3. 多功能纳米诊疗技术

张学记北京科技大学团队

张学记深圳大学团队
导师介绍
张学记
https://www.x-mol.com/university/faculty/8847
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号