集成化前处理技术助力高灵敏度蛋白互作组解析
蛋白质是生命活动的实际执行者,解析蛋白质相互作用网络对于深刻理解生命活动过程以及疾病发生发展机理至关重要。亲和纯化-质谱(Affinity purification – mass spectrometry, AP-MS)是一种经典的分析策略,已被广泛应用于解析蛋白复合物的组成以及其动态变化。传统的AP-MS样品前处理流程包括基于多肽探针或者标签抗体的亲和富集、非特异性吸附蛋白的去除、蛋白酶解、洗脱以及除盐。这一过程不仅步骤冗长,而且由于涉及到多步大体积的溶液置换,样品损失较大,因此通常需要数百微克乃至毫克级别的细胞裂解物。灵敏度的限制使得传统的AP-MS工作流程较难应用于样品量较少(如临床样本)或者需要昂贵的长链多肽作为配体时的蛋白相互作用分析实验。
针对上述问题,南方科技大学理学院化学系的田瑞军教授(点击查看介绍)团队发展了一种基于Spintip的集成化AP-MS样品前处理技术FISAP,可用于多通道以及高灵敏度蛋白相互作用组的质谱解析。FISAP装置简单易用,通过将亲和纯化填料注入C18除盐Spintip即可完成组装。通过利用SDS可调控C18对蛋白/多肽的吸附能力这一特性,所有的AP-MS蛋白样品前处理步骤,包括亲和纯化、蛋白的还原/烷基化/酶解、TMT同位素标记、多肽除盐均可在这一装置中以离心力驱动的方式快速实现(操作时间小于4小时)。此外,得益于集成化设计的优越性,使用FISAP技术完成AP-MS实验所需的蛋白样品以及多肽探针用量相较于传统方法大幅度下降。
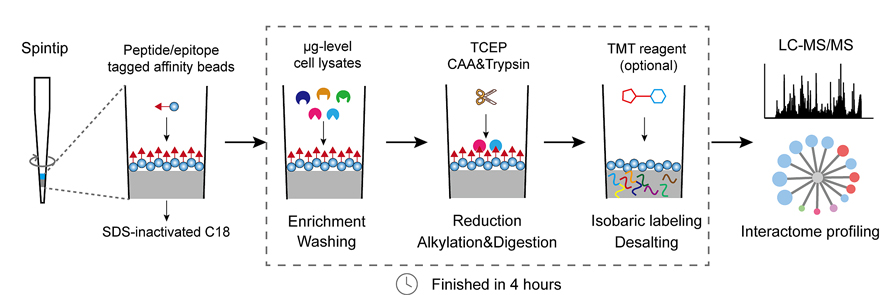
图1. FISAP的操作流程以及原理示意图
在系统优化了FISAP的技术环节之后,作者合成了CD28膜内区上16个氨基酸长度结构域的磷酸化和非磷酸化多肽探针对FISAP的性能进行了考察。在使用50 μg蛋白作为起始样品的情况下,FISAP能有效绘制出CD28膜内区磷酸化依赖的相互作用网络,且定量性能显著优于传统方法。在此基础上,为了进一步提高FISAP技术的灵敏度以及通量,作者优化了一种能有效节省TMT试剂使用量的C18固相同位素标记策略,并将其整合进了FISAP工作流程中。得益于TMT标记的样品在一级质谱(MS1)中的累积效应,FISAP的灵敏度和定量精确性进一步提高,每个通道最低仅需要1 μg的蛋白样品即可完成一次AP-MS实验。最后,作者将FISAP技术的应用场景拓展到了基于标签抗体的免疫沉淀质谱(IP-MS)分析之中。通过构建FLAG-ILK/GFP过表达细胞系,作者使用每个通道仅5 μg的起始样品就成功鉴定了IPP复合物(ILK-PARVA-PARVB-LIMS1-RSU1)的组成。
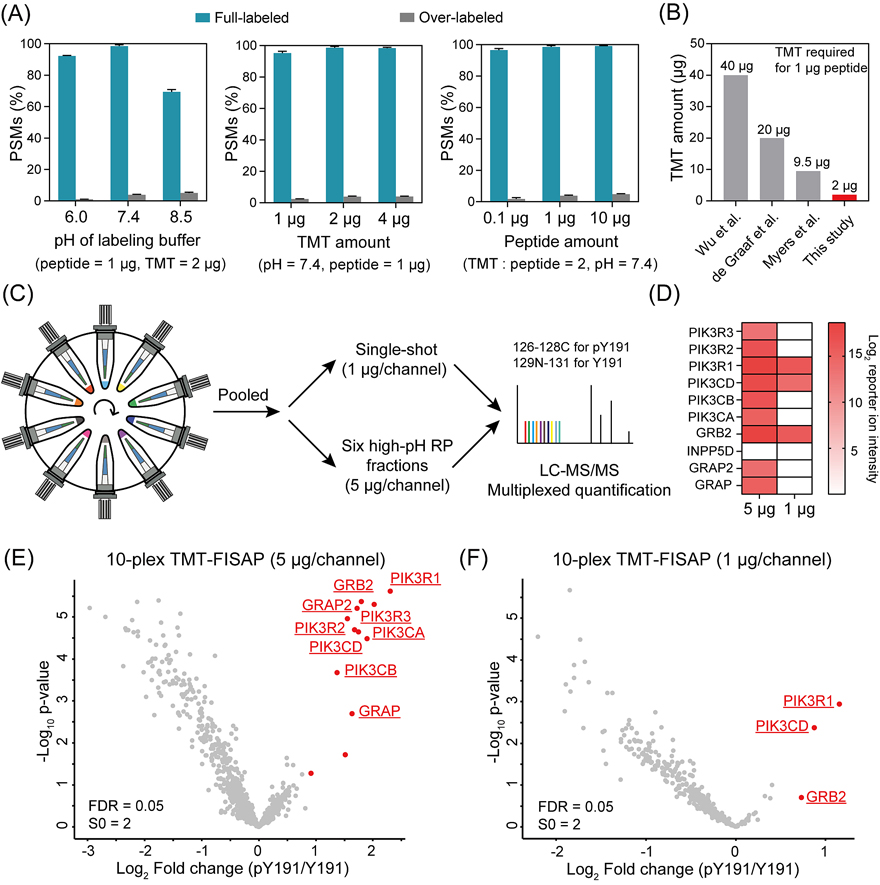
图2. TMT-FISAP用于CD28相互作用组的解析
这一研究成果近期发表于Analytical Chemistry 上,南方科技大学理学院化学系田瑞军教授为论文通讯作者,文章的第一作者是南方科技大学博士生毛亦衡和陈佩忠。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Fully Integrated and Multiplexed Sample Preparation Technology for Sensitive Interactome Profiling
Yiheng Mao, Peizhong Chen, Mi Ke, Xiong Chen, Shanping Ji, Wendong Chen, Ruijun Tian*
Anal. Chem., 2021, DOI: 10.1021/acs.analchem.0c05076
导师介绍
田瑞军
https://www.x-mol.com/university/faculty/49667
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号