NiH催化烯胺不对称氢芳基化构建手性苄胺
手性胺及其衍生物是许多活性药物小分子的重要骨架(图1a),因此科学家们长期致力于开发这类手性化合物的方法,例如烯烃的不对称氢胺化反应构建C–N键,而过渡金属催化的烯胺不对称氢官能团化反应构建C–C键则为这类分子的构建提供了一种补充方法(图1b)。
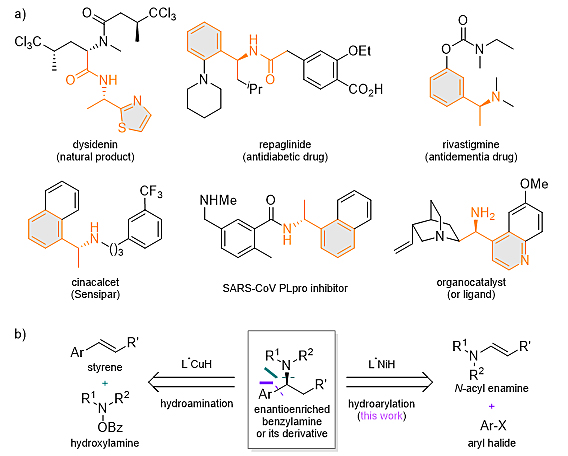
图1. 代表性的手性苄胺分子及其反合成的两种氢官能团化策略
近年来,NiH化学的研究受到国内外化学家们的青睐。前期南京大学团队开发了一种镍氢-双咪唑啉类手性催化剂实现了芳基烯烃的不对称氢芳基化反应,可以实现1,1-二芳基类化合物的不对称合成(Y. He, C. Liu, L. Yu, S. Zhu, Angew. Chem. Int. Ed., 2020, 59, 21530)。在此基础上,为了证明其适用性,作者又将这一催化体系应用到更加富电子的且活性相对更低的N-酰基烯胺的不对称氢芳基化,可以在温和条件下结构多样性地构建手性苄胺(图2)。作者推测该反应过程中对映选择性控制来自于三价镍中间体Ar-Ni(III)-alkyl对映归一性转化。首先,该三价镍中间体发生快速的Ni–C键均裂,得到Ar-Ni(II)-X/烷基自由基对,在手性配体的调控下,该烷基自由基与Ar-Ni(II)-X中间体的重组具有高对映归一性,对映体富集得到单一构型的三价镍中间体,接着经不可逆的还原消除形成对映体富集的芳基化产物。
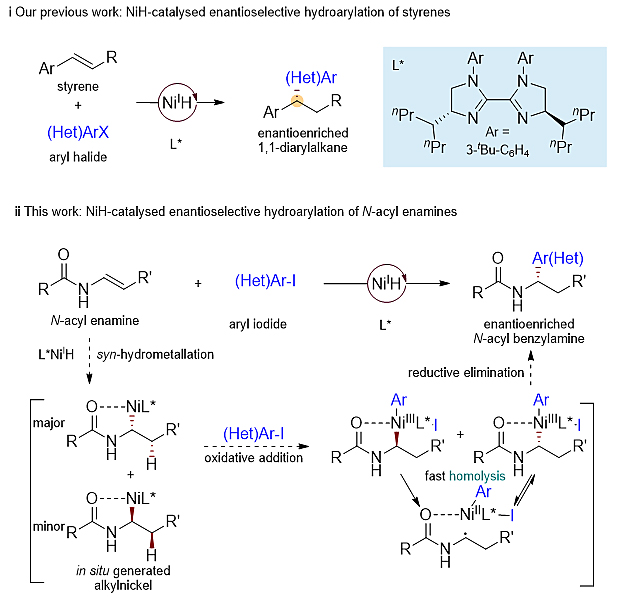
图2. NiH催化烯烃的对映选择性氢芳基化反应
该反应具有底物范围广泛、官能团耐受性良好、反应条件温和等优点(图3)。反应结果表明,富电子的(2a–2e)和吸电子的(2h–2p、2w–2z)芳基碘化物,各种杂环均与体系兼容。同时体系可以应用于具有生物活性和药物分子结构化合物的后期官能团修饰。此外,各种烯酰胺的E和Z异构体都能以很高的产率和优秀的对映选择性得到目标产物。反应体系能够克级放大。
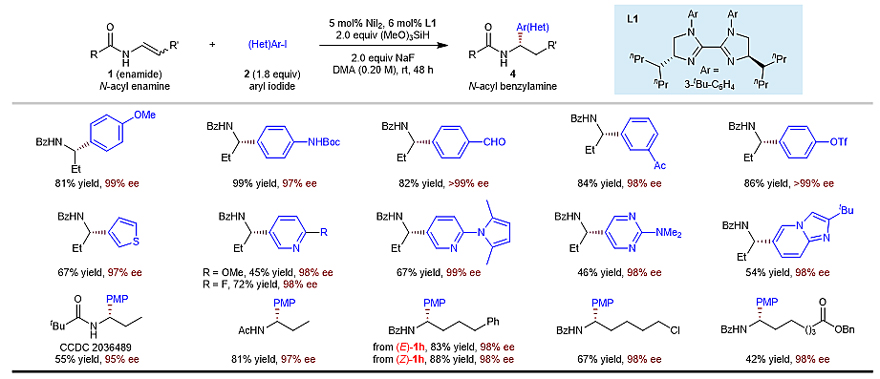
图3. 代表性底物
这一成果近期发表在Nature Communications 上,文章的第一作者是南京大学特任副研究员何玉立博士。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

NiH-Catalyzed Asymmetric Hydroarylation of N-Acyl Enamines to Chiral Benzylamines
Yuli He, Huayue Song, Jian Chen, Shaolin Zhu
Nat. Commun., 2021, 12, 638, DOI: 10.1038/s41467-020-20888-5
导师介绍
朱少林
https://chem.nju.edu.cn/zsl/list.htm
https://www.x-mol.com/groups/slzhu
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号