不对称C-H键官能团化构建手性氮杂螺烯
手性螺烯化合物在不对称催化、材料科学、分子识别等诸多领域中具有非常广泛的应用,因此引起了化学家们的关注。目前其合成方法包括过渡金属催化的炔烃[2+2+2]环加成反应、钯催化芳炔和炔烃的[2+2+2]反应、金催化的分子内炔烃氢芳基化反和有机催化的Fischer吲哚合成反应等。作为螺烯化合物家族的一类重要成员,手性阳离子型氮杂螺烯的获得仍然主要依靠化学拆分或者手性HPLC分离制备,极大影响了其应用研究。因此发展催化不对称反应来高效构建手性氮杂螺烯具有重要的意义。
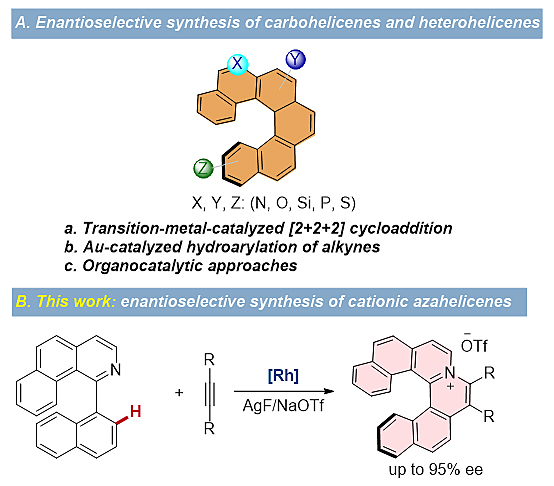
图1. 手性螺烯的催化不对称合成
最近,中国科学院上海有机化学研究所的游书力研究员(点击查看介绍)团队利用自主开发的手性环戊二烯基铑络合物(J. Am. Chem. Soc., 2016, 138, 5242; J. Am. Chem. Soc., 2020, 142, 15678)作为催化剂,手性氨基酸衍生物作为添加剂,从1-芳基苯并异喹啉衍生物和炔烃出发,通过催化不对称C-H键官能团化反应实现了手性阳离子型氮杂螺烯的高效合成。
研究人员发现,在优化条件下各类取代的炔烃衍生物均能参与反应,并以优秀的对映选择性得到阳离子型氮杂[6]螺烯化合物。此外,该方法还可以高效地合成含不同取代基和不同骨架类型的阳离子型氮杂[6]螺烯化合物,反应均表现出非常高的效率和对映选择性。同时,阳离子型氮杂[5]和[7]螺烯化合物也能被高效地合成。
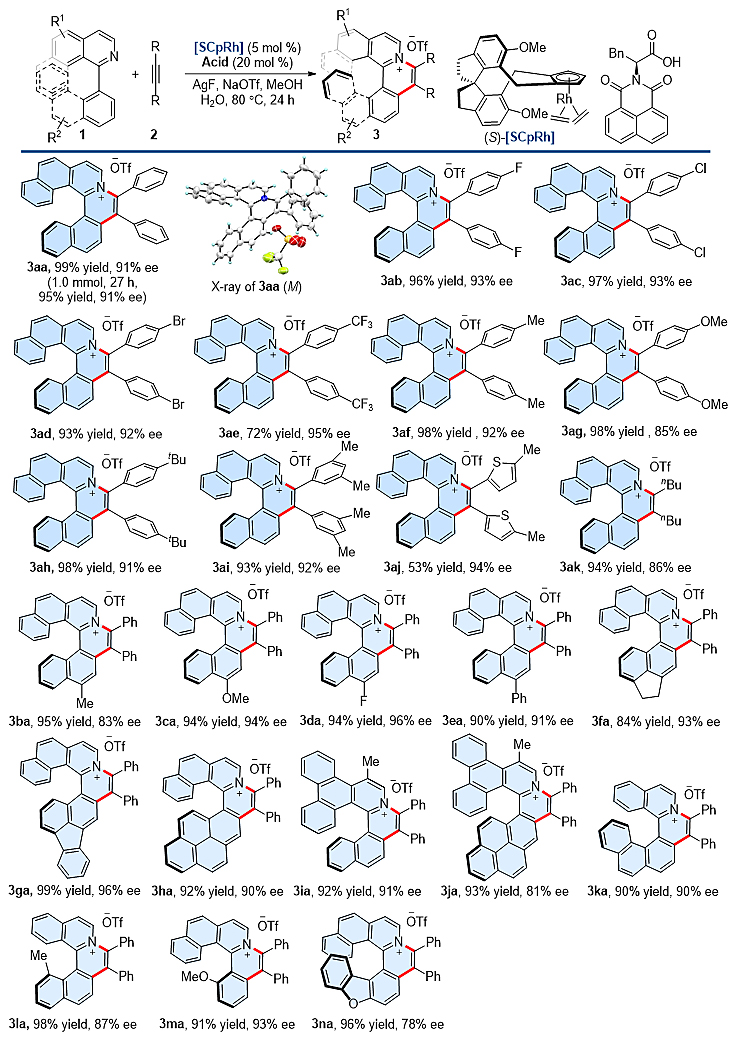
图2. 不对称C-H键官能团化构建氮杂螺烯化合物
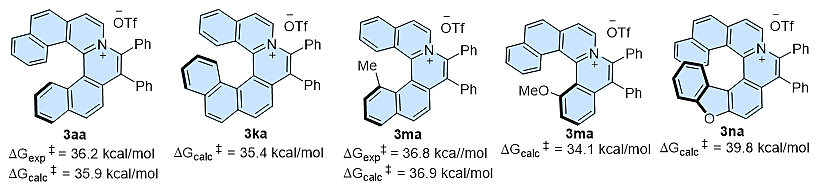
通过DFT计算对代表性的阳离子型氮杂[5],[6]和[7]螺烯化合物对映异构体的互变过程能垒进行了研究。理论计算数值与实验测定的结果表现出很好的一致性,均表明这类螺烯化合物的螺旋手性具有较高的稳定性。
总结
游书力研究员团队实现了金属铑催化1-芳基苯并异喹啉衍生物的不对称C-H键官能团化/环化反应,为手性氮杂螺烯化合物提供了高效的合成方法。相关研究结果发表在近期的J. Am. Chem. Soc.杂志上。文章的第一作者是博士后王强,通讯作者是游书力研究员。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enantioselective Synthesis of Azoniahelicenes by Rh-Catalyzed C–H Annulation with Alkynes
Qiang Wang, Wen-Wen Zhang, Chao Zheng, Qing Gu, Shu-Li You*
J. Am. Chem. Soc., 2021, 143, 114–120, DOI: 10.1021/jacs.0c11735
导师介绍
游书力
https://www.x-mol.com/university/faculty/15598
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号