江苏师范大学石枫课题组Angew:有机小分子协同催化下硝酮与2-吲哚甲醇的区域、对映选择性(3+3)环加成反应
导语:
硝酮是一类应用非常广泛的三元合成砌块,其参与的催化不对称(3+n)环加成反应是合成手性杂环化合物的重要方法。然而,有机小分子催化下硝酮参与的不对称(3+3)环加成反应仍然是一个未知的研究领域。近日,江苏师范大学石枫课题组采用了一种新型的有机小分子协同催化策略——手性磷酸与六氟异丙醇的协同催化策略,实现了硝酮与2-吲哚甲醇的区域选择性和对映选择性(3+3)环加成反应。相关论文发表于Angew. Chem. Int. Ed.。
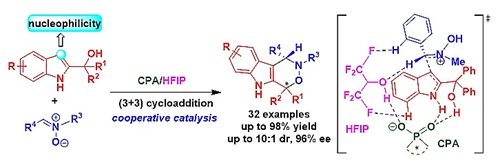
硝酮是一类应用非常广泛的三元合成砌块,其参与的催化不对称(3+n)环加成反应是合成手性杂环化合物的重要方法(图1)。其中,硝酮参与的催化不对称(3+2)环加成反应已经发展地较为成熟,但是大多数反应需要在金属催化下才能实现,仅有少数反应能够在有机小分子催化下实现(图1a)。与之相比,硝酮参与的催化不对称(3+3)、(3+4)环加成反应近几年也得到了快速发展,但都是在金属催化下实现的(图1b-1c)。值得注意的是,硝酮参与的催化不对称(3+3)环加成反应是对映选择性构建六元杂环骨架的重要方法。目前已发展的与硝酮进行催化不对称(3+3)环加成反应的合成砌块主要包括:环丙烷衍生物、三亚甲基甲烷衍生物、乙烯基偶氮乙酸酯以及烯基金物种等。虽然有了这些研究进展,但是有机小分子催化下硝酮参与的不对称(3+3)环加成反应仍然是一个未知的领域,亟需发展。这一领域主要有以下三个难题需要解决(图1d):(1)硝酮难以被有机小分子催化剂活化;(2)缺乏既能够被有机小分子活化,又能和硝酮发生不对称(3+3)环加成反应的合成砌块;(3)缺乏合适的有机小分子催化策略,用于控制(3+3)环加成的反应性和对映选择性。因此,实现有机小分子催化下硝酮参与的不对称(3+3)环加成反应非常具有挑战性。
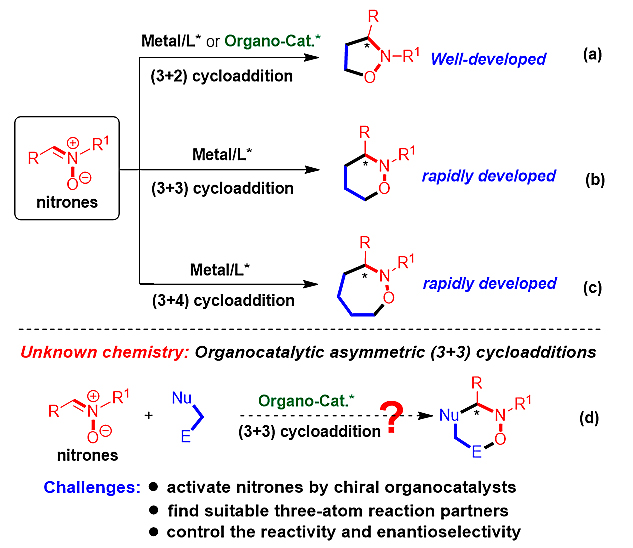
图1. 硝酮参与的催化不对称环加成反应的概况
江苏师范大学石枫课题组基于对吲哚甲醇化学的理解(工作小结: J. Org. Chem., 2017, 82, 7695; Acc. Chem. Res., 2020, 53, 425; 代表性工作: Angew. Chem. Int. Ed., 2017, 56, 116; Angew. Chem. Int. Ed., 2019, 58, 8703; Angew. Chem. Int. Ed., 2019, 58, 3014; Chin. J. Chem., 2020, 38, 543),设想2-吲哚甲醇是否可以作为三元合成砌块,实现有机小分子催化下硝酮参与的不对称(3+3)环加成反应。近年来,2-吲哚甲醇由于其C3位特殊的亲电性,其参与的催化不对称C3亲电取代反应和环加成反应发展地十分迅速(图2a)。然而,2-吲哚甲醇C3位的亲核性反应却几乎没有报道。目前,仅有一例手性磷酸催化下2-吲哚甲醇C3亲核性(4+3)环加成反应(图2b),2-吲哚甲醇参与的其他类型C3亲核性反应仍有待开发。在该类反应中,存在一些挑战性问题(图2c),例如:如何调控2-吲哚甲醇C3位的亲核性和亲电性?如何控制2-吲哚甲醇因不同的C3反应性而产生的区域选择性和对映选择性?因此,开发新颖的策略实现2-吲哚甲醇的催化不对称C3亲核性反应具有重要的研究价值。

图2. 2-吲哚甲醇参与的催化不对称反应的概况
为了发展有机小分子催化下硝酮参与的不对称(3+3)环加成反应,以及开发2-吲哚甲醇参与的新型催化不对称C3亲核性反应,作者设计了手性磷酸催化下硝酮与2-吲哚甲醇的不对称(3+3)环加成反应。选择手性磷酸作为催化剂的原因是考虑到该类催化剂可以通过氢键作用同时活化两种反应物,促使2-吲哚甲醇1的C3位表现出亲核性,并进攻硝酮2的亚胺基团,进而发生不对称(3+3)环加成反应得到产物3。这一设计不仅可以实现首例有机小分子催化下硝酮参与的不对称(3+3)环加成反应,而且可以实现首例2-吲哚甲醇参与的C3亲核性催化不对称(3+3)环加成反应(图3a)。
然而,2-吲哚甲醇和硝酮还有另外一种区域选择性的反应途径,即手性磷酸使2-吲哚甲醇1质子化后脱水,形成C3位具有亲电性的离域碳正离子中间体,然后接受硝酮2中氧负离子的进攻,进而得到另外一种区域选择性的(3+3)环加成产物3'(图3b)。因此,控制好反应性、区域选择性和对映选择性是实现作者所设计的2-吲哚甲醇与硝酮的催化不对称(3+3)环加成反应的关键因素。
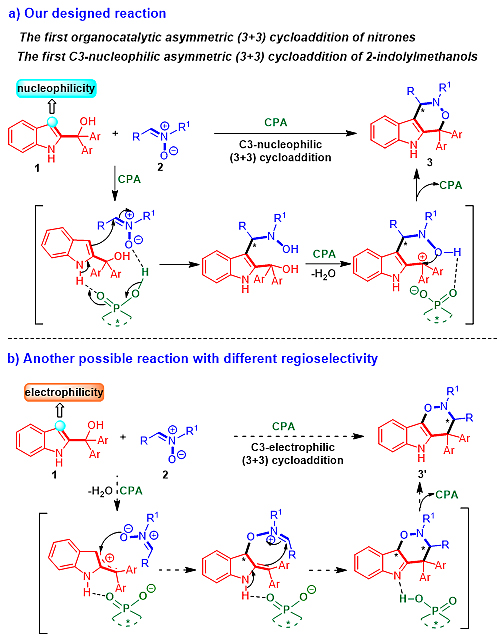
图3. 所设计的反应以及另一种具有不同区域选择性的可能反应
最初,作者选用2-吲哚甲醇1a和硝酮2a作为反应物,进行反应的尝试(表1)。当采用手性磷酸(R)-4a作为催化剂时,可以区域专一性地得到产物3aa,但是收率和立体选择性都很低(entry 1, 26% yield, 11% ee),这说明控制该反应的反应活性和对映选择性都具有很大的挑战性。由于协同催化具有突出的优势,作者希望通过手性磷酸与其他有机小分子协同催化的策略来解决这一挑战性问题。考虑到六氟异丙醇(HFIP)是一种对有机反应具有特殊作用的添加剂,因此,作者尝试了手性磷酸和HFIP的协同催化策略。结果发现,在反应体系中加入HFIP后,反应的收率和对映选择性都有了很大的提高(entry 2, 64% yield, 45% ee),这说明HFIP是手性磷酸的一种优良的共催化剂。随后,在HFIP和手性磷酸的共催化模式下,作者对手性磷酸、溶剂、温度等反应条件进行了仔细的筛选,最终以95%的收率和95% ee得到了目标产物3aa。

表1. 反应条件的筛选
随后,作者对底物的适用范围进行了研究(图4),带有不同取代基的2-吲哚甲醇1和硝酮2都能很好地适用于此反应,高收率、高对映选择性地得到(3+3)环加成产物3。在反应中,作者没有观察到另一种区域选择性产物3'的生成,说明此反应具有高度的区域专一性。
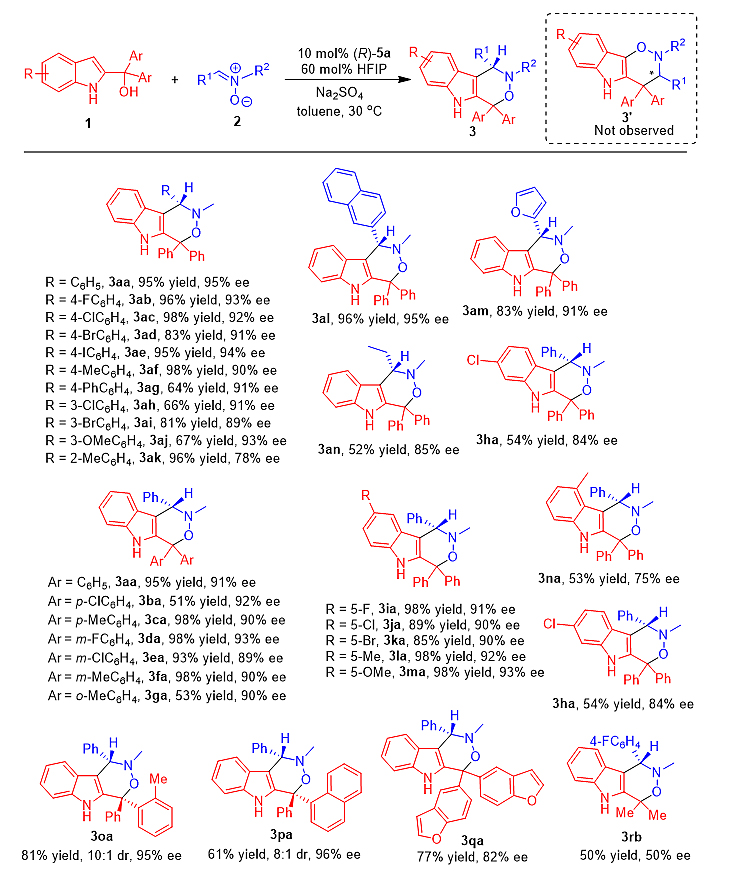
图4. 底物的适用范围
为了研究反应的实用性和产物的用途(图5),作者进行了放大量实验以及衍生化实验,获得了优良的收率,对映选择性也基本能保持。通过对产物进行抗肿瘤活性研究,发现一些化合物对人体前列腺肿瘤细胞具有较好的细胞毒活性。
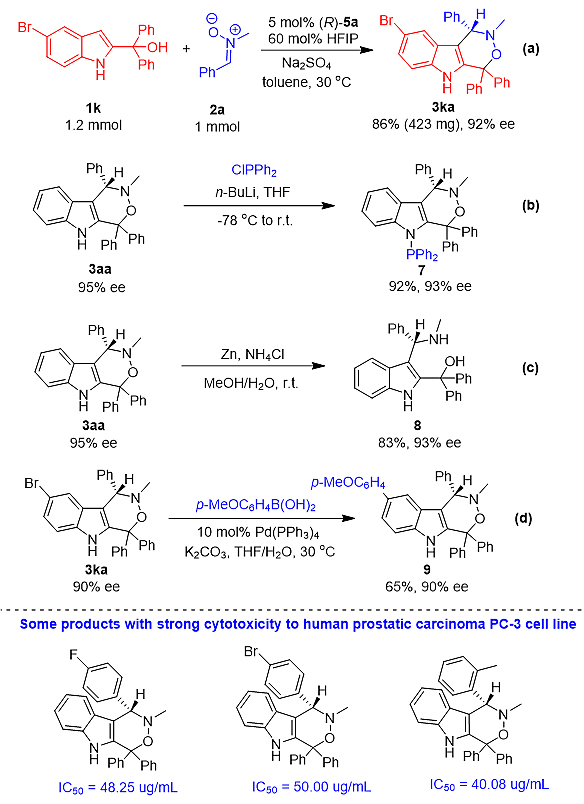
图5. 反应的实用性和产物的生物活性
为了深入研究HFIP在此反应中的作用,作者进行了一系列控制实验(表2)。当不加HFIP时,反应能够发生,但是收率和ee值都不好,这说明HFIP不仅能够提高反应活性,还对对映选择性控制起重要作用。不加手性磷酸无法得到产物,说明单纯使用HFIP不能催化该反应。当使用三氟乙醇代替HFIP时,反应也能发生,但是收率和ee值都有所降低。当使用不含氟原子的异丙醇以及正丁醇代替HFIP时,几乎得不到产物。以上结果说明含氟原子的醇,特别是HFIP对此(3+3)环加成反应具有独特的协同催化效果,这可能与该类醇中的氟原子有关。
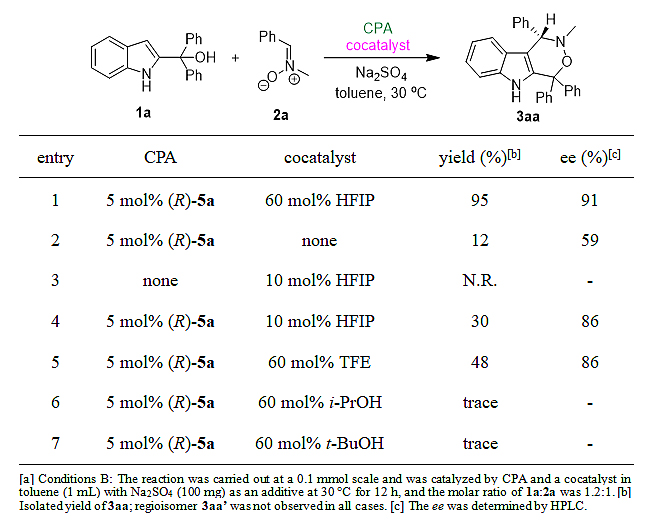
表2. 探究HFIP作用的控制实验
作者还通过高分辨质谱对反应中可能的中间体进行了监测(图6),发现了较弱的中间体A的信号以及较强的中间体B的信号,这表明此(3+3)环加成反应是分步反应,即2-吲哚甲醇的C3位先进攻硝酮的亚胺基团,然后才发生分子内环化反应。此外,作者将2-吲哚甲醇的NH用甲基保护后,反应不能发生,这说明吲哚的NH和催化剂形成的氢键对底物的活化具有重要作用。

图6. 探究可能的反应中间体和活化模式
为了深入研究HFIP的作用和反应的机制,在实验基础之上,作者对反应的可能路径进行了理论计算(图7)。计算显示,硝酮2a首先和手性磷酸(R)-5a作用,形成中间体C。该过程使硝酮的氧负离子变成羟基,不仅降低了硝酮的亲核性,而且使2-吲哚甲醇难以形成离域的碳正离子,从而难以得到具有另一种区域选择性的产物3'(图7a)。因此,这个计算结果解释了区域专一性得到产物3的原因。
接着,作者分别计算了手性磷酸和HFIP协同催化的反应路径A以及单一手性磷酸催化的反应路径B。计算发现,在路径A中(图7b),手性磷酸和HFIP不仅在形成手性中心的关键过渡态TS-1中通过多重氢键模式活化反应物,而且在后续步骤的过渡态TS-2及TS-3中也产生多重氢键的活化作用。因此,HFIP作为手性磷酸的共催化剂,在整个反应过程都发挥着重要的作用。而在路径B中(图7c),只存在手性磷酸对反应物的氢键活化模式。
为了解释HFIP在反应中的作用,作者将路径A和路径B的自由能进行了对比(图7d),在大多数步骤中,路径A的过渡态能垒显著低于路径B。例如,过渡态TS-1和TS-1'是形成手性中心的关键步骤,路径A中TS-1的能垒(20.39 kcal‧mol-1)远远低于路径B中TS-1'的能垒(29.85 kcal‧mol-1),这有力地说明了路径A比路径B更容易发生。此外,路径A整个过程的能垒为8.41 kcal‧mol-1 (从零点到TS-2),比路径B的能垒19.21 kcal‧mol-1(从零点到TS-3')低很多。这些结果表明,HFIP作为共催化剂可以显著降低关键过渡态的能垒和整个反应过程的能垒。

图7. 通过理论计算研究HFIP的作用和反应的路径
为了进一步理解HFIP与手性磷酸的协同催化模式,作者对比了路径A和路径B中关键过渡态的结构(图8)。在形成手性中心的过渡态TS-1中,HFIP与其他试剂形成了四重氢键作用。具体而言,HFIP的羟基与手性磷酸阴离子以及硝酮前手性中心的C-H同时形成两个氢键,更重要的是,HFIP的两个氟原子分别与两个底物中苯环的C-H形成C-H•••F的氢键作用(2.420 Å和2.462 Å,在红色椭圆形中)。此外,手性磷酸的P=O基团还与2-吲哚甲醇的O-H和N-H基团形成了两个氢键。因此,在这种协同催化体系中,HFIP与手性磷酸这两种催化剂与底物形成了多重氢键作用,就像螃蟹的两个钳子紧紧地抓住底物,从而固定了两个底物发生亲核加成反应时的空间取向,这对控制该关键步骤的对映选择性起到了重要作用。与之相比,在TS-1'中,手性磷酸与底物之间的氢键作用较弱,从而导致TS-1'的能垒远高于TS-1 (9.46 kcal‧mol-1)。
当对比路径A和路径B中后续步骤的过渡态TS-2和TS-2'以及TS-3和TS-3'时,也存在类似的情况。即在过渡态TS-2及TS-3中,不仅HFIP的羟基与手性磷酸的P=O基团形成氢键,而且HFIP的氟原子与底物形成N-H•••F或C-H•••F的氢键作用,从而能够很好地活化底物。与之相比,在TS-2'和TS-3'中,由于没有HFIP作为共催化剂,手性磷酸与底物的氢键作用比较弱,从而导致过渡态的能垒较高。
因此,理论计算的结果阐明了HFIP作为手性磷酸共催化剂的作用,该作用不仅可以稳定反应的关键过渡态,而且可以产生一种手性控制的环境,从而对提高2-吲哚甲醇与硝酮发生(3+3)环加成反应的反应活性和控制反应的对映选择性发挥重要作用。
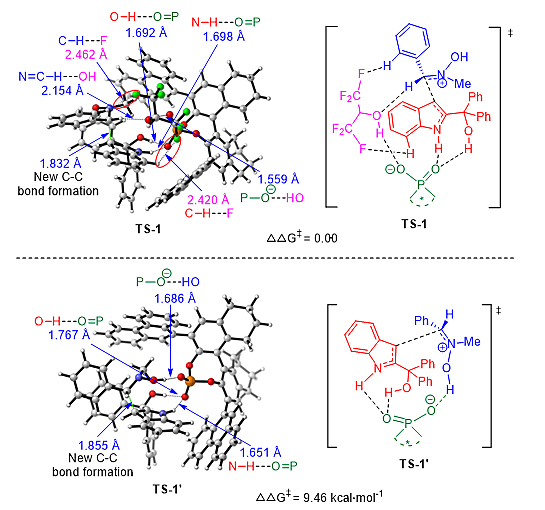
图8. 对比两种路径中关键过渡态TS-1和TS-1'
综上所述,石枫课题采用六氟异丙醇与手性磷酸协同催化的策略,实现了硝酮与2-吲哚甲醇的区域专一性和对映选择性(3+3)环加成反应,高效、高选择性地构建了手性吲哚并六元杂环骨架。该反应不仅实现了第一例有机小分子催化下硝酮参与的(3+3)环加成反应,而且代表了首例2-吲哚甲醇参与的C3亲核性不对称(3+3)环加成反应。更重要的是,理论计算阐明了HFIP作为手性磷酸共催化剂的作用方式,该作用不仅可以稳定反应的关键过渡态,而且可以产生一种手性控制的环境,从而提高反应活性和控制反应的对映选择性。这一研究不仅丰富了硝酮和2-吲哚甲醇的化学,而且为不对称协同催化领域增加了新的内容。
上述研究成果发表在Angew. Chem. Int. Ed.,江苏师范大学硕士研究生李天真为第一作者,实验部分由石枫教授和张宇辰副教授共同指导完成,理论计算部分由湖南科技大学硕士研究生邓双在石枫教授和焦迎春副教授共同指导下完成。该项工作得到了国家自然科学基金和江苏省自然科学基金的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Regio‐ and Enantioselective (3+3) Cycloaddition of Nitrones with 2‐Indolylmethanols Enabled by Cooperative Organocatalysis
Tian-Zhen Li, Si-Jia Liu, Yu-Wen Sun, Shuang Deng, Wei Tan, Yingchun Jiao, Yu-Chen Zhang, Feng Shi
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202011267
石枫教授课题组简介

江苏师范大学石枫课题组成立于2013年,课题组指导教师目前包括石枫教授(中间)、张宇辰副教授(左一)、谭伟讲师(右一),课题组学生包括硕士研究生和本科生。课题组对学生的培养理念是“英雄不论出身”,努力把每一个学生都培养成优秀的学生、同龄人中的佼佼者,不放弃任何一个学生。课题组培养的硕士研究生中,有13人获得研究生国家奖学金,有10人以第一作者在业界公认的国际重要科技期刊《J. Am. Chem. Soc.》《Angew. Chem. Int. Ed.》《Chin. J. Chem.》发表高质量学术论文12篇,1人获得“江苏省三好研究生”荣誉称号,有90%以上通过“申请-考核制”考取名校博士研究生。
石枫课题组长期致力于催化不对称构建生物活性手性杂环骨架,尤其是含有吲哚母核的手性杂环骨架。通过设计和开发新型的含有吲哚母核的平台分子及其参与的催化不对称反应,为构建吲哚类手性生物活性杂环骨架提供了高效、高立体选择性的方法(工作总结:Acc. Chem. Res., 2020, 53, 425)。课题组不仅在含吲哚母核的中心手性杂环骨架的催化不对称构建领域取得了标志性成果(代表性工作:Angew. Chem. Int. Ed., 2014, 53, 13912; Angew. Chem. Int. Ed., 2015, 54, 5460; ACS Catal., 2017, 7, 6984; Angew. Chem. Int. Ed., 2018, 57, 5398; Angew. Chem. Int. Ed., 2019, 58, 8703; Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202011267),而且在含吲哚母核的轴手性杂环骨架的催化不对称构建领域取得了原创性成果(代表性工作:Angew. Chem. Int. Ed., 2017, 56, 116; Angew. Chem. Int. Ed., 2019, 58, 8703; Angew. Chem. Int. Ed., 2019, 58, 15104; Chin. J. Chem., 2020, 38, 543; J. Am. Chem. Soc., 2020, 142, 15686),促进了该领域的发展(综述:Chem. Eur. J., 2020, DOI: 10.1002/chem.202001397)。
石枫课题组主页
https://www.x-mol.com/groups/Shi_Feng
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!




























 京公网安备 11010802027423号
京公网安备 11010802027423号