C-糖基转移酶应用于抗糖尿病活性C-糖苷的酶-化学法合成
C-糖基是多种临床药物及活性天然产物的必需药效基团。C-糖苷在自然界中分布局限、结构多样性不足,同时化学法C-糖基化面临选择性差、基团保护与脱保护等挑战,路线长、成本高,而由C-糖基转移酶催化的酶法C-糖基化可克服上述不足。自2009年从水稻中功能鉴定了第一个植物C-糖基转移酶以来,已有10余个植物C-糖基转移酶被发现,但这些C-糖基转移酶对底物结构有严格的要求,大都难以催化不含酰基的苷元,制约了C-糖基转移酶在药物合成及发现中的应用。
中国医学科学院药物研究所戴均贵(点击查看介绍)团队与叶菲(点击查看介绍)团队从中药芦荟发现了一个新颖C-糖基转移酶AbCGT。AbCGT能罕见催化不含酰基的芳香酚类化合物进行高效C-糖基化,结合化学法合成了具有良好SGLT2抑制活性和选择性的新颖C-糖苷,研究结果对抗糖尿病创新药物的发现及绿色合成具有重要意义(图1)。
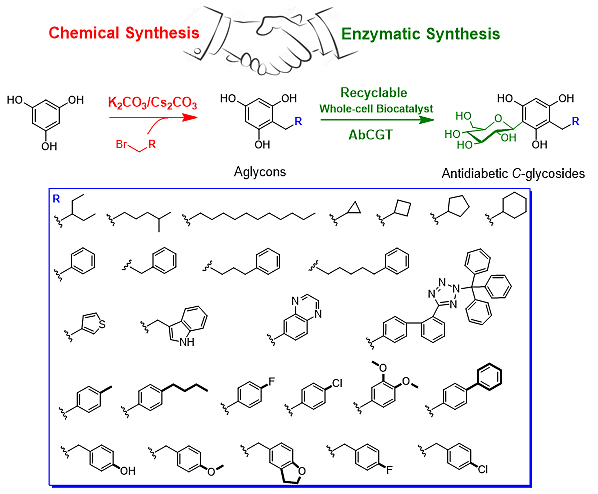
图1. 抗糖尿病活性C-糖苷的酶-化学法合成
研究者首先利用化学法一步合成多种苷元,再利用酶法高效选择性引入C-糖基,实现了结构多样新颖C-糖苷的酶-化学法合成。同时,研究团队针对C-糖苷对分子靶点SGLT2的生物活性及其作用特征进行了研究,发现了16个具较强SGLT2抑制活性的新颖C-糖苷(图2),并探讨了构效关系。通过进一步SGLT2选择性评价和3种动物模型的控制血糖水平的药效评价,确定了一个具有药物开发潜力的新颖C-糖苷46a(图3)。随后,研究者构建了全细胞催化合成体系用以合成目标活性分子。在该体系中重组工程细胞作为催化剂可被多次重复利用,且无需添加昂贵的UDP-葡萄糖供体,目标活性C-糖苷的理论累计产量可达3.95 g/L,实现了其绿色、经济合成。该研究不仅为C-糖基转移酶的实际应用提供了方向,亦为抗糖尿病创新药物发现提供了先导化合物。

图2. 从细胞水平评价C-糖苷的SGLT2抑制活性
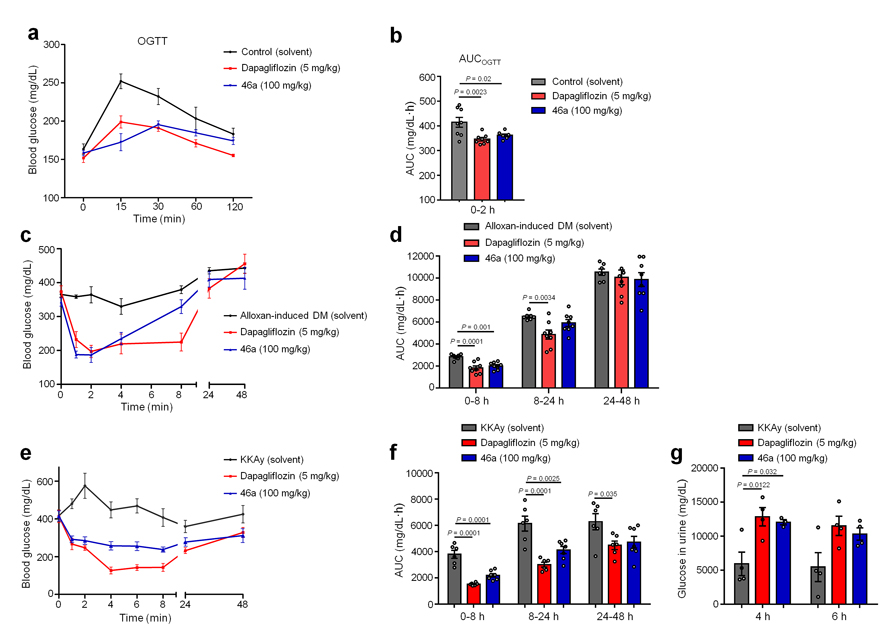
图3. 从动物水平评价C-糖苷46a的抗糖尿病活性
这一成果近期发表在Nature Communications 上。药物研究所戴均贵研究员、叶菲研究员、解可波副研究员为该文的共同通讯作者,解可波与张晓琳博士为论文的共同第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Exploring and applying the substrate promiscuity of a C-glycosyltransferase in the chemo-enzymatic synthesis of bioactive C-glycosides
Kebo Xie, Xiaolin Zhang, Songyang Sui, Fei Ye, Jungui Dai
Nat. Commun., 2020, 11, 5162, DOI: 10.1038/s41467-020-18990-9
解可波副研究员简介:
https://www.x-mol.com/university/faculty/224717
http://www.imm.ac.cn/cn/teacherinfo.asp?rstid=2306
叶菲研究员简介:
https://www.x-mol.com/university/faculty/27265
http://www.imm.ac.cn/cn/teacherinfo.asp?rstid=245
戴均贵研究员简介:
https://www.x-mol.com/university/faculty/27240
http://www.imm.ac.cn/cn/teacherinfo.asp?rstid=228
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



























 京公网安备 11010802027423号
京公网安备 11010802027423号